Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
ELECTROCHEMICAL SYNTHESIS OF PACHYCARPINE, BIOLOGICALLY ACTIVE SUBSTANCE
В Казахстане произрастает более 20 тысяч видов растений, 6 тысяч из них содержат биологически активные вещества (БАВ). Из этих шести тысяч 600 видов можно использовать как полуфабрикат для производства лекарственных веществ, а из более 500 видов можно получать готовые лекарственные препараты.
Но существующие технологии производства лекарственных препаратов очень трудоемки, многостадийны и энергоемки. Кроме того, чистота получаемых продуктов оставляет желать лучшего, поэтому они не конкурентоспособны на мировом рынке. В связи с этим определенный интерес представляет поиск других, более эффективных методов получения БАВ на основе растительного сырья Республики Казахстан (РК). Из растительного сырья путем экстракции получают лекарственные препараты: морфин, кодеин, папаверин и т.п., а сопутствующие алкалоиды идут в отвал, т.к. некоторые из них проявляют токсичность, другие малоэффективны, а некоторые вообще не обладают фармакологической активностью. До настоящего времени эти побочные продукты находятся в складских помещениях нереализованными. Но структуры этих алкалоидов позволяют получать на их основе уже известные или же новые БАВ путем изменения их структуры, введения новых функциональных групп –ОН, –ОСН3, –ОС2Н5, –NO2, димеризация и т.д. [1, 2].
Целью данной работы является электрохимический синтез БАВ ‒ пахикарпина на основе алкалоидов группы d-спартеина: афиллина и афиллидина.
Для проведения электролиза при постоянном значении потенциала электрода использовался потенциостат ПЭБ-20. Электролиз проводили в стеклянном электролизере с керамической диафрагмой, пропитанной жидким стеклом. Система термостатирования состояла из ультратермостата U-10 (теплоноситель – вода). Перемешивание проводилось с помощью магнитной мешалки. Потенциалы электродов контролировались относительно ртутно-сульфатного полуэлемента. Концентрация исходных и конечных веществ в процессе электролиза контролировалась путем титрования кремневольфрамовой кислотой. Определение состава и количественного содержания газообразных продуктов осуществлялось с помощью газоанализатора КГИ-2. Для электроокисления или электровосстановления природных гетероциклических соединений обычно используются чаще всего Hg или Pb электроды, хотя имеются случаи электролиза и на других материалах электродов [1–4].
В данной работе с целью выбора материала катода для электровосстановления смеси алкалоидов афиллина и афиллидина в пахикарпин были предварительно исследованы металлы как с высоким, так и с низким перенапряжением водорода. На основании результатов поисковых опытов в качестве материала катода был выбран ‒ Pb.
Методы идентификации конечных продуктов
Разделение и анализ конечных продуктов электросинтеза проводились с помощью тонкослойной хроматографии на пластинах «Syllifol» (Чехия). Элюирование проводили экспериментально подобранными системами растворителей (хлороформ-метанол-бензол) в соотношении 1:0,5:0,1 об. Установление строения полученных целевых веществ проводились путем снятия ИК-, ЯМР- и масс-спектров. Снятие ИК-спектров проводились на двулучевом спектрофотометре «Specord-75J» (400–4000 см–1). Для снятия ЯМР-спектров использовались приборы «Varian-S-100XL» (США) с частотой 100 МГц и «Hitahi» (Япония) частотой ‒ 60 Мгц. Спектры снимались при t = 25 °С и концентрации 20–30 мг/0,5 мл СНСl3 или D2O. Масс-спектр снимался на масс-спектрометре «Varian-MAT-313» (США) при напряженности электронного поля Е = 60 эВ и t = 25 °С без растворителя.
Электрохимическое восстановление афиллина и афиллидина в пахикарпин
При производстве анабазина гидрохлорида ‒ лекарственного препарата из алколоидов «Anabasis appilla» образуются отходы в виде смеси алкалоидов: лупинина, афиллина, афиллидина и анабазамина в соотношении 0,1:0,8:0,05:0,05 масс. При их разделении на фракции лупинин и анабазамин легко переходят в водорастворимые соли хлоргидраты. А смесь афиллина и афиллидина относится к высококипящей фракции, и для их разделения на отдельные компоненты требуются дополнительные реактивы и расходы. Поэтому для получения пахикарпина нами в качестве исходного сырья была использована смесь афиллина и афиллидина. Электрохимическое восстановление смеси афиллина и афиллидина в соотношении концентрации 1:1 масс. проводилось в водном растворе Н2SO4 в интервале концентрации электролита 1,0:2,5 М. Электролиз при контролируемом потенциале свинцового катода проводился в интервале Е = 0,60:1,25 В
Влияние концентрации электролита
Влияние природы электролита и рН среды на процесс электровосстановления рассматривался в ряде работ [5,9–12]. Авторами отмечается влияние кислотности среды на выход целевых продуктов при восстановлении ряда гетероциклических соединений. На рис. 1 приведена зависимость выхода по веществу (ВВ %) и выхода по току (ВТ %) от концентрации электролита.
Как заметно из рис. 1 и как было отмечено выше, концентрация свободной серной кислоты благоприятно влияет на процесс. Вместе с тем, как видно из рис. 1, кривые зависимости ВВ % (кривая-1) и ВТ % (кривая-2) от концентрации электролита проходят через максимум при = 1,4 М. По-видимому, максимум обусловлен образованием солей исходных афиллина и афиллидина в растворе электролита и увеличением скорости диффузии на поверхность свинцового катода в области ДЭС, а также увеличением скорости десорбции конечного продукта пахикарпина от поверхности электрода, что согласуется с данными литературы [6-8].
На рис. 2 показана зависимость выхода пахикарпина ВВ % и ВТ % от потенциала свинцового катода: кривая 1 – ВВ %, кривая 2 – ВТ %.
Влияние плотности тока
Электрохимическое восстановление протекает в довольно широком диапазоне катодных плотностей тока: от 0,01 до 0,1 А/см2.
Как видно, повышение плотности тока благоприятно влияет на выход целевого продукта. На рис. 2 видно, что выход пахикарпина проходит через максимум при Е = –1,2 В. С дальнейшим повышением потенциала катода выход продукта уменьшается, что, по-видимому, связано с десорбцией исходного афиллина и афиллидина. Как известно, органические вещества могут адсорбироваться на поверхности электрода при определенном потенциале. Е = –1,2 В, по всей видимости, соответствует тому потенциалу, когда наблюдается максимальная адсорбция исходных веществ. Препаративное электровосстановление смеси афиллина и афиллидина при контролируемом потенциале Pb-катода показало, что образование целевого продукта происходит при Е = –0,95:–1,25 В. Электролиз при Е = –0,95 ± 0,3 В, как показал анализ состава раствора, приводит к полному восстановлению афиллидина до афиллина. Максимальный выход целевого продукта электролиза пахикарпина образуется при Е = –1,2 В.
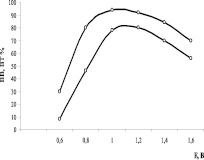
Рис. 1. Зависимость выхода по ВВ % и ВТ % пахикарпина от концентрации электролита H2SO4
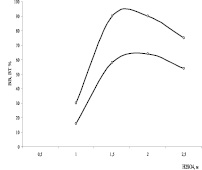
Рис. 2. Зависимость выхода по ВВ % и ВТ % пахикарпина от потенциала катода
Влияние температуры и времени электролиза
Температурную зависимость ВВ % и ВТ % пахикарпина исследовали в пределах 25–40 °С. Влияние времени электролиза на процесс исследовали в интервале 0,5–3 ч.
Обычно катодные процессы проводятся при низких значениях температуры с целью упрощения технологии процесса и получения стабильных, химически устойчивых конечных продуктов. На основании предварительных экспериментов установлено, что влияние температуры процесса на выход целевого продукта – пахикарпина ‒ очень незначительно, увеличение температуры приводит к некоторому уменьшению выхода целевого продукта в основном за счет процессов осмоления конечных веществ.
Методом математического моделирования электросинтеза были определены оптимальные условия ведения процесса: время электролиза τ = 1,2 часа, потенциал катода Ук = +120 В, температура t = 25–30 °С, концентрация исходной смеси Сисх = 0,6 М, концентрация серной кислоты = 1,4 М.
При оптимальных условиях ведения процесса выход по веществу и току пахикарпина составляют 92,0 и 69 % соответственно.
Идентификация конечных продуктов электросинтеза
На основании результатов ТСХ и адсорбционной хроматографии при электровосстановлении смеси афиллина и афиллидина образуются два конечных продукта с Rf = 0,6 (продукт 1) и Rf = 0,92 (продукт 2).
Вещество с Rf -0,92 (продукт 2) составлял основную массу полученных продуктов.
В отличие от ИК-спектра продукта 1 в спектре продукта 2 не наблюдаются полосы поглощения в области 3500 см–1, характерные для гидроксильной группы. В спектре продукта 2 не обнаружен обертон колебаний > С = О лактамной группы в диапазоне частот 3300 см–1, характерный для спектров исходных алкалоидов. Полоса поглощения в спектре начинается при 2920 см–1, образуя два пика с максимумами 2910 см–1, причем очень сильные и широкие с интенсивностью ≈ 90,0 %, что характерно для деформационных колебаний > С – Н2 связей алкалоидов группы d-спертеина. В ЯМР-спектре продукта 2 полностью отсутствуют характерные сигналы функциональных групп. Сигналы при δм.д = 1,25, δм.д = 2,11, δм.д = 2,61 относятся, по-видимому, только к колебаниям протонов > С – Н2 связей, т.к. колебания протонов функциональных групп обыкновенно лежат в более высокой области химического сдвига.
В масс-спектре продукта 2 при электронном ударе образуются основные фрагменты ионов с массой m/e = 97,110,137,197,224. Недиссоциированный ион с m/e = 234 определен как молекулярный. Ион с m/e = 137 является максимальным, интенсивность остальных ионов на рисунке приведена относительно интенсивности максимального иона в %. Образование основного фрагмента с массой m/e = 136,137,138 при электронном ударе Е = 60 эв характерно для алкалоидов группы d-спартеина (пахикарпина). Наибольшая интенсивность фрагмента с m/e = 136 для алкалоидов пахикарпина наблюдается и в работе авторов [10]. Молекулярный ион с М+ = 234 в спектре продукта 2 по массе совпадает с молекулярной массой алкалоида пахикарпина, что дало возможность предположить их идентичность. Поэтому для подтверждения этого предположения были сняты в тех же условиях, что и спектры продукта 2, ИК-, ЯМР- и масс-спектры природного пахикарпина. При сравнении соответствующих спектров продукта – 2 и спектров природного пахикарпина выявлена их полная аналогия.
По результатам анализа ИК-, ЯМР- и масс-спектров природного пахикарпина и вещества – 2, последний был идентифицирован, как пахикарпин[13,14].
Схема реакции и ее обсуждение
По литературным данным, при электровосстановлении гетероциклических соединений, содержащих в своей структуре карбонильные > С = О группы, в зависимости от условий ведения процесса могут образоваться полностью восстановленные гетероциклические углеводороды, гидрокси- или димерные производные. В сернокислых растворах на электродах с высоким перенапряжением в основном образуются углеводороды и гидрооксипроизводные.
На основании результатов вольтамперометрических и емкостных измерений, а также данных анализа по идентификации образование продуктов электровосстановления можно представить следующим образом:
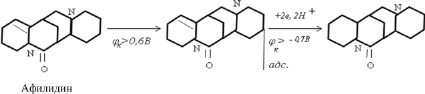
Схема 1
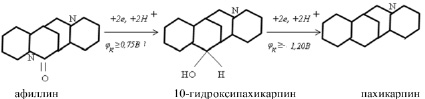
Схема 2
На основании результатов идентификации продуктов электровосстановления смеси афиллина и афиллидина основным продуктом электролиза является пахикарпин.
При Е > –0,6 В афиллидин адсорбируется на поверхности свинцового катода. Максимум адсорбции, по данным вольтамперных и импедансных измерений, находится при Е > –0,95 В. При таком потенциале катода, по-видимому, происходит протонизация связи молекулы афиллидина в положении 5 и 6, по схеме 1, и он переходит в афиллин, который является одним из компонентов исходной смеси.
Афиллин максимально адсорбируется при Е ≥ –1,20 В, при этом потенциале к нему присоединяются 2е и 2Н+ с образованием 10-гидроксипахикарпина по схеме 2. Затем 10-гидроксипахикарпин также принимает 2е, 2Н+ и с замещением гидрокси-группы образуется полностью восстановленное гетероциклическое соединение – пахикарпин. Такая схема процесса хорошо согласуется с данными идентификации продуктов электросинтеза пахикарпина, проведенного при контролируемом потенциале.
Анализ продуктов электролиза при контролируемом потенциале показал, что при Е ≤ –0,6 В не происходит восстановления афиллидина, в основном образуются смолообразные продукты. Афиллидин до афиллина восстанавливается при Е ≥ –0,65 В. Следы 10-гидроксипахикарпина появляются при значении Е = –0,75 В, что, по-видимому, объясняется восстановлением адсорбированного афиллина. С увеличением Е > –0,75 В повышается выход по веществу 10-гидроксипахикарпина и при значении Е ≥ –0,8 В наблюдается образование пахикарпина. Максимальный выход по веществу пахикарпина наблюдается при Е ≥ –1,20 В.
Количественную очистку основного продукта пахикарпина от исходной смеси афиллина и афиллидина можно проводить путем перевода его в водорастворимую соль хлоргидрат пахикарпина.
Заключение
Установлено электрохимическое поведение алкалоидов группы d-спартеина: афиллина и афиллидина. Показана возможность электрохимического восстановления смеси алкалоидов в биологически активное вещество – пахикарпин. Определено влияние экспериментальных факторов на процесс. Сняты ИК-, ЯМР- и масс-спектры целевого продукта пахикарпина. Установлены оптимальные условия ведения процесса.
Рецензенты:
Надиров К.С., д.х.н., профессор, зав. кафедрой «Нефтегазовое дело», ЮКГУ им. М.О. Ауэзова, г. Шымкент;
Шакиров Б.С., д.т.н., профессор, зав. кафедрой «Экология», ЮКГУ им. М.О. Ауэзова, г. Шымкент.
Работа поступила в редакцию 22.11.2013.
Библиографическая ссылка
Имангалиев Т.А., Акилов Т.К., Джалилов К.А., Адиходжаева К.Б., Токтибаева К.Р., Атаханова Н.А., Алпысбаева Е.Т. ЭЛЕКТРОХИМИЧЕСКИЙ СИНТЕЗ БИОЛОГИЧЕСКИ АКТИВНОГО ВЕЩЕСТВА ПАХИКАРПИНА // Фундаментальные исследования. 2013. № 10-12. С. 2644-2648;URL: https://fundamental-research.ru/en/article/view?id=32845 (дата обращения: 30.04.2026).



