Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
SYNTHESIS AND INVESTIGATION OF NEW POLY(1-VYNILIMIDAZOLE) IONOCHROMES
Синтез новых сигнальных систем для эффективного и селективного определения ионов и получение наноматериалов на оптически прозрачных полимерных подложках при помощи ковалентного связывания полученных молекул в поверхностном слое полимера является основной задачей данного исследования [2–9]. Потребность в системах, контролирующих химический состав окружающей среды, диктуется необходимостью постоянного мониторинга химического состава (анионного, катионного и молекулярного) гидросферы, литосферы, атмосферы. Одно из возможных направлений решения этой проблемы связано с использованием наноматериалов, содержащих сигнальные органические молекулы, взаимодействие которых с субстратом генерирует электромагнитный сигнал, регистрируемый визуально или с применением современных физико-химических методов контроля оптических свойств материалов.
Создание эффективной фотодинамической сенсорной системы основывается на тщательном подборе составляющих его частей. В первую очередь – рецептора, отвечающего за селективное распознавание аналита. Во вторую – флуорофора (или, в общем случае, сигнального фрагмента), преобразующего сигнал химического (физического) взаимодействия в оптический или электрический сигнал. Фотодинамические сенсорные системы, содержащие в составе рецепторного фрагмента разнообразные гетероциклические производные, могут быть использованы не только для обнаружения катионов, но и, как показывают последние исследования, в качестве эффективных сенсоров на биологически важные анионы органических кислот.
Целью проводимых работ является синтез и исследование новых ионактивных материалов, содержащих привитые фрагменты, в структуру которых входит как флуорофор, так и дополнительный координационный центр.
Материалы и методы исследования
Спектры ЯМР 1Н получены на спектрометре Varian Unity 300 (300 МГц) в DMSO-d6. В качестве внутреннего стандарта использовались остаточные сигналы (CH3)2SO (d 2,50 м.д.). Электронные спектры поглощения сняты на спектрофотометре Varian Cary 100, спектры люминесценции измерены на спектрофлуориметре Varian Cary Eclipse. Колебательные спектры сняты на приборе Varian Excalibur 3100 FT-IR. Температуры плавления определяли в стеклянных капиллярах на приборе ПТП (М). Полноту протекания реакций и индивидуальность полученных соединений контролировали с помощью ТСХ (пластины Silufol U254, элюент – CHCl3/EtOH, v/v – 5/1, проявление парами йода во влажной камере).
Поли(1-винил)имидазол (1) получен по методу, описанному в работе [1].
Общая методика получения кватернизованных полимеров (7–11, 13, 17–19). Нагревали смесь 1 г поли(1-винил)имидазола, 100 мл 1-бутанола и 5 ммоль (10 или 2,5 ммоль) соответствующего алкилгалогенида (2–6, 12, 14–16) в течение 10–12 ч (для 2–6,12) и 30–35 ч (для 14–16). По окончании реакции растворитель выпаривали на роторном испарителе в вакууме водоструйного насоса до 1/4 объема (7–11, 13) или досуха (17–19). При получении ацетамидных (7–9, 13) и пропионамидных (10, 11) производных остаток разбавляли 50 мл ацетона, тщательно размешивали и кипятили полученную суспензию 15–20 мин. Смесь охлаждали и через ~30 мин осадок отфильтровывали, тщательно промывали на фильтре ацетоном, измельчали и сушили при 100 °С.
В случае солей (17–19) густое масло, полученное после отгонки растворителя, обрабатывали толуолом (~40–50 °С, 3×25 мл), переносили в вакуум-эксикатор и сушили в вакууме над P2O5 до кристаллизации (3–4 дня).
Поли(3-{2-[(антрацен-9-илметил)(S-(-)-1-фенилэтил)амино]-2-оксоэтил}-1-винилимидазолий хлорид)-поли(1-винилимидазол) (7). Выход 71 %. Тпл 112–114 °С (разл.). Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 1,80–3,10 м {(9Н)n, (CH3)n, [(СНСН2)2]n}, 4,40–5,30 м [(3Н)n, (СН)n, (СН2)n], 5,50–6,00 м [(2Н)n, (СН2)n], 6,60–10,00 м [(20Н)n, (HAr)n].
Поли(3-{2-[(антрацен-9-илметил)(2-метоксифенил)амино]-2-оксоэтил}-1-винилимидазолий хлорид)-поли(1-винилимидазол) (8). Выход 77 %. Тпл 154–156 °С (разл.). Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 2,00–3,30 м {(6Н)n, [(СНСН2)2]n}, 4,60–5,50 м [(5Н)n, (OСН3)n, (СН2)n], 5,60–6,10 м [(2Н)n, (СН2)n], 7,00–9,90 м [(19Н)n, (HAr)n].
Поли(3-{2-[(антрацен-9-илметил)(3,5-дихлорфенил)амино]-2-оксоэтил}-1-винилимидазолий хлорид)-поли(1-винилимидазол) (9а). Выход 84 %. Тпл 124–125 °С (разл.). Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 1,60–3,20 м {(12Н)n, [(СНСН2)4]n}, 4,30–5,00 м [(2Н)n, (СН2)n], 5,40–6,10 м [(2Н)n, (СН2)n], 6,60–9,60 м [(24Н)n, (HAr)n].
Поли(3-{2-[(антрацен-9-илметил)(3,5-дихлорфенил)амино]-2-оксоэтил}-1-винилимидазолий хлорид)-поли(1-винилимидазол) (9б). Выход 80 %. Тпл 167–168 °С (разл.). Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 1,70–3,10 м {(6Н)n, [(СНСН2)2]n}, 4,30–5,40 м [(2Н)n, (СН2)n], 5,60–6,50 м [(2Н)n, (СН2)n], 6,80–10,20 м [(18Н)n, (HAr)n].
Поли(3-{2-[(антрацен-9-илметил)(3,5-дихлорфенил)амино]-2-оксоэтил}-1-винилимидазолий хлорид) (9в). Выход 88 %. Тпл 190–191 °С (разл.). Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 2,40–3,40 м {(3Н)n, [(СНСН2)]n}, 4,70–5,30 м [(2Н)n, (СН2)n], 5,50–6,10 м [(2Н)n, (СН2)n], 7,20–9,30 м [(15Н)n, (HAr)n].
Поли(3-{3-[(антрацен-9-илметил)(S-(-) -1-фенилэтил)амино]-3-оксопропил}-1-винилимидазолий хлорид) (10). Выход 88 %. Тпл 184–185 °С (разл.). Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 2,00–3,60 м {(11Н)n, (CH3)n, (CH2)n, [(СНСН2)2]n}, 4,10–5,40 м [(3Н)n, (СН)n, (СН2)n], 5,60–6,50 м [(2Н)n, (СН2)n], 6,80–9,80 м [(20Н)n, (HAr)n].
Поли(3-{3-[(антрацен-9-илметил)(3,5-дихлорфенил)амино]-3-оксопропил}-1-винилимидазолий хлорид) (11). Выход 88 %. Тпл 161–162 °С (разл.). Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 1,80–2,90 м {(6Н)n, [(СНСН2)2]n}, 3,10–3,50 м [(2Н)n, (СН2)n], 4,20–4,80 м [(2Н)n, (СН2)n], 5,40–6,00 м [(2Н)n, (СН2)n], 6,50–9,60 м [(18Н)n, (HAr)n].
Поли{3-[2-оксо-2-(хинолин-8-иламино)этил]-1-винилимидазолий хлорид}-поли(1-винилимидазол) (13). Выход 75 %. Тпл 172–173 °С (разл.). Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 2,00–3,60 м {(6Н)n, [(СНСН2)2]n}, 4,80–6,60 м [(4Н)n, (СН2)n, (СН2)n], 7,20–9,80 м [(21Н)n, (HAr)n].
Поли(3-{2-[(антрацен-9-илметил)амино]этил}-1-винилимидазолий хлорид)-поли(1-винилимидазол) (17). Выход 78 %. Тпл > 220 °С (разл.). ИК спектр, ν, см–1: 3310, 3240, 1600, 1495, 1410, 1240, 1155. Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 1,60–2,60 м {(6Н)n, [(СНСН2)2]n}, 3,30–4,20 м [(4Н)n, (СН2СН2)n]; 5,60–6,40 м [(2Н)n, (СН2)n], 6,70–9,40 м [(15Н)n, (HAr)n].
Поли(3-{2-[(антрацен-9-илметил)(метил)амино]этил}-1-винилимидазолий хлорид)-поли(1-винилимидазол) (18). Выход 64 %. Тпл > 150 °С (разл.). Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 2,00–5,70 м {(13Н)n, (СН3)n, [(СН2СН2)]n, [(СНСН2)2]n]}, 5,70–6,60 м [(2Н)n, (СН2)n], 6,90–9,40 м [(15Н)n, (HAr)n].
Поли(3-{3-[(антрацен-9-илметил)амино]пропил}-1-винилимидазолий хлорид)-поли(1-винилимидазол) (19). Выход 60 %. Тпл > 170 °С (разл.). Спектр ЯМР 1Н, δ, м.д. (DMSO-d6): 1,70–6,50 м {(15Н)n, [(СН2CH2СН2)]n, [(СНСН2)2]n, (СН2)n, (NH)n]}, 6,70–9,00 м [(15Н)n, (HAr)n].
Результаты исследования и их обсуждение
С целью исследования возможности использования поли(1-винилимидазолиевых) материалов, содержащих антраценовый фрагмент, в качестве эффективных сенсоров на катионы и анионы, а также изучения влияния структуры рецепторного фрагмента на ионактивные свойства были синтезированы полимерные материалы с использованием серии новых алкилгалогенидных фрагментов [1].
Так, кватернизацией пиридиновых атомов азота, входящих в состав матрицы, при взаимодействии с алкилгалогенидами различной структуры, такими как N-(антрацен-9-илметил)-N-R1-2-хлорацетамиды (2–4) и N-(антрацен-9-илметил)-N-R1-3-хлорпропионамиды (5, 6), был получен ряд поливинилимидазольных ионохромов (7, 8, 9а-в, 10, 11).
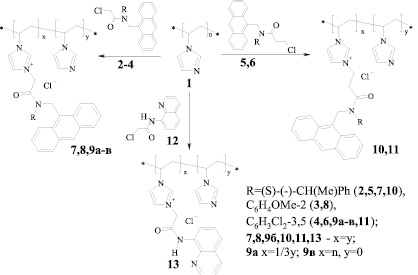
В данном случае взаимодействие протекает в течение 10–12 ч при кипячении реагентов в среде 1-бутанола и в соотношении реагентов (полимер/алкилгалогенид), необходимом для участия в кватернизации половины пиридиновых атомов азота (x = y). При использовании ацетамида (4) для количественной оценки влияния соотношения свободных имидазолиевых фрагментов к кватернизованным на хемосенсорные свойства были получены материалы с соотношением фрагментов x = 1/3y (9a) и x = n, y = 0 (9в). В качестве кватернизующего соединения использовали также 2-хлор-N-(хинолин-8-ил)ацетамид (12). В ЯМР 1Н спектрах всех синтезированных полимерных амидов проявляются характеристические сигналы – группа мультиплетов в области 1,60–3,00 м.д., характеризующих (CH–CH2)n-полимерный фрагмент, и уширенные полосы от СH2-групп (амидной и заместителей при атоме азота). На основании количественных соотношений между сигналами протонов полимерного алифатического фрагмента и CH2-амидных групп установлено, что все полученные соединения соответствуют заявленным структурам.
С применением N-R-N-(антрацен-9-илметил)-N-(2-хлорэтил)амина (14, 15) и N-(антрацен-9-илметил)-N-(3-хлорпропил)амина (16) в качестве алкилирующих агентов получены заряженные полимеры (17–19). В отличие от получения соответствующих полимерных амидов (7–13) при синтезе алкиламиноалкильных производных поли(1-винилимидазола) (17–19) значительно увеличивается время реакции – до 30–35 ч, что обусловлено, прежде всего, меньшей активностью хлора в производных (14–16). Дополнительные сложности при синтезе данных производных связаны с выделением и очисткой конечных продуктов. После удаления растворителя в вакууме полученные полимеры выделяются в виде густых гигроскопических масел, постепенно кристаллизующихся при стоянии в вакуум-эксикаторе над P2O5.
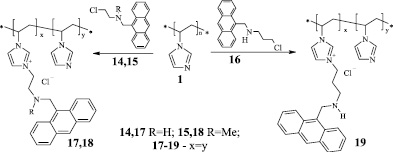
Согласно данным ЯМР 1H спектроскопии имидазолиевые соли (17–19) также полностью соответствуют заявленным структурам и количественному соотношению фрагментов. По данным электронной спектроскопии полимеры (7–11, 17–19) обладают флуоресценцией «классического» антраценового типа – три полосы с λмакс 420–423 нм, в случае хинолинового производного (13) наблюдается флуоресценция с одиночным максимумом в области λмакс 510 нм.
Хемосенсорная активность производных (7–11, 13, 17–19) исследовалась в растворах (с 5∙10–6 моль/л) путем сравнения спектров флуоресценции до и после добавления соответствующих катионов (Zn2+, Cd2+, Ni2+, Cu2+, Pb2+, Hg2+) и анионов (AcO–, CN–, NO3–, F–, Cl-) (рисунок). Изучение хемосенсорной активности полученных полимерных хемосенсоров (7–11, 13, 17–19) по отношению к катионам выявило существенную зависимость структуры сенсора и его направленности (селективности). Так, в случае амидных производных (7–11, 13) наиболее селективной оказывается реакция на ионы Ni2+ [максимальное тушение флуоресценции в 10 раз происходит в случае соединений (7, 13)]. В то же время для аминных систем (17–19) характерным является взаимодействие с катионами Zn2+ и Cd2+, приводящее к значительному разгоранию флуоресценции (таблица).
Относительное изменение интенсивности флуоресценции соединений (4–11, 13) (с 5,0∙10–6 моль/л) в MeCN при добавлении катионов металлов (с 2,5∙10–5 моль/л)
|
Соед. |
Относительное изменение интенсивности флуоресценции, I/I0 |
|||||
|
Zn2+ |
Cd2+ |
Cu2+ |
Ni2+ |
Pb2+ |
Hg2+ |
|
|
7 |
1,0 |
0,9 |
0,6 |
0,1 |
0,7 |
0,7 |
|
8 |
0,9 |
1,3 |
0,7 |
0,2 |
0,6 |
0,6 |
|
9а |
1,1 |
1,0 |
0,5 |
0,2 |
0,6 |
0,6 |
|
9б |
0,9 |
0,9 |
0,8 |
0,3 |
0,8 |
0,7 |
|
9в |
1,0 |
1,0 |
0,8 |
0,7 |
1,0 |
1,5 |
|
10 |
0,8 |
1,0 |
0,6 |
0,5 |
0,6 |
1,2 |
|
11 |
0,9 |
1,2 |
0,5 |
0,4 |
0,8 |
1,2 |
|
13 |
2,8 |
0,7 |
0,4 |
0,1 |
0,5 |
0,6 |
|
17 |
15,0 |
6,0 |
0,4 |
0,8 |
0,9 |
2,0 |
|
18 |
10,0 |
7,0 |
0,7 |
0,9 |
1,0 |
0,8 |
|
19 |
9,0 |
7,0 |
0,6 |
0,8 |
1,0 |
3,0 |
При взаимодействии полученных производных (7-11,13,17-19) с тетрабутиламмониевыми солями наиболее существенные изменения интенсивности флуоресценции вызываются ионами F- и AcO‒.
При возрастании числа амидных фрагментов в ряду 9а–9б–9в происходит увеличение как чувствительности, так и селективности по отношению к ацетат-аниону. Так, добавление NBu4+AcO– (NBu4+F–) к ацетонитрильным растворам солей (9а–в) вызывает увеличение интенсивности флуоресценции в 7,0 (8,0), 9,0 (6,0) и 17,0 (3,0) раз соответственно (см. рисунок).
Для всех полимерных систем (7–11, 17–19), содержащих антраценовый флуорофор, добавление катионов или анионов не вызывает каких-либо существенных сдвигов максимума флуоресценции. В то же время добавление ионов к раствору соединения (13) приводит к гипсохромным (от 4 до 91 нм) сдвигам максимума флуоресценции, не оказывая значительного влияния на её интенсивность.
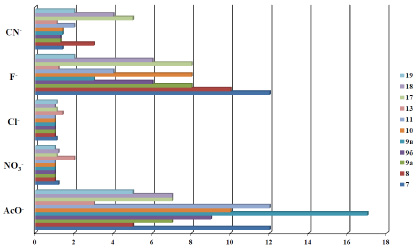
Относительное изменение интенсивности флуоресценции соединений (7–11, 13, 17–19) (с 5,0∙10–6 моль/л) в MeCN при добавлении солей NBu4+A– (с 2,5∙10–5 моль/л)
Заключение
Таким образом, исследование новых поли(1-винилимидазолиевых) материалов в качестве потенциальных хемосенсорных систем показало, что они являются эффективными реагентами для определения катионов Zn2+, Cd2+ и анионов AcO–. Установлено, что наиболее селективные и эффективные сенсоры на анионы могут быть получены при кватернизации всех пиридиновых атомов азота в поли(1-винилимидазольной) матрице.
Работа выполнена при финансовой поддержке Минобрнауки России в рамках ФЦП «Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2007–2013 годы» (проект № 14.A18.21.0803).
Рецензенты:
Межерицкий В.В., д.х.н., проф., зав отделом НИИ ФОХ ЮФУ, г. Ростов-на-Дону;
Стариков А.Г., д.х.н., в.н.с. НИИ ФОХ ЮФУ, г. Ростов-на-Дону.
Работа поступила в редакцию 30.10.2013.
Библиографическая ссылка
Толпыгин И.Е., Федянина А.Ю., Старикова А.А., Николаева О.Г., Левитина И.В., Плужникова С.Ю., Муханов Е.Л., Дубоносов А.Д., Брень В.А. СИНТЕЗ И ИССЛЕДОВАНИЕ НОВЫХ ПОЛИ(1-ВИНИЛИМИДАЗОЛЬНЫХ) ИОНОХРОМОВ // Фундаментальные исследования. 2013. № 10-10. С. 2207-2211;URL: https://fundamental-research.ru/en/article/view?id=32737 (дата обращения: 17.05.2026).



