Известно, что в развитии многих патохимических процессов определенную роль играют активные формы кислорода (АФК). Снижение активности естественной антиоксидантной системы организма связано со многими неблагоприятными факторами: это влияние ксенобиотиков, различные виды излучения, ухудшение экологической обстановки, широкое распространение социальных заболеваний, постоянные стрессы, потребление загрязненной пищи, неконтролируемый прием лекарственных препаратов. Понятно, что поиск новых источников антиоксидантов является актуальной задачей [8].
В 2004 году НИИ питания РАМН на основании изучения ежедневного рациона питания опубликовал рекомендуемые уровни потребления пищевых и биологически активных веществ [6]. В качестве одного из альтернативных источников полифенольных соединений, в том числе флаван-3-олы (катехин, эпикатехин, галлокатехин, эпигаллокатехин) или янтарной кислоты предложено использовать крыжовник отклоненный (Grossularia reclinata (L) Mill.) [7].
Обладая широким спектром фармакологической активности, флавоноиды применяются в медицине как желчегонные, гипоазотемические, гепатозащитные, противоязвенные, капилляроукрепляющие средства [9]. Широкий спектр действия флавоноидов объясняется их избирательностью по отношению к активным формам кислорода (АФК): при гиперпродукции АФК они проявляют антиоксидантные свойства, а при низком уровне генерации АФК – прооксидантные. Удачное сочетание низкой токсичности с высокой фармакологической активностью делает их чрезвычайно перспективными для профилактики и лечения многих заболеваний [8].
Целью настоящего исследования является изучение антиоксидантной активности крыжовника отклоненного.
Химический состав крыжовника отклоненного по сравнению с другими садовыми культурами зависит от сорта, возраста, почвенных и климатических условий, поэтому данные по химическому составу крыжовника в разных источниках отличаются между собой сильнее, чем по другим садовым культурам.
Следует также отметить, что из-за невысокого спроса этой ягоды со стороны большинства населения его полезные качества изучены слабее, чем у других ягод. Но даже то, что известно о крыжовнике, привлекает к себе внимание и дает основание считать его полезной и целебной ягодой [1, 4].
В народной медицине используются плоды, листья, цветки и семена всех видов рода Grossularia Mill. [1, 3].
Отвар из ягод крыжовника используется при лечении заболеваний желудочно-кишечного тракта, обладает болеутоляющим, слабительным и диуретическим действием [3]. Настой листьев рекомендуют при туберкулезе легких [1]. Спелые ягоды, благодаря наличию серотонина, обладают противоопухолевыми свойствами. Крыжовник способствует защите от рaдиaции, что обьясняют свойством пектина связывать и выводить из организма тяжелые металлы и радионуклиды. Сок крыжовникa используется для лeчeния лучeвых порaжeний, a сырой джeм – для профилaктики гипeртонии, склeрозa сосудов (зaкупорки сосудов тромбaми) и инфaрктов [3].
По данным литературы, химический состав различных надземных органов крыжовника отклоненного представлен флавоноидами, катехинами, фенолокислотами, кумаринами, антоцианами, которые являются основными природными антиоксидантами [3, 4].
Материал и методы исследования
Для исследования были выбраны три сорта наиболее распространённых на Северном Кавказе: «Московский красный», «Юбилейный ярко-жёлтый» и «Огни Краснодара без шипов». Сырьё собрано в период плодоношения в июле 2011 г.
Структурное многообразие фенольных антиоксидантов делает трудным их разделение на индивидуальные вещества и их количественное определение. Поэтому суммарное содержание антиоксидантов, присутствующих в образце, часто является более информативным параметром [8].
Определение общего содержания антиоксидантов в различных извлечениях из исследуемых видов сырья проводили на жидкостном хроматографе «Цвет Яуза-01-АА».
Массовую концентрацию антиоксидантов измеряют, используя градуировочный график зависимости выходного сигнала от концентрации кверцетина и/или галловой кислоты.
Сущность амперометрического метода измерения массовой концентрации антиоксидантов заключается в измерении силы электрического тока, возникающего при окислении молекул антиоксиданта на поверхности рабочего электрода при определенном потенциале, который после усиления преобразуется в цифровой сигнал. Величина возникающей при этом силы электрического тока будет зависеть как от природы и концентрации анализируемых веществ, так и от типа материала рабочего электрода и потенциала, приложенного к электроду [5].
Результаты исследования и их обсуждения
Спиртовые и водно-спиртовые извлечения антиоксидантов определяли исходя из площадей пиков дифференциальных кривых соответствующих экстрактов [2]. Площади пиков, а также концентрации антиоксидантов в пересчете на кверцетин и галловую кислоту представлены в табл. 1.
Исходя из экспериментальных данных, представленных в табл. 1, можно сделать вывод о том, что максимальное содержание антиоксидантов выявлено в экстракте из листьев крыжовника отклоненного сорт «Московский красный», полученном спиртом этиловым 40 %.
Методика выполнения измерений содержания антиоксидантов в напитках и пищевых продуктах, биологически активных добавках, экстрактах лекарственных растений амперометрическим методом, разработанная ОАО НПО «Химавтоматика», аттестована ФГУП «Всероссийский научно-исследовательский институт метрологической службы» в соответствии с ГОСТ Р 8.563-96, ГОСТ Р ИСО 5725-2002 (свидетельство об аттестации МВИ № 31-07).
При соблюдении всех регламентированных условий и проведении анализа в точном соответствии с данной методикой значение погрешности (и ее составляющих) результатов измерений не должны превышать значений, представленных в табл. 2.
Методика получения анализируемых извлечений: точную навеску измельченного сырья (около 1 г) помещали в колбу вместимостью 100 мл, добавляли примерно 30 мл спирта этилового соответствующей концентрации или воды и кипятили на водяной бане в течение 30 минут. Для приготовления экстрактов из ягод их предварительно измельчали и растирали в ступке. Содержимое колбы фильтровали через бумажный фильтр в мерную колбу вместимостью 100 мл. Извлечение вышеуказанным способом повторяли еще 2 раза, фильтр промывали экстрагентом и доводили объем фильтрата до метки. В случае необходимости пробу разбавляли [2].
Таблица 1
Содержание антиоксидантов (в пересчете на кверцетин и галловую кислоту), полученных из крыжовника отклоненного
|
Объект исследования крыжовник отклонённый |
Используемые экстрагенты |
Площадь пика (Sп нА/с) |
Содержание антиоксидантов (в пересчете на кверцетин, мг/г) |
Содержание антиоксидантов (в пересчете на галловую к-ту, мг/г) |
|
Сорт «Московский красный» |
||||
|
Листья |
спирт этиловый 96 % |
1228,02 |
0,482 ± 0,004 |
0,292 ± 0,011 |
|
спирт этиловый 70 % |
2667,73 |
1,134 ± 0,015 |
0,727 ± 0,016 |
|
|
спирт этиловый 40 % |
3965,20 |
1,715 ± 0,021 |
1,101 ± 0,023 |
|
|
вода |
2739,62 |
1,167 ± 0,018 |
0,746 ± 0,021 |
|
|
Ягоды |
спирт этиловый 96 % |
1068,17 |
0,413 ± 0,006 |
0,243 ± 0,009 |
|
спирт этиловый 70 % |
1285,99 |
0,515 ± 0,007 |
0,315 ± 0,013 |
|
|
спирт этиловый 40 % |
1818,41 |
0,754 ± 0,011 |
0,474 ± 0,007 |
|
|
вода |
1048,28 |
0,392 ± 0,003 |
0,256 ± 0,006 |
|
|
Стебли |
спирт этиловый 96 % |
1110,57 |
0,167 ± 0,002 |
0,132 ± 0,007 |
|
спирт этиловый 70 % |
1337,52 |
0,213 ± 0,003 |
0,161 ± 0,004 |
|
|
спирт этиловый 40 % |
1509,17 |
0,303 ± 0,004 |
0,193 ± 0,005 |
|
|
вода |
945,79 |
0,182 ± 0,005 |
0,106 ± 0,003 |
|
|
Сорт «Юбилейный ярко-жёлтый» |
||||
|
Листья |
спирт этиловый 96 % |
1101,81 |
0,433 ± 0,005 |
0,257 ± 0,011 |
|
спирт этиловый 70 % |
2601,74 |
1,102 ± 0,015 |
0,692 ± 0,016 |
|
|
спирт этиловый 40 % |
3062,42 |
1,305 ± 0,012 |
0,845 ± 0,023 |
|
|
вода |
2716,80 |
1,201 ± 0,013 |
0,747 ± 0,019 |
|
|
Ягоды |
спирт этиловый 96 % |
996,11 |
0,389 ± 0,005 |
0,222 ± 0,006 |
|
спирт этиловый 70 % |
1140,83 |
0,445 ± 0,007 |
0,273 ± 0,005 |
|
|
спирт этиловый 40 % |
1635,11 |
0,676 ± 0,009 |
0,412 ± 0,008 |
|
|
вода |
1390,75 |
0,567 ± 0,007 |
0,348 ± 0,011 |
|
|
Стебли |
спирт этиловый 96 % |
1300,96 |
1,032 ± 0,017 |
0,164 ± 0,007 |
|
спирт этиловый 70 % |
2117,16 |
1,763 ± 0,019 |
0,282 ± 0,012 |
|
|
спирт этиловый 40 % |
2345,46 |
1,978 ± 0,023 |
0,319 ± 0,013 |
|
|
вода |
1940,92 |
1,605 ± 0,020 |
0,255 ± 0,009 |
|
|
Сорт «Огни Краснодара без шипов» |
||||
|
Листья |
спирт этиловый 96 % |
1307,11 |
0,521 ± 0,009 |
0,313 ± 0,005 |
|
спирт этиловый 70 % |
2699,87 |
1,115 ± 0,018 |
0,732 ± 0,010 |
|
|
спирт этиловый 40 % |
3181,04 |
1,369 ± 0,026 |
0,878 ± 0,014 |
|
|
вода |
2939,59 |
1,255 ± 0,021 |
0,804 ± 0,011 |
|
|
Ягоды |
спирт этиловый 96 % |
1103,15 |
0,427 ± 0,016 |
0,256 ± 0,007 |
|
спирт этиловый 70 % |
1442,25 |
0,583 ± 0,011 |
0,351 ± 0,008 |
|
|
спирт этиловый 40 % |
1769,73 |
0,728 ± 0,013 |
0,452 ± 0,006 |
|
|
вода |
1022,15 |
0,392 ± 0,006 |
0,221 ± 0,007 |
|
|
Стебли |
спирт этиловый 96 % |
1005,36 |
0,199 ± 0,003 |
0,113 ± 0,002 |
|
спирт этиловый 70 % |
1125,78 |
0,224 ± 0,012 |
0,138 ± 0,003 |
|
|
спирт этиловый 40 % |
1432,58 |
0,292 ± 0,010 |
0,175 ± 0,005 |
|
|
вода |
861,02 |
0,167 ± 0,009 |
0,096 ± 0,004 |
|
Примечание. Извлечения, содержащие максимальное количество антиоксидантов выделены полужирным курсивом.
Перед выполнением каждого цикла анализируемых проб проводили контроль чистоты аналитической системы. Для этого после выхода прибора на рабочий режим в него в качестве пробы вводили элюент. Если дрейф фонового тока не превышает 5 %, система считается чистой. Для каждой из проб проводили по пять последовательных измерений выходного сигнала (площади пика) анализируемого антиоксиданта. Массовую концентрацию антиоксидантов исследуемого образца, эквивалентную кверцетину, определяли по градуировочному графику кверцетина. При расчете результата учитывали разбавление пробы.
Таблица 2
Метрологические характеристики, приведенные в аттестованной ФГУП ВНИИМС методике
|
Диапазон измерений массовой концентрации (массовой доли), мг/г (по кверцетину) |
Показатель точности (границы относительной погрешности) ± δ, %, при Р = 0,95 |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σr, % |
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости), σR, % |
Предел повторяемости, r, %, Р = 0,95, n = 2 |
|
От 0,2 до 4000 вкл. |
28 |
10 |
14 |
28 |
Массовую концентрацию Х, мг/г, определяли по формуле
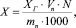
где Хг – массовая концентрация антиоксидантов, найденная по градуировочному графику, мг/л; Vn – объем раствора (экстракта) анализируемой пробы, мл; mn – навеска анализируемого вещества, г; N – кратность разбавления анализируемого образца.
Если выполняется условие приемлемости, за результат измерений принимют среднее арифметическое результатов двух параллельных определений:
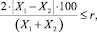
где X1, X2 – результаты параллельных определений массовой концентрации (массовой доли) антиоксидантов, (мг/г); r – значение предела повторяемости, в данном случае равное 10.
Если условие, представленное выше, не выполняется, то получают еще по два результата в полном соответствии с приведенной МВИ. Тогда за результат измерений принимают среднее арифметическое значение результатов четырех определений, если выполняется условие (8).
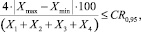
где Хmax, Хmin – максимальное и минимальное значения из полученных четырех результатов параллельных определений массовой концентрации (массовой доли) антиоксидантов, мг/г; CR0,95 – значение критического диапазона для уровня вероятности Р = 0,95 и n – результатов определений, равно:
СR0,95 = f(n)∙σr,
где f(n) – коэффициент критического диапазона, для n = 4 равен 3,6; σr – относительное среднеквадратическое отклонение повторяемости, равное в данном случае 10 % (табл. 2).
Таким образом, условие примет для данного метода следующий вид:
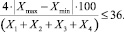
Если данное условие не выполняется, выясняют причины превышения критического диапазона, устраняют их и повторяют выполнение измерений в соответствии с требованиями МВИ.
Результаты анализа в документах, предусматривающих его использование, представляют в виде:
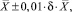 при P = 0,95,
при P = 0,95,
где X – среднее арифметическое значение результатов n определений, признанных приемлемыми по неравенствам (8) или (10); ±δ – границы относительной погрешности, %, (табл. 2).
Выводы
Установлено содержание антиоксидантов в спиртовых и водно-спиртовых, водных извлечениях надземной части. В извлечении из листьев крыжовника отклоненного сорт «Московский красный», полученного спиртом этиловым 40 %, содержание антиоксидантов оказалось максимальным и составляет в пересчете на кверцетин и на галловую кислоту. Эти данные явились обоснованием для выбора спирта этилового 40 % в качестве оптимального экстрагента при получении извлечения, содержащего максимальное количество антиоксидантов.
Рецензенты:
Кодониди И.П., д.фарм.н., доцент кафедры органической химии, Пятигорский медико-фармацевтический институт, филиал ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск;
Попова О.И., д.фарм.н., профессор кафедры фармакогнозии, Пятигорский медико-фармацевтический институт, филиал ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Работа поступила в редакцию 20.09.2013.
Библиографическая ссылка
Аджиахметова С.Л., Андреева О.А., Оганесян Э.Т. АНТИОКСИДАНТНАЯ АКТИВНОСТЬ ЭКСТРАКТОВ ИЗ ЛИСТЬЕВ, ПЛОДОВ И СТЕБЛЕЙ КРЫЖОВНИКА ОТКЛОНЕННОГО (GROSSULARIA RECLINATA (L) MILL.) // Фундаментальные исследования. 2013. № 10-6. С. 1297-1301;URL: https://fundamental-research.ru/en/article/view?id=32535 (дата обращения: 22.04.2026).



