Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
HISTOLOGICAL CHARACTERISTICS OF THE RAT ADRENAL GLAND AFTER SURGICAL LASER IMPACT AT MIDPOINT STAGE
Успехи лазерной хирургии обусловили широкое применение лазеров в современной клинической практике, что, однако, входит в противоречие с отставанием в области фундаментальных исследований реакции тканей и органов на лазерное повреждение, считающейся до сих пор недостаточно изученной [5]. Это особенно справедливо в отношении такого своеобразного, трудного для изучения и вместе с тем важного компонента эндокринной системы, как надпочечник, применение лазера для резекции которого [1, 6] осуществляется на фоне весьма далёкой от полноты картины его ответа на данный вид повреждения.
Для заполнения выявленного пробела мы поставили цель изучить гистологическую картину состояния надпочечника после воздействия хирургическим лазером. Ранее нами уже было представлено описание гистологической картины непосредственно после повреждения лазером этого органа и спустя сутки [2]. Настоящее исследование развивает затронутую тему и посвящено динамике последующих восстановительных процессов в надпочечнике в средние сроки – с конца первой до конца второй недели после лазерной деструкции.
Материал и методы исследования
Объектом исследования послужили 14 лабораторных белых крыс-самцов линии Wistar массой 348 ± 30 г., у которых с помощью аппарата «Лами» лучом диодного лазера со стандартными для эндокринных желёз параметрами: длина волны 1020 нм, мощность излучения 2,5 Вт, световод диаметром 400 мкм, продолжительность импульса 190 мс, интервал 10 мс, количество импульсов 150 (суммарная энергия воздействия 71,25 Дж), под эфирным наркозом осуществлялась деструкция части левого надпочечника. На 5 и 7 сутки передозировкой паров эфира производили забой крыс по 7 животных на срок.
Надпочечник обрабатывали по методу Honore [7], который позволяет дифференцировать в мозговом веществе надпочечника две основные субпопуляции хромаффиноцитов – эпинефроциты и норэпинефроциты. Согласно этому методу материал фиксировали в 5 % глутаровом альдегиде, заливали в парафин, а срезы окрашивали сочетанием бихромата калия и толуидинового синего. В результате норэпинефроциты окрашивались в зелёный, а эпинефроциты ‒ в серовато-фиолетовый цвет.
Результаты исследований и их обсуждение
5 сутки. Абляционная каверна, образовавшаяся на месте воздействия лазерного луча [2], заполнена экссудатом компонентами крови и зреющей грануляционной тканью, тесно связанной с капсулой, откуда активно мигрируют фибробласты и тучные клетки, прорастают кровеносные сосуды (рис. 1).
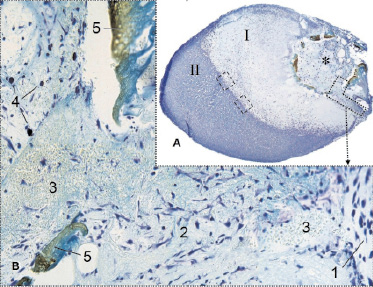
Рис. 1. Надпочечник крысы на 5 сутки после воздействия лазером. * – абляционная каверна: I – зона некроза; II – зона выживания; лазером: 1 – капсула; 2 – фибробласты; 3 – экссудат; 4 – тучные клетки; 5 – струп; ---- – область, представленная на Рис.2. Фикс. глут. альдегидом, окр. по Honore. A – Об. 4х, B – Об. 40х, фотонасадка 27х
Струп, покрывающий края каверны, представлен карамелизированной жёлто-коричневой массой, светлеющей до золотистой по мере удаления от края повреждения. Располагающаяся под струпом зона губчатого некроза изменила свой вид по сравнению с описанным ранее в первые сутки после лазерного воздействия [2]. Наружный и внутренний его слои уже не имеют четкой границы между собой, обе сильно деструктурированы – полностью утратили черты клеточного строения и слабо воспринимают красители. Зона компактного некроза слабо прокрашивается, имеет начальные признаки набухания и резко отграничивается от выжившей части органа. Очертания этой зоны лишь приблизительно повторяют очертания края каверны и её ширина, измеренная от края каверны до выжившей ткани, составляет 1–2 мм.
В толще некротизированной части органа разбросан разнородный некротический детрит, полиморфноядерные лейкоциты и фибробласты, присутствует экссудат компонентами крови. Наибольшая концентрация лейкоцитов и фибробластов обнаруживается в пограничной с зоной выживания области, здесь же наиболее выражено образование новых сосудов. В этой области изредка встречаются эндокриноциты, оказавшиеся изолированными от основной массы клеток своей популяции и имеющие ядра неправильной формы.
В выжившей части органа эндокриноциты и нейроны хорошо прокрашиваются и имеют нормальный вид. Эпинефроциты и норэпинефроциты мозгового вещества отчётливо дифференцируются (рис. 2). В толще выживших эндокриноцитов можно встретить клетки с пикнотизированными ядрами, но вне связи с границей повреждения.
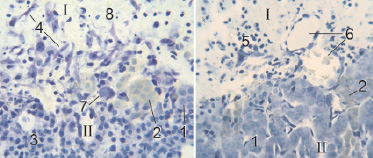
Рис. 2. Граница некроза и выживания в надпочечнике крысы на 5 сутки после воздействия лазером: I – зона некроза; II – зона выживания; 1 – эпинефроциты; 2 – норэпинефроциты; 3 – эндокриноциты сетчатой зоны коры; 4 – фибробласты; 5 – лейкоциты; 6 – новые сосуды; 7 – нейрон; 8 – экссудат. Фикс. глут. альдегидом, окр. по Honore. Об.4х., фотонасадка 27х
7 сутки. Струп, в котором сохранилась только светлоокрашенная часть, начал фрагментироваться. Поражённая часть резко отекает и увеличивается в размерах. Всю полость абляционной каверны заполняет грануляционная ткань (рис. 3). Активное формирование грануляционной ткани происходит в зоне некроза, где останки погибших клеток фактически распались, а на их месте разбросаны заполненные гранулами золотисто-жёлтого цвета фагоциты, фибробласты и лейкоциты. Более сосредоточенно эти клетки располагаются на границе зоны выживания, при этом фибробласты имеют вытянутую форму и ориентированы в основном вдоль неё. Выжившие эндокриноциты и нейроны имеют нормальный вид. Хромаффиноциты отчётливо дифференцируются (рис. 4). Как и на 5 сутки, в зоне выживания продолжают встречаться погибшие эндокриноциты с пикнотизированными ядрами, но вне связи с границей повреждения.
14 сутки. Отёчность и размеры поражённой части уменьшилась. На месте абляционной каверны располагаются распавшиеся на фрагменты струп и губчатая зона некроза, окруженные грануляционной тканью. Зона некроза густо оккупирована одноядерными макрофагами и в меньшей степени гигантскими многоядерными клетками, которые образуют мощный пласт в ее срединной части. Фагоциты заполнены гранулами, идентичными по окрашиванию и консистенции остаткам струпа или губчатых некротических масс. Выжившие эндокриноциты неотличимы от нормальных. Граница зоны выживания и некроза стала более контрастной, чем в первую неделю после воздействия: по одну сторону нет остатков погибших эндокриноцитов, по другую ‒ изолированных выживших (рис. 5).
Наблюдаемые в надпочечнике процессы в ответ на лазерное повреждение с конца первой до конца второй недели после воздействия в целом соответствуют схеме восстановления после аналогичного воздействия, описанного для других паренхиматозных органов, особенно для печени [3, 4, 8], за исключением ярко выраженной экссудации. Можно предположить, что причина такого отличия кроется в исключительно богатом кровоснабжении надпочечника, относительная величина кровотока в котором одна из самых высоких в организме и превосходит таковую в поджелудочной железе и печени в 2–2,5 раза [9, 10].
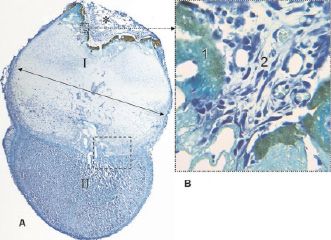
Рис. 3. Надпочечник крысы на 7 сутки после воздействия лазером. * – абляционная каверна: I – зона некроза; II – зона выживания; 1 – струп; 2 – зрелая грануляционная ткань; ↔ – отёк; --- – область, представленная на Рис.4. Фикс. глут. альдегидом., окр. по Honore. A – Об. 4х, B – Об. 40х, фотонасадка 27
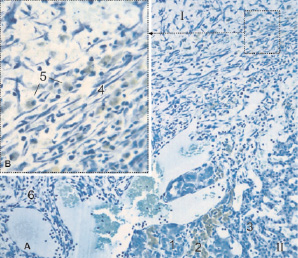
Рис. 4. Надпочечник крысы на 7 сутки после воздействия лазером: I – зона некроза; II – зона выживания; 1 – эпинефроциты; 2 – норэпинефроциты; 3 – эндокриноциты сетчатой зоны коры; 4 – фибробласты; 5 – фагоциты; 6 – полиморфноядерные лейкоциты. Фикс. глут. альдегидом, окр. по Honore. A – Об. 10х, B – Об. 40х, фотонасадка 27х
Следует также отметить тесную связь развивающейся грануляционной ткани с капсулой надпочечника как не только наиболее массивным, но и наименее пораженным соединительно тканным элементом органа.
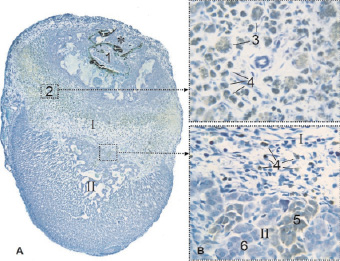
Рис. 5. Надпочечник крысы на 14 сутки после воздействия лазером. * – место воздействия: I – зона некроза; II – зона выживания; 1 – фрагменты струпа в зрелой грануляционной ткани; 2 – пласт фагоцитов; 3 – гигантские многоядерные клетки; 4 – одноядерные макрофаги; 5 – норэпинефроциты; 6 – эпинефроциты. Фикс. глут. альдегидом., окр. по Honore. A – Об. 4х, B – Об. 40х, фотонасадка 27х
Обнаружение на 7 сутки в струпе только светлоокрашенной внутренней части, очевидно, связано с тем, что более ломкая темноокрашенная обугленная поверхность струпа под действием разрастающейся грануляционной ткани крошится и отслаивается от более пластичной внутренней его части, прочно связанной с нижележащими слоями.
Несовпадение очертаний края каверны и зоны поражения, вероятно, объясняется асимметрией сосудистой сети надпочечника и его формой, так как распределение температуры в органе зависит не только от особенностей лазера (тип, мощность излучения, частота импульсов и др.) и природы облучаемых тканей (однородность, теплопроводность и т.п.), но и специфики перфузии в ней крови и кривизны поверхности, принимающей воздействие [3, 11].
Обращает на себя внимание, что в зоне выживания эндокриноциты интегрированные друг с другом как в интактном органе внешне нормальны и относительно стабильны весь период наблюдения. В то время как эндокриноциты, выжившие в пограничной зоне некроза и изолированные от своей популяции, многочисленные на 1 сутки [2] и изредка встречающиеся на 5 сутки, к 7 суткам исчезают. Можно предположить, что эти клетки ранее были смертельно повреждены и затем медленно угасли, и/или губительную роль для них сыграло лишение родного микроокружения, необходимого для нормального функционирования и жизнеспособности.
В половине случаев всех сроков некроз занимает весь объём органа кроме капсулы и узкой подкапсулярной зоны. В этих случаях наблюдается массивная инфильтрация лейкоцитами и последующее заполнение грануляционной тканью всего объёма органа. Данный вариант развития событий подтверждает справедливость утверждения, что применённое воздействие со стандартными для эндокринных желёз параметрами вследствие малых размеров надпочечника крысы приводят к избыточному перегреву и поражению у части органов всего их объёма, за исключением самой периферической области (капсулы) [2]. Орган после этого, очевидно, идёт по пути полной морфофункциональной дегенерации.
Выводы
1. При частичном поражении лазером паренхимы эндокриноциты, интегрированные в неповреждённой части, имеют нормальную морфологию и относительно стабильны весь период наблюдения.
2. Эндокриноциты, выжившие в пограничной области и оказавшиеся изолированными от клеток своей популяции, имеют аномальный вид и к 7 суткам исчезают.
3. В повреждённой части наблюдается формирование и созревание грануляционной ткани, выраженная экссудация компонентами крови и отёк (наибольший на 7 сутки), обильное заселение полиморфноядерными лейкоцитами и фагоцитами (в большей степени мононуклеарными макрофагами, в меньшей ‒ многоядерными гигантскими клетками), образующими к 14 суткам мощный пласт вдоль границы с зоной выживания. Абляционная каверна деформируется и зарастает грануляционной тканью, её краевая зона, образованная струпом и слоем губчатого некроза, распадается на фрагменты.
4. Лазерное поражение всей паренхимы надпочечника приводит к массивной инфильтрации лейкоцитами и заполнению грануляционной тканью всего объёма органа.
Рецензенты:
Гансбургский А.Н., д.м.н., профессор кафедры гистологии, цитологии и эмбриологии, ГБОУ ВПО «Ярославская государственная медицинская академия» Минздрава РФ, г. Ярославль;
Михайлов В.П., д.м.н., профессор, заведующий кафедрой патологической физиологии, ГБОУ ВПО «Ярославская государственная медицинская академия» Минздрава РФ, г. Ярославль.
Работа поступила в редакцию 16.09.2013.Библиографическая ссылка
Кемоклидзе К.Г., Тюмина Н.А. ГИСТОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА НАДПОЧЕЧНИКА КРЫСЫ ПОСЛЕ ВОЗДЕЙСТВИЯ ХИРУРГИЧЕСКИМ ЛАЗЕРОМ НА СРЕДНЕСРОЧНОМ ЭТАПЕ // Фундаментальные исследования. 2013. № 10-5. С. 1084-1089;URL: https://fundamental-research.ru/en/article/view?id=32457 (дата обращения: 02.06.2026).



