Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE MORPHOLOGICAL BASIS OF THE CAUSES OF RECURRENCE IN PATIENTS WITH POSTOPERATIVE VENTRAL HERNIAS
Послеоперационные вентральные грыжи любой локализации являются частым осложнением в абдоминальной хирургии. Частота их зависит от заживления послеоперационной раны и при первичном натяжении составляет 1 %, при вторичном достигает 11 %, а в РФ после ряда операций – 52 % [1].
Широкое внедрение синтетических имплантатов по свойствам, приближенным к требованиям идеального протезирующего материала, позволило произвести революцию в лечении данной патологии [2]. Так, за последние 5 лет в герниологической практике наметилась положительная тенденция снижения частоты послеоперационных осложнений и рецидивов, связанных с применением синтетических имплантатов благодаря практически повсеместному внедрению методов ненатяжной пластики грыжевых ворот. В сравнение с этим частота рецидивов при закрытии грыжевых ворот местными тканями по-прежнему достигает 50–100 %.
Активно продолжается обсуждение вопроса, что успех лечения больного с грыжей зависит от расположения синтетического эндопротеза относительно апоневрозов мышц живота. Так, при расположении имплантата в позициях in lay, on lay частота рецидивов может достигать 13 %. Позиция имплантата sub lay часто сопровождается развитием спаечного процесса [3]. При использовании комбинированных методов закрытия грыжевых ворот частота рецидивов составляет 0,5 %.
Если до 6 месяцев после пластики передней брюшной стенки способ операции, примененный синтетический эндопротез, общий статус больного играют первостепенное значение, то на поздних сроках, когда процесс интеграции эндопротеза должен быть уже завершен, остается неясным механизм рецидива грыжи.
Известно, что почти все искусственные материалы при имплантации in vivo в той или иной степени со временем разрушаются за счет факторов биодеградации [5, 6]. Число исследований, посвященных физическим, химическим и биологическим свойствам полипропиленовых имплантатов велико и носит противоречивый характер [4]. Отсутствие комплексной оценки делает затруднительным объяснение причин рецидивов у больных с послеоперационными вентральными грыжами.
Цель исследования – провести морфологический анализ причин рецидивов у больных, оперированных по поводу послеоперационных вентральных грыж на различных сроках.
Материал и методы исследования
После начала широкого использования протезирующей герниопластики на базе ММУ «Городская клиническая больница № 1 им. Н.И. Пирогова» у больных с первичными и рецидивными послеоперационными вентральными грыжами прошло 17 лет. Проведен морфологический анализ биопсийного интраоперационного материала, полученного от 32 больных, находившихся на лечении в условиях хирургических отделений ММУ Городская клиническая больница № 1 им. Н.И. Пирогова и Самарской областной клинической больницы им. М.И. Калинина за период с 2010 г. по июнь 2013 г. (исследование продолжается). Мужчин было – 9, женщин – 23. Средний возраст пациентов составил – 61 год.
У всех больных до развития рецидива предшествовала имплантация с применением как тяжелых, так и легких синтетических полипропиленовых эндопротезов.
Все рецидивы клинически были разделены по срокам на ранние (до 6 месяцев с момента последней операции) и поздние (6 месяцев и более).
Образцы тканей для гистологического исследования получали непосредственно из зоны рецидива грыжи (зона вновь сформированных грыжевых ворот) – 4 фрагмента 0,5×0,5 см.
Полученный материал фиксировали в 10 %-м растворе нейтрального формалина, обезвоживали, заливали в парафин. Срезы толщиной 5–6 мкм изготавливали на микротоме Sakura Accu-Cut SRM200 (Sakura, Finetek, Япония), окрашивали гематоксилином и эозином, пикрофуксином по Ван Гизон, крезил виолетом по стандартным методикам.
Просмотр и фотосъемку препаратов производили с помощью аппаратурного комплекса «Видеотест» с программным обеспечением «Морфология 5.2». (ООО «Видеотест», Санкт-Петербург, Россия).
Результаты исследования и их обсуждение
При микроскопической оценке фрагментов тканей больных с ранним рецидивом (19 пациентов) волокна синтетических полипропиленовых эндопротезов, при визуализации их при помощи светового микроскопа, не претерпевали каких-либо видимых изменений. Волокна оставались гладкими, при этом средний их диаметр, определенный на поперечных срезах, полностью соответствовал исходному, указанному фирмой-производителем (0,14, 0,15, 0,16).
Граница волокно – ткань была представлена скоплением макрофагов, гигантских клеток инородных тел с количеством ядер от 8–28, визуализируемых в одной плоскости гистологического среза (рис. 1, а). В этой зоне отсутствовали волокнистые структуры, за счет чего формировался люфт размером 78,8 ± 19,3 мкм. Несколько к периферии от волокон эндопротеза хорошо прослеживали муфты, представленные соединительной тканью, с циркулярно-ориентированными коллагеновыми волокнами с тенденцией к фиброзу и недостаточно выраженным сосудистым компонентом, где определяли нарушения гемодинамики преимущественно в виде сладжей и стазов. Прилегающая к волокнам грануляционная ткань, как правило, была с признаками воспаления от слабовыраженного до значительного за счет лимфоцитарной диффузной инфильтрации.
От циркулярных муфт к периферии регенерата гетерогенность грануляционной ткани сохранялась также за счет преобладания клеточного компонента, представленного активированными фибробластами на фоне признаков воспаления и нарушений гемодинамики – полнокровия венозных сосудов, в просвете которых присутствовали свертки крови. В некоторых полях зрения определяли периваскулярные кровоизлияния (рис. 1, б).
Периваскулярно были выявлены единичные дегранулированные тучные клетки (рис. 2).
Морфологическая картина у больных с поздними рецидивами послеоперационных вентральных грыж (13 пациентов) показала отсутствие признаков завершения регенераторных процессов в зоне имплантации синтетического эндопротеза и признаки патологической перестройки имеющегося регенерата при сохранении хронического асептического воспаления в нем.
Грануляционная ткань, расположенная вокруг волокон, сохраняла гетерогенность, но с превалированием фиброзного компонента, макрофагальный инфильтрат был выражен в меньшей степени. Зона первого контакта волокно-ткань была по-прежнему представлена гигантскими клетками инородных тел с количеством ядер до 50 в одной плоскости гистологического среза. Размер сформированного люфта волокно-ткань увеличивался до 425 ± 20,1. Каждое волокно эндопротеза окружала фиброзная циркулярно-ориентированная муфта, за которой следовали продольно ориентированные так же фиброзно-измененные волокна соединительной ткани.
а 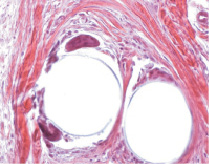 б
б 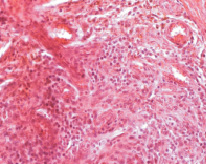
Рис. 1. Фрагменты грануляционной ткани у больного с ранним рецидивом послеоперационной вентральной грыжи: а – гетерогенная полнокровная грануляционная ткань, прилегающая к волокну полипропиленового эндопротеза в виде муфты. Гигантские клетки инородных тел (стрелки). Окраска гематоксилин-эозин. х260; б – гетерогенная полнокровная грануляционная ткань отдаленной зоны. Окраска гематоксилин-эозин. х260
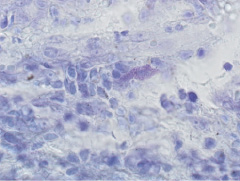
Рис. 2. Дегранулированная тучная клетка на периферии соединительно-тканной муфты (стрелка). Окраска крезил виолет. х400
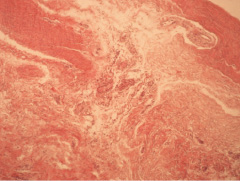
Рис. 3. Состояние зоны непосредственного рецидива. Окраска гематоксилин-эозин. Ув. 100
Характерной особенностью стали зоны непосредственного рецидива, в которых визуализировали пучки коллагеновых волокон с нарушенной целостностью, заполненные рыхлой неоформленной соединительной тканью (рис. 3).
Таким образом, при развитии раннего и позднего рецидива ведущую роль приобретают тканевые реакции, развивающиеся на границе волокно-эндопротез. Ключевое значение приобретает макрофагальная реакция, поддерживающая хроническое асептическое воспаление и «ложно-персистирующие механизмы биодеградации», которые направлены как на сам материал, так и на окружающую соединительную ткань. Все это приводит к образованию люфта, формирует локусы разрывов фиброзно-измененной соединительной ткани, которые в совокупности с действием производящих факторов и особенностями расположения эндопротеза (in lay, on lay) способствуют развитию рецидива.
Рецензенты:
Федорина Т.А., д.м.н., профессор, заведующая кафедрой общей и клинической патологии: патологической анатомии и патологической физиологии ГБОУ ВПО СамГМУ Минздрава России, г. Самара;
Колсанов А.В., д.м.н., профессор, заведующий кафедрой оперативной хирургии и клинической анатомии с курсом инновационных технологий ГБОУ ВПО СамГМУ Минздрава России, г. Самара.
Работа поступила в редакцию 14.08.2013.


Библиографическая ссылка
Пономарева Ю.В., Белоконев В.И., Волова Л.Т., Гуляев М.Г. МОРФОЛОГИЧЕСКИЕ ОСНОВЫ ПРИЧИН РЕЦИДИВОВ У БОЛЬНЫХ С ПОСЛЕОПЕРАЦИОННОЙ ВЕНТРАЛЬНОЙ ГРЫЖЕЙ // Фундаментальные исследования. 2013. № 9-2. С. 263-266;URL: https://fundamental-research.ru/en/article/view?id=32257 (дата обращения: 27.05.2026).



