Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
STUDY OF GENES DNA-REPAIRED MECHANISMS IN CANCER CELLS WITH NORMAL AND MUTANT GENE TP53
Последствиями влияния радиационного воздействия на живые клетки являются различные типы повреждений ДНК: образование перекрестных связей в белках ДНК, перекрестных связей между цепями ДНК, оксидация и разрушение оснований, разрушение углеводно-фосфатных цепей, разрыв одной и двух цепей ДНК. В выживших клетках могут наблюдаться отсроченные эффекты ионизирующего излучения: мутации, хромосомные абберации, генетическая нестабильность. Эти генетически поврежденные клетки могут стать основой возникновения злокачественных опухолей. Похожие изменения ещё в большей степени могут наблюдаться в раковых клетках, в частности, после радиационного воздействия в процессе лучевой терапии. Ген ТР53 и кодируемый им белок р53 вовлечен в регуляцию клеточного ответа на стрессорные воздействия путем остановки клеточного цикла в контрольных точках для осуществления репарации ДНК либо индукции апоптоза в случае невозможности устранения ее повреждений [2, 4, 7]. Утрата функции гена р53 наблюдается практически в каждом случае злокачественных заболеваний, а его недостаточность приводит к развитию опухолей [1].
Белок р53 обладает исключительно коротким временем жизни, что достигается за счет регулируемого активного убиквитин-зависимого и убиквитин-независимого разрушения [3, 5]. Инициаторами разрушения р53 служат несколько убиквитиновых лигаз типа Е3 [1]. Наиболее изученной среди них является убиквитиновая лигаза Mdm2, которая сама является продуктом гена, активируемого р53 [8, 13, 14]. Процесс взаимодействия р53 с белком Mdm2 тонко регулируется за счет множества механизмов [9]. Одни механизмы направлены на регуляцию активности Mdm2, в то время как другие нацелены на модификации его мишени – самого белка р53 [12]. Через белки р53 и Mdm2 многоклеточный организм может элиминировать мутантные клетки. Комплекс р53:Mdm2 является одним из ключевых механизмов регуляции репарации ДНК. Клетки содержат ряд различных сигнальных путей и эффекторов, которые опосредуют репарацию различных типов повреждений ДНК. Эти пути включают эксцизионную репарацию оснований (BER), репарацию двунитевых разрывов ДНК, зависимую от гомологической рекомбинации (HRR), негомологичное соединение концов (NHEJ), эксцизионную репарацию нуклеотидов (NER) и репарацию неправильно спаренных оснований (MMR) [6]. Нарушение эффективной репарации в раковых клетках способствует возникновению химио- и радиорезистентных раковых опухолей и метастазированию здоровых органов и тканей. Исследование особенностей функционирования ДНК-репарирующих механизмах в различных типах раковых опухолей, в частности, в ТР53-мутантых опухолях поможет выяснить причины радио- и химиорезистентности.
Целью настоящей работы явилось изучение особенностей экспрессии генов ДНК-репарирующих механизмов в раковых клетках с нормальным и мутантным геном ТР53.
Материал и методы исследования
Использовали клеточную линию рака прямой кишки человека HCT-116 с нормальным геном ТР53 – НСТ116 р53 +/+ и изогенную клеточную линию HCТ-116 с мутантным геном ТР53 – НСТ116 р53 –/–. Клетки облучали рентгеновским излучением, генерируемым терапевтическим акселератором Cliniac 600 при комнатной температуре в дозах 4 Грэй одноразово. Клетки облучались в 24-луночных планшетах (объём лунки 2,5 мл.). Профили экспрессии генов в клетках НСТ116 р53 +/+ и НСТ116 р53–/– облученных в дозе 4 Гр изучали через 1, 12 и 24 часа после облучения с использованием микроматрицы Affymetrix серии HGU133А.
РНК выделяли из 3∙106 клеток с использованием набора для выделения РНК в соответствии с инструкцией производителя. Целостность выделенной РНК проверяли с использованием биоанализатора Agilent 2100 по целостности 18S и 28S рибосомальной РНК с помощью электрофореза в 1 % агарозном геле. Библиотеку клонированных ДНК готовили с использованием набора GeneChipExpression 3’-Amplification One-CyclecDNASynthesisKit. Мечение биотином анти-смысловых библиотек клонированных РНК и очистка были проведены с использованием набора GeneChipExpression 3’-Amplification Reagentsfor IVT Labeling в соответствии с протоколом производителя. Количество полученной РНК и ДНК оценивалось спектрофотометрически с использованием спектрофотометра NanoDrop. Фрагментацию кРНК проводили при 94 °C в термоциклере в течение 35 минут. Синтезированные биотинилированные кРНК вначале гибридизировали с контрольной матрицей «Test-3» с целью оценки качества полученных кРНК. Если качество биотинилированных кРНК соответствовало расчётному, то тогда проводили гибридизацию с матрицей HGU133А. Матрицу окрашивали стрептовидин-фикоэритрином. Окрашенную матрицу отмывали от несвязавшегося белка и сканировали на сканере GeneArray G2500A.
Для обработки материала использовали программы GeneCards и GeneAnnot. Для построения дендрограмм использовали программы Cluster 3.0 и TreeView. Принадлежность генов к тому или иному механизму репарации ДНК определяли по базе данных KEGG.
Для сравнения экспрессии генов ДНК-репарирующих механизмов между клеточными линиями с нормальным и мутантным геном ТР53 использовали балльную шкалу. Динамика экспрессии гена в двух клеточных линиях на протяжении 1, 12 и 24 часов оценивалась в 3 балла, если она была идентична на протяжении всего эксперимента; в 2 балла – если динамика экспрессии совпадала по двум временным точкам; в 1 балл – при совпадении по 1 временной точке и в 0 баллов, если она полностью различалась в двух клеточных линиях. Сумму баллов делили на общее число генов одного из ДНК-репарирующих механизмов и получали среднее значение, по которому производили сравнение сходства экспрессии генов в двух клеточных линиях между основными путями репарации ДНК.
Результаты исследования и их обсуждение
На рис. 1, а показан путь эксцизионной репарации оснований BER, который устраняет однонитевые разрывы ДНК и участки отсутствия нескольких оснований, а также удаляет специфические поврежденные основания [11].
Такие компоненты пути эксцизионной репарации оснований, как OGG1 (8-оксогуанидин ДНК гликозилаза), TDG (тимин–ДНК гликозилаза) и UNG (урацил–ДНК гликозилаза) демонстрируют одинаковую экспрессию в течение всего эксперимента в двух клеточных линиях. Гены NEIL3 (эндонуклеазы NEIL VIII–3), MBD4 (домен 4 метил-CpG-связывающего белка), NEIL1 (эндонуклеазы NEIL VIII–1), MPG (N-метилпурин-ДНК гликозилаза) и NTHL1 (nth эндонуклеазы III–1) имеют схожую динамику экспрессии на 1 и 24 часах, а ген MYH 1 (гомолог MutY) на 1 и 12 часах после облучения. Схожая активность экспрессии гена SMUG1 (однонитевая селективная монофункциональная урацил-ДНК-гликозилаза 1) фиксируется только на 12 часе эксперимента в клеточных линиях с нормальным и мутантным геном ТР53. Все гены после 24 часов с момента воздействия на них рентгеновского излучения одинаково экспрессируются в двух клеточных линиях.
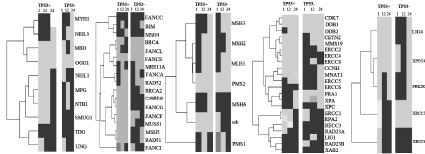
а б в г д
Рис. 1. Экспрессия генов основных путей репарации ДНК в клеточных линиях рака прямой кишки человека HCT-116 с нормальным геном ТР53 – НСТ116 р53 +/+ и изогенная клеточная линия HCТ-116 с мутантным геном ТР53 – НСТ116 р53:а – механизм эксцизионной репарации оснований BER; б – механизм репарации двунитевых разрывов ДНК, зависимый от гомологической рекомбинации HRR; в – механизм эксцизионной репарации неправильно спаренных оснований MMR; г – механизм эксцизионной репарации нуклеотидов NER; д –механизм репарации двунитевых разрывов ДНК, негомологичное соединение концов NHEJ. Черным цветом обозначены гены, экспрессия которых возрастает по отношению к контрольной группе. Серым цветом обозначены гены, экспрессия которых снижается по отношению к контрольной группе. ТР53 (+) – раковая клеточная линия НСТ116 с нормальным геном TP53. ТР53 (–) – раковая клеточная линия НСТ116 с мутантным геном TP53
На рис. 1, б показан путь репарации двунитевых разрывов ДНК, зависимой от HRR, устраняет двунитевые разрывы в ДНК посредством гомологичного механизма восстановления непрерывной спирали ДНК [11].
Компоненты пути HRR – FANCC (белок, ассоциирующийся с анемией Фанкони, комплементарная группа C), FANCE (белок, ассоциирующийся с анемией Фанкони, комплементарная группа E) и RAD52 (гомолог белка RAD52) после 1, 12 и 24 часов имеют одинаковую динамику экспрессии в двух клеточных линиях. Аналогичный результат у генов MSH4 (гомолог белка MUTS), BRCA1 (белок ассоциирующийся с раком молочной железы 1), FANCA (белок, ассоциирующийся с анемией Фанкони, комплементарная группа А) и FANCF (белок, ассоциирующийся с анемией Фанкони, комплементарная группа F), экспрессия которых различна лишь после 24 часов с момента воздействия на них рентгеновского облучения. Гены BIM (белок BCL2), FANCL (белок, ассоциирующийся с анемией Фанкони, комплементарная группа L) и MUS81 (гомолог эндонуклеазы MUS81) одинаково экспрессируются только после 1 часа, а BRCA2 (белок, ассоциирующийся с раком молочной железы 2), MSH5 (небелковое кодирование), RAD51 (гомолог белка RAD51) и FANCI (белок, ассоциирующийся с анемией Фанкони, комплементарная группа I) после 24 часов. Активность экспрессии гена C190RF40 и FANCG (белок, ассоциирующийся с анемией Фанкони, комплементарная группа G) в двух клеточных линиях на протяжении всего эксперимента не имеет сходства.
На рис. 1, в показан путь репарации неправильно спаренных оснований ДНК (MMR).У генов MLH1 (белок, ассоциирующий сраком толстой кишки, неполипозныйтип 2), PMS2 (белок пост-мейотической сегрегации 2) и PMS1(белок пост-мейотической сегрегации) прослеживается схожая динамика экспрессии в двух клеточных линиях в течение всего эксперимента. Такие компоненты репарационного пути, как MSH3 (гомолог 3 белка MUTS), MSH2 (гомолог 2 белка MUTS) экспрессируются одинаково после 1 и 24 часов, а MSH6 (гомолог 6 белка MUTS) после 1 и 12 часов. Активность экспрессии гена ssb (белок, ассоциирующий с синдромом Шегрена антиген B) в двух клеточных линиях имеет сходство лишь спустя 1 час.
На рис. 1, г показан путь эксцизионной репарации нуклеотидов (NER). В двух клеточных линиях с нормальным и мутантным геном ТР53 на протяжении всего эксперимента наблюдается одинаковая активность экспрессии у генов CDK7 (циклин-зависимая киназа 7), DDB1 (белок, связывающийся со специфическими повреждениями ДНК, тип 1), XPC (белок, ассоциированный с пигментной ксенодермой тип C) и XAB2 (белок, связывающий XAB, тип 2). Одинаковая динамика экспрессии прослеживается у генов DDB2 (белок, связывающийся со специфическими повреждениями ДНК, тип 2), CETN2 (центрин), MMS19 (нуклеотидный гомолог репарации MMS19), RAD23A (гомолог А белка Rad23) и RAD23B (гомолог B белка Rad23), но лишь в точках 12 и 24 часов, а у генов ERCC5 (белок ERCC5), ERCC6 (белок ERCC6), ERCC1 (белок ERCC1), RPA2 (РНК полимераза Iполипептидов B) и LIG1 (АТФ-зависимая ДНК лигаза I) через 1 и 12 часов после облучения. Такие компоненты пути NER, как ERCC8 (белок ERCC8) и XPA (белок, ассоциированный с пигментной ксеродермой, комплиментарная группа A) имеют схожую экспрессию после 12 часов, а ERCC2 (белок ERCC2), CCNH (циклин H), MNAT1 (menage a troishomolog 1, cyclin H assembly factor (Xenopuslaevis), RPA1 (репликация белка A1) и ERCC3 (белок ERCC3) после 24 часов. Активность экспрессии гена ERCC4 (белок ERCC4) в двух клеточных линиях на протяжении всего эксперимента не имеет сходства.
В пути NHEJ (рис. 1, д) нет генов, которые показывали бы схожую динамику экспрессии в двух клеточных линиях на протяжении всего эксперимента. Ген XRCC4 (X-ray repair complementing defective repairin Chinese hamster cells 4) имеют схожую активность экспрессии в клеточных линиях в точке 1 и 12 час, а PRKDC (протеинкиназы, ДНК-активация, каталитических полипептидов) и XRCC6 на 12 и 24 часах. Одинаково экспрессируется ген XRCC5 в точке 1 час, а LIG4 (лигаза IV, ДНК, АТФ-зависимых) в точке 24 часа в клеточных линиях после воздействия на них рентгеновского облучения.
Путь MMR (рис. 2) в двух клеточных линиях имеет наибольшее сходство динамики экспрессии генов, которая равна 2,28 баллам. Похожие результаты показывает путь BER, который на 0,08 баллов уступает MMR. Средние результаты у пути NER ‒ 1,81 баллов. В путях NHEJ и HRR экспрессия генов является наиболее разобщенной и сходство экспрессии генов в двух клеточных линиях составило лишь 1,6 и 1,47 баллов.
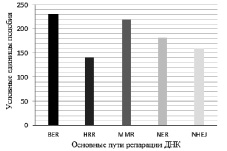
Рис. 2. Сравнение соответствия экспрессии генов ДНК-репарирующих механизмов между клеточными линиями с нормальным и мутантным геном ТР53. BER – механизм эксцизионной репарации оснований; HRR – механизм репарации двунитевых разрывов ДНК, зависимый от гомологической рекомбинации; MMR – механизм эксцизионной репарации неправильно спаренных оснований; NER – механизм эксцизионной репарации нуклеотидов; NHEJ –механизм репарации двунитевых разрывов ДНК, негомологичное соединение концов
В норме двунитевые разрывы ДНК возникают с невысокой частотой в период репликации генома, но их число увеличивается при воздействии внеклеточных агентов. В качестве такого агента может выступать ионизирующее излучение, которое способствует большому количеству двунитевых разрывов в ДНК клетки. За восстановление двунитевых разрывов отвечают два механизма репарации ДНК – HRR и NHEJ. HRR воссоединяет концы ДНК без потери информации с помощью матрицы сестринской хроматиды [10]. В противоположность этому при NHEJ концы ДНК часто укорачиваются, и этот вариант является потенциально мутагенным [15].
В эксперименте установлено, что под воздействием ионизирующего излучения экспрессия генов клеточной линии с мутантным геном ТР53 существенно отличается от клеточной линии с геном дикого типа. Изменение экспрессии генов механизма репарации NHEJ в клеточной линии с мутантным геном ТР53 оказывает влияние на эффективность репарации двунитевых разрывов ДНК. Неисправность этих механизмов может привести к аберрациям хромосом и возникновению генетической нестабильности, что в итоге можно связать с высокой радиорезистентностью ТР53-мутантных опухолей.
Заключение
Таким образом, сравнительный анализ динамики экспрессии генов, продукты которых являются участниками ДНК-репарирующих механизмов в клетках линий HCT-116 p53 –/– и HCT-116 p53 +/+ через 1,12 и 24 часа после радиационного воздействия в дозе 4 Гр позволил сделать следующие выводы:
1. Радиационная индуцированная динамика экспрессии генов механизмов репарации гомологичных рекомбинаций и репарации соединений негомологичных концов отличаются в клеточных линиях с нормальным и мутантным геном ТР53.
2. Мутация гена ТР53 не оказывает влияние на радиационно-индуцированную динамику экспрессии генов механизмов репарации ошибочно спаренных нуклеотидов и эксцизионной репарации удалений поврежденных оснований.
Работа выполнена при поддержке федеральной целевой программы «Научные и научно-педагогические кадры инновационной России» грант № 14.B37.21.0558.
Рецензенты:
Балыкин М.В., д.б.н., профессор, заведующий кафедрой адаптивной физической культуры Института медицины, экологии и физической культуры, ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск;
Слесарев С.М., д.б.н., доцент, заведующий кафедрой биологии и биоэкологии Института медицины, экологии и физической культуры, ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск.
Работа поступила в редакцию 11.07.2013.
Библиографическая ссылка
Глущенко Е.С., Белогубов П.В., Антонова А.В., Семенова М.А., Живодерников И.В., Свеколкин В.П., Викторов Д.А., Мастиленко А.В., Иванская Н.Н., Столбовская О.В., Шутов А.М., Макеева Е.Р., Остаточников В.А., Напалкова С.М., Саенко Ю.В. ИЗУЧЕНИЕ ОСОБЕННОСТЕЙ ЭКСПРЕСИИ ГЕНОВ ДНК-РЕПАРИРУЮЩИХ МЕХАНИЗМОВ В РАКОВЫХ КЛЕТКАХ С НОРМАЛЬНЫМ И МУТАНТНЫМ ГЕНОМ ТР53 // Фундаментальные исследования. 2013. № 8-4. С. 867-871;URL: https://fundamental-research.ru/en/article/view?id=32012 (дата обращения: 14.05.2026).



