Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
MICROSTRUCTURE OF MATERIAL FORMED BY NON–EQUILIBRIUM ELECTROCHEMICAL OXIDATION OF COPPER AND ALUMINIUM
В настоящее время получению оксидов металлов и оксидных систем уделяется большое внимание. При этом текстура материала, оказывающая влияние на его характеристики, во многом определяется составом материала, а для материалов одного состава зависит от способа получения [5].
Среди разнообразных способов синтеза оксидов металлов следует выделить электролиз в неравновесных условиях [2]. Возможность варьирования состава системы в широких пределах, минимальное содержание примесей, повышенный запас внутренней энергии, простота аппаратурного оформления процесса синтеза позволяют рассматривать неравновесный электролиз как перспективный способ получения наноразмерных оксидов металлов и оксидных систем.
С помощью неравновесного электрохимического окисления металлов под действием переменного тока промышленной частоты был осуществлен синтез медь-алюминиевой оксидной системы. Вследствие повышенной реакционной способности, обусловленной развитой поверхностью, дефектной структурой, продукт неравновесного электрохимического окисления меди и алюминия является неустойчивым и интенсивно взаимодействует с контактирующими средами. Это проявляется при выделении продукта из раствора электролита с помощью декантации и заключается в образовании основных карбонатов за счет растворенного диоксида углерода воздуха [3]. Термообработка продукта приводит к разложению карбонатов с образованием оксидов меди и алюминия. Способ получения медь-алюминиевой оксидной системы через стадию образования карбонатов назван карбонатным.
Во избежание изменения фазового состава продукт электролиза подвергался экспресс-отмывке от ионов электролита в течение суток и сушке при остаточном давлении 3–5 кПа. Данный способ получения медь-алюминиевой оксидной системы назван оксидным.
Цель данной работы состояла в исследовании состава и микроструктуры продуктов неравновесного электрохимического окисления меди и алюминия, полученных карбонатным и оксидным способами.
Материалы и методы исследования
Электрохимический синтез медь-алюминиевой оксидной системы под действием переменного тока промышленной частоты проводился в соответствии с методикой, приведенной ранее при описании кинетических закономерностей неравновесного электрохимического окисления меди и алюминия [4].
Фазовый состав продуктов определялся рентгенофазовым анализом (РФА), проводимым с помощью дифрактометра ДРОН 3М, в следующих условиях: CuКα-излучение, I = 25 мкА, U = 35 кВ, скорость съемки 4 q/мин, область сканирования углов (2θ) 10–70°. Рентгенографический анализ фазового состава, размеров областей когерентного рассеяния (ОКР) проводился с использованием базы данных PCPDFWIN, а также программы полнопрофильного анализа «Powder Cell 2.4».
Микрофотографии образцов, высушенных при минимальном остаточном давлении и пониженном содержании оксида углерода в воздухе, получены с помощью растрового электронного микроскопа JEOL JSM-7500FA, а образца, сушка которого проводилась на воздухе, – с помощью сканирующего электронного микроскопа S–3400N.
Результаты исследования и их обсуждение
Неравновесное электрохимическое окисление меди и алюминия проводилось в растворе хлорида натрия с концентрацией 3 % мас. при температуре 90 °С и плотности тока 1,0 А/см2.
Фазовый состав продукта, полученного оксидным способом, и размер кристаллитов (ОКР) рассчитывались по рентгенограмме исходного образца (рис. 1, I), структура которого иллюстрируется микрофотографиями (рис. 1, II–IV).
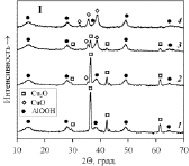



Рис. 1. Рентгенограммы оксидного продукта электрохимического окисления меди и алюминия, хранившегося на воздухе в течение 0 (1), 30 (2), 60 (3), 90 (4) суток, и микрофотографии при увеличении 5 000 (II), 25 000 (III), 100 000 (IV)
Продукт неравновесного электрохимического окисления меди и алюминия, высушенный при остаточном давлении 3–5 кПа, состоит из оксида меди (I) и оксигидроксида алюминия – бемита. Несмотря на то, что содержание оксида меди (I) в образце существенно меньше, чем содержание бемита, интенсивность его рефлексов значительно больше. Различия в интенсивностях рефлексов обусловлены разной степенью окристаллизованности фаз. На рентгенограмме не прописываются рефлексы хлорида натрия (электролит).
Нечеткие рефлексы бемита, простирающиеся на несколько удвоенных углов отражения (2θ), свидетельствуют о том, что бемит является слабоокристаллизованным. Это также подтверждается результатами расчета размера частиц бемита, согласно которым область когерентного рассеяния бемита составляет 3–4 нм. Для первичных частиц оксида меди (I) по результатам расчета характерны несколько большие размеры (15–20 нм).
Микрофотографии, приведенные на рис. 1, II–IV, свидетельствуют о том, что продукт неравновесного электрохимического окисления меди и алюминия образован не отдельными частицами с размерами, указанными выше, а представляет собой агломераты. Известно, что агломерация частиц происходит вследствие стремления минимизировать поверхностную энергию, обусловленную большой поверхностью раздела, наличием неравновесных фаз и повышенным содержанием дефектов кристаллической структуры.
В зависимости от условий старения для бемита характерно образование игольчатых, пластинчатых или ажурных частиц [1]. Для первичных частиц оксида меди (I) характерны несколько большие размеры и также агломерация при старении с образованием частиц различной формы. Несмотря на то, что для оксида меди (I) более типично образование частиц кубической формы, в настоящее время разработаны способы его получения в виде сфер, полых сфер, трубок, нанопроволок, а также агломератов пластинчатых частиц [7, 9, 10].
Сопоставление микрофотографий с изображениями распределения элементов (медь, алюминий, кислород, хлор, натрий) по поверхности позволило определить преимущественный фазовый состав каждого элемента структуры. Микронные агломераты бемита состоят из значительно более мелких частиц, имеющих пластинчатую форму. Оксид меди (I) равномерно распределен по поверхности бемита в виде округлых агломератов с размерами до 500 нм.
Содержание ионов электролита (хлора и натрия), равномерно распределенных по поверхности, более 1 % мас. Это говорит о том, что ионы электролита не полностью отделены от продукта, полученного оксидным способом.
По карбонатному способу (рис. 2, 1) продукт состоит из гидрата двойного карбоната меди-алюминия Cu2,5Al2C1,7O8,9·5,2H2O и основного карбоната меди – малахита Cu2(OH)2CO3, а также бемита, для которого не характерно образование карбонатов на воздухе. Гидрат двойного карбоната меди-алюминия может быть отнесен к классу слоистых двойных гидроксидов (layered double hydroxides – LDH) [6]. На этом основании данное соединение обозначено как Cu–Al/LDH.
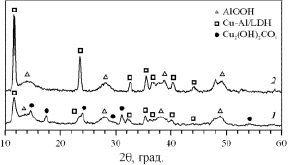
Рис. 2. Рентгенограммы карбонатного продукта электрохимического окисления меди и алюминия
Карбонатный способ также не позволяет получать индивидуальные частицы. Для образца, в состав которого входят обе углеродсодержащие фазы, агломерация и агрегация частиц обусловливают существование трех структурных форм (рис. 3): агрегаты пластинок в форме цветков с размерами 4–5 мкм; сростки иголок длиной 5–6 мкм; крупные бесформенные агломераты более мелких частиц, их основная масса имеет размеры 5–10 мкм, присутствует также небольшое количество более крупных агрегатов с размерами 20–25 мкм.
Элементный анализ, проведенный посредством рентгеновской энерго-дисперсионной спектроскопии, позволил идентифицировать описанные элементы структуры (таблица).
Известно [8], что для обладающего слоистой структурой Cu-Al/LDH характерна неупорядоченная агрегация пластин. Элементный анализ позволил подтвердить, что агрегированные пластинки (1) являются однофазными, их состав соответствует соединению, обозначенному, как Cu-Al/LDH. Поскольку игольчатая структура характерна для основного карбоната меди, проводился пересчет элементного состава иголок на данную фазу. Иголки (2) состоят из основного карбоната меди и бемита с мольным соотношением 1,4:1. Бесформенные агломераты (3) представляют собой бемит с небольшим количеством соединений меди. Независимо от того, какое из соединений меди образует данные агломераты, последние характеризуются избыточным содержанием кислорода. Полагаем, что источником избыточного кислорода являются гидроксильные группы или молекулы воды слабоокристаллизованного бемита. В отличие от агломератов (3) высокая сходимость результатов МРА и нашего расчета для иголок (2) может быть обусловлена тем, что в их состав входит более окристаллизованный бемит, формула которого близка к AlOOH.

Рис. 3. Микрофотографии карбонатного продукта электрохимического окисления меди и алюминия при увеличении 1 000 (I), 3 000 (II)
Фазовый состав элементов структуры продукта неравновесного электрохимического окисления меди и алюминия
|
Номер на рис. 2 |
Способ определения содержания элементов |
Содержание элемента, % ат. |
||
|
O |
Al |
Cu |
||
|
1 |
МРА* |
76,68 |
10,42 |
12,90 |
|
Расчет** для фазы Cu2,5Al2C1,7O8,9·5,2H2O |
75,81 |
10,75 |
13,44 |
|
|
2 |
МРА* |
69,58 |
8,16 |
22,26 |
|
Расчет для 1,4 Cu2(OH)2CO3+AlOOH |
70,29 |
7,97 |
21,74 |
|
|
3 |
МРА* |
82,93 |
14,28 |
2,79 |
|
Расчет для 10,2 AlOOH+Cu2(OH)2CO3 |
67,55 |
27,15 |
5,30 |
|
|
Расчет** для 10,8 AlOOH+Cu2,5Al2C1,7O8,9·5,2H2O |
70,00 |
25,10 |
4,90 |
|
Примечания: * МРА – микрорентгеноспектральный анализ;
** Расчет без учета углерода и водорода.
В базе данных PCPDFWIN, необходимой для анализа размеров областей когерентного рассеяния (ОКР) с помощью программы полнопрофильного анализа «Powder Cell 2.4», отсутствует информация о фазе Cu–Al/LDH. Это не позволило установить размер кристаллитов продукта, полученного карбонатным способом. Тем не менее явно выраженная поликристалличность всех элементов структуры и высокое значение удельной поверхности, составляющее 226,8 м2/г, позволяет говорить о том, что размеры структурных элементов, из которых состоят агломераты, располагаются в нанодиапазоне.
При условиях, когда содержание оксида углерода в среде невелико (рис, 2, 2), образование основного карбоната меди не происходит. Согласно результатам рентгенофазового анализа, в составе образца содержится оксид меди (II). Наложение рефлексов бемита, Cu-Al/LDH и оксида меди (II) не позволяет достоверно идентифицировать фазу оксида меди (II). Однако дополнение фазового состава результатами визуального наблюдения за процессом старения осадка позволяет утверждать о наличии оксида меди (II) в составе продукта. Длительное хранение оксида меди (I) в растворе приводит к тому, что часть оксида меди (I), расположенная внизу слоя осадка, следовательно, менее доступная для образования карбонатов, окисляется до оксида меди (II). Наглядным доказательством данного процесса являлось появление характерной черной окраски оксида меди (II) на фоне желтого оксида меди (I).
Структура продукта, в состав которого не входит основный карбонат меди, неоднородна (рис. 4).

Рис. 4. Микрофотографии карбонатного продукта электрохимического окисления меди и алюминия при увеличении 2 000 (I), 5 000 (II)
Состав каждого элемента структуры определялся из сопоставления микрофотографий с изображениями распределения элементов (медь, алюминий, кислород, хлор, натрий) по поверхности. Агрегированные пластинки, диаметр которых составляет 2–3 мкм, представляют собой Cu–Al/LDH. Иголки и плоские ограненные пластинки толщиной ~ 350 нм соответствуют оксиду меди (II). Бесформенные агломераты бемита имеют размеры 3–8 мкм, присутствует также небольшое количество более крупных агрегатов с размерами 30–50 мкм.
Выводы
1. Продукты неравновесного электрохимического окисления меди и алюминия как высушенный при остаточном давлении 3–5 кПа, так и после самопроизвольной карбонизации на воздухе состоят не из индивидуальных частиц, а представляют собой агломераты различной геометрии.
2. Система оксид меди (I) – бемит представляет собой агломераты частиц бемита, имеющих пластинчатую форму, на поверхности которых равномерно распределены более мелкие агломераты оксида меди (I).
3. Структура продукта карбонизации, содержащего двойной слоистый гидроксид, основной карбонат меди и бемит, представлена агрегатами пластинок, сростками иголок, крупными бесформенными агломератами более мелких частиц.
4. Продукт, состоящий из двойного слоистого гидроксида и бемита, образован агрегированными пластинками и иголками различной геометрии.
Результаты исследования микроструктуры образцов получены на оборудовании Нано-Центра ТПУ (растровый электронный микроскоп JEOL JSM-7500FA).
Работа выполнена в рамках государственного задания «Наука» по теме 3.2702.2011.
Рецензенты:
Козик В.В., д.т.н., профессор, заведующий кафедрой неорганической химии Национального исследовательского Томского государственного университета, г. Томск;
Буйновский А.С., д.т.н., профессор Северского технологического института, филиала ФГАОУ ВПО «Национальный исследовательский ядерный университет «МИФИ», г. Северск.
Работа поступила в редакцию 01.07.2013.Библиографическая ссылка
Усольцева Н.В., Коробочкин В.В., Балмашнов М.А. МИКРОСТРУКТУРА ПРОДУКТОВ НЕРАВНОВЕСНОГО ЭЛЕКТРОХИМИЧЕСКОГО ОКИСЛЕНИЯ МЕДИ И АЛЮМИНИЯ // Фундаментальные исследования. 2013. № 8-3. С. 750-755;URL: https://fundamental-research.ru/en/article/view?id=31995 (дата обращения: 16.05.2026).



