Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
CARDIOELECTRIC FIELD OF THE RAT DURING POSTISHEMIC REPERFUSION OF THE LEFT CORONARY ARTERY
Восстановление кровотока в ишемизированном участке миокарда (реперфузия) является наиболее эффективной стратегией для уменьшения размера инфаркта миокарда [3]. Несмотря на положительные эффекты, реперфузия может вызывать патологическое «реперфузионное повреждение». Изменения в энергетическом обеспечении кардиомиоцитов, нарушения внутриклеточного ионного гомеостаза и генерация активных форм кислорода являются основными факторами повреждения миокарда на стадии ранней реперфузии [14]. Нарушение метаболизма в поврежденных кардиомиоцитах сопровождается изменениями электрических процессов [16].
Кардиоэлектрическое поле (КЭП) формируется совокупностью потенциалов кардиомиоцитов и отображается на поверхность тела животных и человека [1]. На основе изменений пространственных и временных параметров КЭП можно судить о функциональном состоянии миокарда [6, 15]. Изучение формирования КЭП на экспериментальных моделях, на животных позволит подойти к пониманию механизмов восстановления возбудимости миокарда при морфо-функциональных изменениях, происходящих в сердце в результате кратковременной ишемии и последующей реперфузии.
Целью работы явилось исследование структурных и функциональных изменений миокарда и их отображение на кардиоэлектрическое поле в период реполяризации желудочков сердца в условиях ишемии и последующей реперфузии.
Материалы и методы исследования
Эксперименты проведены на самцах крыс линии Вистар (n = 12) возрастом 4–5 месяцев. Крыс наркотизировали уретаном (1,2 г/кг, в/м), переводили на искусственное дыхание. Грудную клетку вскрывали парастернально слева, проводили 10-минутную окклюзию левой передней нисходящей коронарной артерии при помощи окклюдера, позволяющего затем неинвазивно возобновлять кровоток в сосуде. Грудную клетку послойно зашивали. После 10-минутной окклюзии проводили 60-минутную неинвазивную реперфузию.
Кардиоэлектрические потенциалы регистрировали методом синхронной многоканальной электрокардиотопографии от 64 подкожных электродов, распределённых равномерно по поверхности грудной клетки животных. Униполярные кардиоэлектрические потенциалы на поверхности тела и биполярные ЭКГ в отведениях от конечностей регистрировали до, на фоне окклюзии и последующей реперфузии коронарной артерии.
По эквипотенциальным моментным картам в период конечной желудочковой активности оценивали пространственную и временную динамику электрического поля сердца на поверхности тела крыс.
Для анализа кардиоэлектрического поля (КЭП) в период реполяризации желудочков нами было выделено три временных характеристики:
1. TbBSPM – начало формирования КЭП.
2. TpeakBSPM – достижение положительным экстремумом своего максимального значения в период реполяризации желудочков, максимальная электрическая активность.
3. TendBSPM – окончания реполяризации желудочков.
Отсчет времени (в мс) производили относительно RII пика на ЭКГ во II отведении от конечностей.
Для оценки постишемического реперфузионного повреждения миокарда проводили гистологические исследования левого желудочка сердца крыс. Были изготовлены поперечные гистологические срезы толщиной 7 мкм в апикобазальном направлении (Криостат Leica СМ 1510S, Германия), окрашенные гематоксилин-эозином. Оценивали каждый 10-й срез. Гистологические срезы фотографировали с помощью камеры-окуляра DCM 500 (Бельгия) и программы для визуализации Scope Photo.
Статистика. Данные представлены в виде среднего арифметического ± стандартное отклонение. Достоверными принимали значения с критерием Вилкоксона для двух зависимых выборок(р < 0,05).
Результаты исследования и их обсуждение
Пространственные характеристики кардиоэлектрического поля
Кардиоэлектрическое поле, характерное для периода реполяризации желудочков (до, на фоне окклюзии и на фоне реперфузии), формируется на поверхности тела крыс в период восходящей части ТII-волны (TbBSPM). В начальную фазу реполяризации желудочков сердца зона электропозитивности на КЭП располагается до окклюзии каудально, электронегативности – краниально (рис. 1, а), на фоне окклюзии положительная зона расположена каудально на леволатеральной части вентральной поверхности грудной клетки, отрицательная – на дорсальной (рис. 1, б). На фоне реперфузии левой коронарной артерии зона электропозитивности располагается каудально, электронегативности – краниально на поверхности грудной клетки (рис. 1, в).
В период максимальной электрической активности, соответствующей вершине ТII-волны, при достижении положительным экстремумом своего максимального значения в период реполяризации желудочков (TpeakBSPM) и в период окончания реполяризации желудочков (TendBSPM) на нисходящей части ТII-волны, зона положительных потенциалов на КЭП на поверхности тела до окклюзии расположена каудально, электронегативности – краниально. Ишемия и постишемическая реперфузия приводят к изменению взаимного расположения зон кардиопотенциалов на КЭП на поверхности грудной клетки только на начальном этапе реполяризации желудочков сердца.
Временные характеристики кардиоэлектрического поля
Время начала формирования КЭП, характерного для реполяризации желудочков сердца (TbBSPM), достоверно не изменялось при окклюзии и реперфузии коронарной артерии относительно исходного состояния. На фоне окклюзии изменений времени TendBSPM выявлено не было, при реперфузии показано достоверное увеличение времени TendBSPM по сравнению с исходным состоянием. Достоверно увеличивается длительность начального периода реполяризации желудочков ТbBSPM-ТpeakBSPM. На фоне окклюзии изменений длительности периода ТbBSPM-ТendBSPM выявлено не было, показано достоверное увеличение длительности этого периода на фоне реперфузии (таблица).
Морфологическое исследование миокарда
Гистологическое исследование стенок левого желудочка сердца крыс после постишемической 60-минутной реперфузии коронарной артерии выявило реперфузионное повреждение миокарда. Были выявлены морфологические изменения миокарда: участки контрактур кардиомиоцитов и волнообразная деформация волокон, мелкоочаговая лейкоцитарная инфильтрация стромы только на передней стенке левого желудочка (рис. 2).
Для анализа патоморфологических изменений в разных слоях миокарда после кратковременной ишемии и последующей реперфузии нами были условно выделены зоны: выше места перевязки коронарной артерии; травмы; пограничная; ишемии-реперфузии; ниже зоны ишемии-реперфузии (рис. 3).
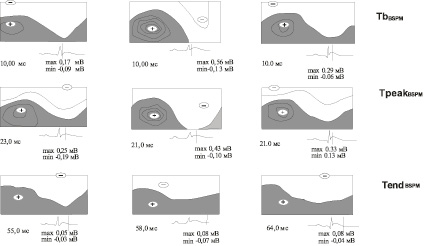
а б в
Рис. 1. Эквипотенциальные моментные карты на поверхности тела крыс линии Вистар в исходном состоянии, на фоне 10 минутной окклюзии и на фоне 60-минутной реперфузии коронарной артерии в период реполяризации желудочков (крыса № 43).Примечание. Закрашена область положительных кардиоэлектрических потенциалов, не закрашена отрицательных. Под каждой картой приведена ЭКГII с отметкой времени и указаны амплитуды наибольших положительных (max) и отрицательных (min) кардиопотенциалов в соответствующий момент времени. Знаками «+» и «–» обозначено местоположение максимального отрицательного и положительного кардиопотенциалов. Левая половина каждой карты соответствует вентральной стороне тела, правая ‒ дорсальной:а – исходное состояние; б – на фоне окклюзии; в – на фоне реперфузии
Временные параметры электрического поля сердца на поверхности тела крыс до, на фоне окклюзии и при реперфузии коронарной артерии (в мс)
|
Параметры |
До окклюзии |
На фоне окклюзии |
На фоне реперфузии |
|
TbBSPM |
9,9 ± 2,0 |
8,3 ± 1,8 |
9,9 ± 2,2 |
|
ТpeakBSPM |
21,1 ± 3,6 |
24,0 ± 6,8 |
26,8 ± 5,8 |
|
ТendBSPM |
65,7 ± 6,4 |
70,4 ± 11,9 |
77,5 ± 11,3* |
|
ТbBSPM-ТendBSPM |
55,5 ± 6,6 |
62,0 ± 11,6 |
68,6 ± 8,8* |
|
ТbBSPM-ТpeakBSPM |
11,1 ± 2,7 |
17,0 ± 5,2 |
17,9 ± 5,7* |
|
ТpeakBSPM-ТendBSPM |
44,4 ± 5,5 |
46,3 ± 10,5 |
50,6 ± 12,1 |
Примечание: * – значения достоверно отличаются относительно исходного состояния (р < 0,05).
В зоне травмы (1000 мкм) нами были обнаружены контрактуры кардиомиоцитов у 89 % крыс, волнообразная деформация волокон у 56 %, мелкоочаговая лейкоцитарная инфильтрация стромы у 44 %. Контрактуры у 88 % крыс встречаются на границе субэпикарда с интрамуральным слоем.
Волнообразная деформация выявлена в интрамуральном слое на границе с эпикардом у 40 % и на границе с эндокардом у 60 % крыс. У 44 % крыс очаги лейкоцитарной инфильтрации обнаружены на субэндокарде в основании передней папиллярной мышцы.
В пограничной зоне (200–300 мкм от зоны травмы) были выявлены участки контрактур кардиомиоцитов у 89 %, лейкоцитарная инфильтрация и волнообразная деформация стромы выявлены у 22 % крыс. Лейкоцитарная инфильтрация обнаружена на субэндокарде в основании передней папиллярной мышцы. Волнообразная деформация волокон выявлена у всех животных в интрамуральном слое.
В зоне ишемии-реперфузии (750–900 мкм от зоны травмы) наблюдали сходные изменения с пограничной зоной.
В зоне выше перевязки (500 мкм от зоны травмы) и в зоне ниже ишемии-реперфузии патологических изменений миокарда выявлено не было.
Появление волнообразной деформации волокон в зоне травмы, вероятно, было вызвано механическим повреждением миокарда. Появление лейкоцитарной инфильтрации стромы наблюдается только в зоне травмы на субэндокарде.
а  б
б
в 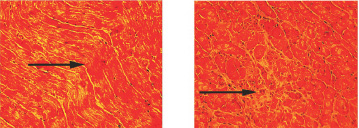 г
г
Рис. 2. Морфологические изменения миокарда на передней стенке левого желудочка крыс линии Вистар в условиях постишемической реперфузии левой нисходящей коронарной артерии:а – кардиомиоциты крысы в исходном состояние (субэпикардиальная зона; ув. 375);б – контрактура кардиомиоцитов крысы (указано стрелкой; ув.600); в – волнообразная деформация кардиомиоцитов (указано стрелкой; ув. 375); г – лейкоцитарнаяинфильтрация стромы (указано стрелкой; ув. 375)
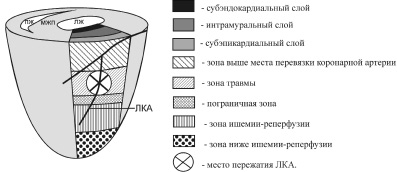
Рис. 3. Схема расположения зон патоморфологических измененийв миокарде крыс при постишемической реперфузии:ЛЖ – левый желудочек; ПЖ – правый желудочек; МЖП – межжелудочковая перегородка; ЛКА – левая коронарная артерия
Контрактуры кардиомиоцитов, которые наблюдаются в зоне травмы, в пограничной зоне и в зоне ишемии-реперфузии, являются результатом постреперфузионного повреждения миокарда левого желудочка крыс.
Развитие ишемического повреждения миокарда зависит от своевременного восстановления коронарного кровотока в пораженном сосуде [3]. Недостаток кислорода при ишемии миокарда приводит к нарушению энергетического обеспечения кардиомиоцитов. Восстановленный кровоток при реперфузии, снижая клеточную гибель в зоне ишемии, одновременно запускает процессы, оказывающие повреждающий эффект на миокард, главным образом окислительный стресс и воспаление [17]. Нарушение транспорта и метаболизма кальция – избыточное поступление ионов кальция (Са2+) из экстрацеллюлярного пространства внутрь кардиомиоцитов [14] может приводить к контрактурам. Пусковыми факторами развития стойкого патологического сокращения миофибрилл – контрактурных повреждений кардиомиоцитов и волнообразной деформации волокон являются нарушение клеточного гомеостаза и накопление ионов кальция в саркоплазме [4].
Нами обнаружена лейкоцитарная инфильтрация стромы миокарда в субэндокарде передней стенки левого желудочка. Реперфузия вызывает накопление нейтрофилов в поврежденной ишемией ткани, являясь индикатором воспаления [17].
Электрическое поле сердца на поверхности тела грызунов в период реполяризации желудочков сердца ранее было показано [5; 13]. В период реполяризации желудочков сердца на КЭП поверхности тела крыс зона положительных потенциалов расположена каудально, отрицательных – краниально [13]. При окклюзии левой коронарной артерии, которая обеспечивает кровоснабжение передней и латеральной стенки левого желудочка, у крыс зона электропозитивности смещается к леволатеральной части вентральной поверхности грудной клетки, отрицательная – на дорсальную [2]. У собак при окклюзии левой нисходящей коронарной артерии зона положительных кардиопотенциалов в период реполяризации желудочков расположена на вентральной стороне грудной клетки, при окклюзии левой огибающей коронарной артерии – на леволатеральной стороне грудной клетки [10]. У человека при переднем инфаркте миокарда, вызванном окклюзией левой нисходящей коронарной артерии, область положительных потенциалов однотипно располагается на вентральной поверхности грудной клетки [9]. Таким образом, у теплокровных животных и человека при окклюзии расположение области положительных кардиопотенциалов на вентральной поверхности туловища связано с расположением зоны пережатия коронарной артерии в период реполяризации желудочков сердца.
Нами показано, что у крыс на фоне 60-минутной постишемической реперфузии происходит восстановление взаимного расположения областей кардиопотенциалов до исходного состояния. У пациентов с окклюзией левой коронарной артерии после проведения трансмуральной баллонной ангиопластики происходит восстановление расположения зон кардиопотенциалов, близкое к здоровому [6].
На фоне постишемической реперфузии происходит удлинение фазы восстановления возбудимости миокарда (ТbBSPM-ТendBSPM). В период острой ишемии метаболические изменения в кардиомиоцитах приводят к изменению функции ионных каналов, электрическому ремоделированию, отвечающему за нарушение проведения и рефрактерности, увеличению электрической гетерогенности миокарда, удлинению QT интервала на ЭКГ [7; 12]. Проведено исследование по оценке динамики длительности QT у пациентов после тромболизиса в зависимости от эффективности реперфузии. У пациентов с успешным тромболизисом длительность QT значимо снижалась, а при сохраняющемся тромбозе – увеличивалась [10]. Другие авторы сообщают, что удлинение QT зачастую сопровождает спонтанную реперфузию [8].
Таким образом, острая окклюзия коронарной артерии у крыс приводит к изменению взаимного расположения зон кардиопотенциалов: положительная зона расположена каудально на леволатеральной части вентральной поверхности грудной клетки, отрицательная – на дорсальной. Постишемическая реперфузия миокарда на кардиоэлектрическом поле на поверхности тела экспериментальных животных приводит к восстановлению взаимного пространственного расположения зон кардиопотенциалов к исходному; к значимому изменению относительно исходного состояния, длительности реполяризации желудочков сердца за счет начального периода. После ишемии и реперфузии у крыс были выявлены морфологические изменения миокарда: участки контрактур кардиомиоцитов и волнообразная деформация волокон, мелкоочаговая лейкоцитарная инфильтрация стромы на передней стенке левого желудочка.
Исследования выполнены при поддержке гранта РФФИ № 12-04-01814, научного проекта для молодых ученых и аспирантов УрО РАН № 13-4-НП-442.
Рецензенты:
Рощевский М.П., д.б.н., профессор, академик РАН, главный научный сотрудник, ФГБУН «Коми научный центр Уральского отделения Российской академии наук», лаборатория сравнительной кардиологии, г. Сыктывкар;
Бочаров М.И., д.б.н., профессор, заведующий кафедрой физиологии и спортивной медицины факультета гуманитарного образования, ФГБОУ ВПО «Ухтинский государственный университет», г. Ухта.
Работа поступила в редакцию 07.06.2013.
Библиографическая ссылка
Мазур М.В., Суслонова О.В., Рощевская И.М. КАРДИОЭЛЕКТРИЧЕСКОЕ ПОЛЕ КРЫС ПРИ ПОСТИШЕМИЧЕСКОЙ РЕПЕРФУЗИИ ЛЕВОЙ КОРОНАРНОЙ АРТЕРИИ // Фундаментальные исследования. 2013. № 8-1. С. 98-103;URL: https://fundamental-research.ru/en/article/view?id=31879 (дата обращения: 07.05.2026).



