Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE EFFECT OF NEOADJUVANT CHEMOTHERAPY ON AUTOLOGOUS BLOOD ON THE ANTIOXIDANT SYSTEM IN THE TUMOR TISSUEAND THE TUMOR-SURROUNDING TISSUE IN THE PATIENTS WITH SOFT TISSUE SARCOMA
Саркомы мягких тканей (СМТ) относятся к наиболее агрессивным опухолям человека и характеризуются склонностью к рецидивированию, раннему метастазированию и, как следствие, низкими показателями выживаемости больных. И после комплексного лечения с проведением пред- и послеоперационной химиотерапии частота возникновения рецидивов и метастазов СМТ остается весьма высокой [10, 15], что объясняет актуальность поиска новых методов лечения.
Одним из проявлений опухолевого процесса является системное неспецифическое нарушение метаболических процессов в организме, например, активация свободнорадикального окисления; при этом не меньшее значение имеют локальные метаболические изменения в тканях. Поскольку известно участие активных форм кислорода (АФК) в регуляции клеточной пролиферации, инвазии и метастазирования опухолей [2, 4, 13], изучение окислительного гомеостаза, в частности, его антиоксидантного звена, в опухоли и немалигнизированных тканях, взаимодействующих с неоплазмой, является важным как для понимания условий развития и прогрессирования СМТ, так и для выяснения механизмов, опосредующих эффекты лечения.
Материалы и методы исследования
Были обследованы 30 пациентов с первично резектабельными (T2a-bN0M0) верифицированными злокачественными опухолями. Больные были разделены на две группы. Пациентам контрольной группы проводили оперативное лечение с последующей химиолучевой терапией. В основную группу вошли больные СМТ, которым была проведена неоадьювантная комбинированная аутобиохимиотерапия (НАБХТ) с последующим оперативным вмешательством и химиолучевой терапией. Методика аутобиохимиотерапии состояла в следующем: в два стерильных флакона, содержащих по 50 мл аутоплазмы, добавляли циклофосфан (600 мг/м2) и метотрексат (40 мг/м2), к форменным элементам крови (около 100 мл) добавляли доксорубицин (40 мг/м2). Полученные смеси инкубировали при 37 °C в течение 30 минут. Доксорубицин с форменными элементами вводили в локтевую вену, а смеси цитостатиков на аутоплазме вводили шприцем из нескольких точек в мягкую ткань перифокальной зоны в проекции опухоли. Химиотерапию проводили в первый и седьмой день, через 14 дней производили удаление опухоли и последующее химиолучевое лечение.
Материалом для исследования служили образцы ткани опухоли и ее перифокальной зоны, полученные во время операции. В качестве интактного контроля были взяты образцы условно здоровой ткани (без гистологических изменений), удаленные по линии резекции. Для оценки состояния ферментативного звена антиоксидантной системы определяли активность супероксиддисмутазы (СОД), каталазы и глутатионпероксидазы (ГПО) общепринятыми спектрофотометрическими методами. Об интенсивности перекисного окисления липидов (ПОЛ) судили по накоплению молекулярного продукта – малонового диальдегида (МДА) [1]. Перечисленные показатели определяли в 10 % гомогенатах тканей (0,04 М Tris-HCl буфер, рН 7,4), полученные результаты представляли в пересчете на мг белка. При статистической обработке полученных данных использовали параметрический t-критерий Стьюдента и непараметрический U-критерий Манна–Уитни.
Результаты исследования и их обсуждение
При сравнительном изучении ферментативного звена антиоксидантной защиты в тканях, полученных от больных контрольной группы, было выявлено снижение активности каталазы в образцах неоплазмы и её перифокальной зоны в среднем на 40,0 % по сравнению с неизмененной тканью (таблица). Одновременно в опухоли была обнаружена активация ГПО, более чем в 2,4 раза по сравнению с показателями в прилегающих зонах. Коэффициент, характеризующий сопряженную работу каталазы и ГПО, в опухоли имел наименьшее значение за счет сдвига системы в сторону усиления активности ГПО.
Достоверных различий активности СОД в образцах изучаемых зон выявлено не было. Исследования содержания продуктов ПОЛ в зоне неоплазии выявило тенденцию к снижению концентрации МДА как по сравнению с неизмененной тканью (на 34,0 %), так и тканью перифокальной зоны (на 22,0 %).
Проведение НАБХТ больным СМТ привело к изменению активности СОД и каталазы почти во всех сравниваемых зонах (таблица). Так, в опухоли было выявлено увеличение активности СОД в 2,5 раза по сравнению с интактным участком и на 82,0 % по сравнению с перифокальной зоной. По отношению к значениям в контрольной группе активность СОД увеличивалась на 80,0 %. В перифокальной зоне наблюдалась тенденция к росту активности СОД и значительное усиление активности каталазы на – 79,0 % по сравнению с интактной зоной, в которой активность фермента снижалась на 42,0 % по сравнению с образцами ткани аналогичной зоны в контроле. Показатели активности ГПО в опухоли и интактной ткани статистически не отличались от значений в контрольной группе. Снижение активности каталазы в интактной зоне привело к достоверному снижению коэффициента каталаза/ГПО почти в два раза по отношению к значению в контроле. В ткани перифокальной зоны происходили значимые изменения в работе ГПО: в изученных образцах активность фермента оставалась ниже значений в опухоли, но при этом оказалась на 42,7 % выше показателей в интактной ткани и на 54,5 % выше значений в контрольной группе. Благодаря сонаправленному повышению активности перекись-удаляющих ферментов в перифокальной зоне коэффициент отношения каталаза/ГПО не изменялся. В большинстве изученных образцов интактной и опухолевой ткани наблюдалось уменьшение накопления продукта липопероксидации: в интактной ткани концентрация МДА снижалась почти вдвое, а в опухоли на 30,6 % по сравнению с образцами соответствующих зон в контроле. Однако как и в контрольной группе, содержание МДА в ткани неоплазмы оставалось наименьшим. В перифокальной зоне наблюдалась тенденция к снижению уровня МДА.
Активность антиоксидантых ферментов и содержание МДА в образцах опухоли СМТ и ткани прилегающих зон
|
Группы |
СОД, у.е./мг белка |
Каталаза, мкМоль/мг белка |
ГПО, МЕ/мг белка |
Коэффициент, Кат/ГПО |
МДА, нМоль/мг белка |
|
|
Контрольная группа |
Интактная ткань n = 16 |
1,053 ± 0,165 |
9,040 ± 1,460 |
270,90 ± 34,60 |
31,78 ± 4,02 |
72,20 ± 9,40 |
|
Опухолевая ткань n = 16 |
1,128 ± 0,163 р > 0,1 |
5,350 ± 0,580 р < 0,01 |
663,80 ± 67,55 р < 0,001 |
8,26 ± 0,65 р < 0,001 |
47,73 ± 7,04 0,1 > р > 0,05 |
|
|
Ткань перифокальной зоны n = 16 |
1,000 ± 0,124 р > 0,1 р1 > 0,1 |
5,551 ± 0,438 р < 0,05 р1 > 0,1 |
268,18 ± 35,82 р > 0,1 р1 < 0,001 |
22,78 ± 1,72 р < 0,05 р1 < 0,001 |
68,4 ± 6,00 р > 0,1 0,1 > р1 > 0,05 |
|
|
Опытная группа (НАБХТ) |
Интактная ткань n = 14 |
0,829 ± 0,101 рк > 0,1 |
5,288 ± 0,677 рк < 0,05 |
290,50 ± 49,7 рк > 0,1 |
18,32 ± 3,32 рк < 0,01 |
42,20 ± 3,30 рк < 0,05 |
|
Опухолевая ткань n = 14 |
2,143 ± 0,350 р < 0,05 р к < 0,05 |
5,074 ± 0,688 р > 0,1 рк > 0,1 |
568,88 ± 36,00 р < 0,001 рк > 0,1 |
9,28 ± 2,35 р < 0,01 рк > 0,1 |
33,12 ± 1,96 р < 0,05 рк < 0,05 |
|
|
Ткань перифокальной зоны n = 14 |
1,175 ± 0,140 0,1 > р > 0,05 р 1 < 0,05 рк > 0,1 |
9,512 ± 1,438 р < 0,05 р1 < 0,05 рк < 0,05 |
414,40 ± 36,54 р < 0,05 р1 < 0,01 рк < 0,01 |
22,2 ± 5,25 р > 0,1 р1 < 0,01 рк > 0,1 |
50,90 ± 3,90 р > 0,1 р1 < 0,05 0,1 > рк > 0,05 |
|
Примечания: р – достоверно по отношению к интактной ткани; р1 – достоверно по отношению к ткани опухоли; рк – достоверно по отношению к идентичной зоне в контрольной группе.
Полученные данные свидетельствуют о том, что в образцах опухоли больных СМТ ведущим ферментом разложения пероксида водорода (Н2О2) является ГПО, в отличие от неизмененной ткани, где доминирует каталазный путь расщепления перекиси, что согласуется с результатами работ других авторов [7, 11]. Такое соотношение активности ферментов, удаляющих пероксиды, с невысокой активностью СОД, вероятно, обеспечивает, с одной стороны, эффективное удаление цитотоксических продуктов липоперекисидации, с другой – поддерживает определенную пропорцию между различными АФК, участвуя тем самым в регуляции пролиферативной активности опухолевых клеток [2, 3, 12].
Проведение НАБХТ не изменило соотношения в системе каталаза – ГПО, однако привело к активации СОД в образцах неоплазмы. Поскольку СОД является индуцибельным субстратом ферментом [3, 8], повышение её активности, полагаем, отражает усиление продукции супероксид аниона (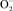 ) в опухолевых клетках в результате развития окислительного стресса под влиянием химиопрепаратов.
) в опухолевых клетках в результате развития окислительного стресса под влиянием химиопрепаратов.
В ряде работ было установлено, что, регулируя содержание 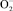 , параллельно являясь Н2О2-образующим ферментом, СОД может влиять на процессы клеточного деления. Так, снижение активности СОД способствует как накоплению
, параллельно являясь Н2О2-образующим ферментом, СОД может влиять на процессы клеточного деления. Так, снижение активности СОД способствует как накоплению 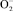 , усиливающего пролиферацию опухолевых клеток, так и уменьшению концентрации Н2О2, способной ингибировать размножение клеток. При стимуляции дифференцировки опухолевых клеток активность СОД возрастает, а увеличение её содержания в опухолевых клетках позволяет им вернуть такие характеристики нормальных клеток, как контроль роста [9, 12, 13]. Таким образом, активация СОД влияет на соотношение концентрации различных оксидантов в опухоли, способствуя ингибированию пролиферации опухолевых клеток.
, усиливающего пролиферацию опухолевых клеток, так и уменьшению концентрации Н2О2, способной ингибировать размножение клеток. При стимуляции дифференцировки опухолевых клеток активность СОД возрастает, а увеличение её содержания в опухолевых клетках позволяет им вернуть такие характеристики нормальных клеток, как контроль роста [9, 12, 13]. Таким образом, активация СОД влияет на соотношение концентрации различных оксидантов в опухоли, способствуя ингибированию пролиферации опухолевых клеток.
Полагаем, что полученные результаты о содержании в опухолевых образцах промежуточного продукта ПОЛ – МДА у больных контрольной и основной групп не противоречат предположению о развитии окислительного стресса в опухоли. По данным литературы, для многих опухолей характерно изменение липидного состава, например, снижение концентрации ненасыщенных жирных кислот в мембранах, являющихся субстратом ПОЛ, а также низкий стационарный уровень ПОЛ [3, 5, 6], что согласуется с нашими данными. После проведенного лечения уровень МДА в ткани неоплазмы снижался еще больше. Учитывая, что активность каталазы и ГПО в основной группе не изменялась, такое снижение может быть следствием не только восстановления липопероксидов антиоксидантами, но и усиления ПОЛ, которое приводит к истощению субстрата и соответственно к наблюдаемому на момент исследования снижению концентрации МДА.
Опираясь на концепцию тканевой теории канцерогенеза, основанной на гипотезе о нарушении тканевого гомеостаза, мы сочли необходимым изучить состояние окислительных процессов в перифокальной зоне и интактной морфологически неизмененной ткани. В контрольной группе единственным выявленным различием показателей активности антиоксидантных ферментов в образцах перифокальной и интактной зоны было высокое значение активности каталазы и соответственно коэффициента каталаза/ГПО в неизмененной ткани. Такое повышение активности каталазы, вероятно, имеет компенсаторный характер, обусловленный развитием оксидативного стресса. На это также указывает уровень МДА в интактной ткани, который, несмотря на активацию фермента, достоверно не отличался от значений в перифокальной зоне.
После проведения НАБХТ, происходило достоверное снижение активности каталазы и концентрации МДА в интактной ткани по сравнению с контролем. В образцах перифокальной зоны, напротив, отмечалось усиление каталазы и ГПО, при этом содержание МДА менялось незначительно. Наблюдаемая в перифокальной зоне перестройка системы антиоксидантной защиты дает основания предполагать, что НАБХТ индуцирует локальный оксидативный стресс. Учитывая высказанное Нейфахом Е.А. [3] и подтвержденное экспериментами предположение о том, что опухоль может являться «антиокидантным паразитом», а также известную способность опухоли к генерации АФК, можно предположить, что, формируя «опухолевое поле», неоплазма способствует развитию оксидативного стресса в прилегающих к ней тканях. В то же время компенсаторная активация антиоксидантых ферментов в перифокальной зоне и связанное с ней изменение пропорции оксидантов, происходящая под действием химиотерапии, приводит к формированию своеобразного «метаболического» барьера, защищающего интактную зону от воздействия опухоли.
Заключение
Полученные результаты дают основание полагать, что одним из механизмов действия НАБХТ является усиление генерации свободных радикалов и индукция окислительного стресса в опухоли и перифокальной зоне, а также снижение интенсивности окисления в неизмененной ткани. Клиническую эффективность предложенного метода подтверждают результаты трёхлетнего наблюдения за больными, получавшими лечение: в контрольной группе возникновение рецидивов и метастазов было отмечено у 8 больных, в основной группе только у одного больного. Таким образом, перитуморальное введение химиопрепаратов приводит к сопряженному изменению свободнорадикального метаболизма в изучаемых зонах, что способствует угнетению опухолевого роста и уменьшению вероятности распространения опухолевого процесса.
Рецензенты:
Микашинович З.И., д.б.н., профессор, заведующая кафедрой общей и клинической биохимии № 1, ГБОУ ВПО «Ростовский государственный медицинский университет» Минздрава РФ, г. Ростов-на-Дону;
Каймакчи О.Ю., д.м.н., ассистент кафедры онкологии, ГБОУ ВПО «Ростовский государственный медицинский университет» Минздрава РФ, г. Ростов-на-Дону.
Работа поступила в редакцию 07.05.2013.
Библиографическая ссылка
Качесова П.С., Андрейко Е.А., Горошинская И.А., Ващенко Л.Н., Внуков В.В., Шалашная Е.В., Аушева Т.В., Нескубина И.В. ВЛИЯНИЕ НЕОАДЬЮВАНТНОЙ КОМБИНИРОВАННОЙ ХИМИОТЕРАПИИ НА АУТОСРЕДАХ НА СОСТОЯНИЕ АНТИОКСИДАНТНОЙ СИСТЕМЫ ОПУХОЛИ И ОКРУЖАЮЩИХ НЕОПЛАЗМУ ТКАНЕЙ У БОЛЬНЫХ САРКОМАМИ МЯГКИХ ТКАНЕЙ // Фундаментальные исследования. 2013. № 5-2. С. 291-295;URL: https://fundamental-research.ru/en/article/view?id=31606 (дата обращения: 28.04.2026).



