Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE DEVELOPMENT PROCESS OF TECHNOLOGICAL METHODOLOGY TO INCREASED OF THE SOLUBILITY OF ACICLOVIR
В настоящее время вирусные конъюнктивиты остаются одной из главных причин обращений к офтальмологам в мире и, несмотря на успехи в лечении этого заболевания, приоритетным направлением в предупреждении вирусных конъюнктивитов различной этиологии является полное и комплексное лечение первоначального заболевания без возникновения рецидивов.
С этой целью на современном фармацевтическом рынке существует ряд препаратов, основная часть которых в своем составе содержит противовирусные действующие компоненты. Однако большинство противовирусных препаратов являются однокомпонентными, непролонгированными, что противоречит современным подходам к рациональному проведению комбинированной фармакотерапии заболеваний.
Такой подход предполагает сочетание нескольких лекарственных веществ в одной лекарственной форме с целью оптимизации терапии многофакторных патологий, к которым относятся и вирусные конъюнктивиты, а также возможной синергичности фармакологического эффекта.
На российском фармацевтическом рынке отсутствуют противовирусные препараты пролонгированного действия, что вызывает необходимость многократного применения существующих препаратов и, как следствие, удлиняет курс медикаментозного лечения, а также не решает проблем, связанных с низкой биодоступностью глазных капель. Исходя из этого, становится очевидной научная актуальность разработки конкурентоспособных многокомпонентных препаратов пролонгированного действия для предупреждения и лечения вирусных конъюнктивитов.
Согласно самым последним оценкам Министерства здравоохранения и социального развития РФ, около 4,7 миллионов человек в Российской Федерации имеют нарушения зрения, вызванные глазными болезнями или нескорректированными рефракционными погрешностями. Из этого числа около 1,6 миллионов человек страдают вирусными конъюнктивитами различной этиологии [4].
По данным Уфимского научно-исследовательского института глазных болезней, заболеваемость конъюнктивитами составляет в среднем 160 случаев на 10000 населения. В структуре воспалительных заболеваний глаз конъюнктивиты составляют около 62 % и около трети от всех глазных патологий.
Наиболее часто встречаются конъюнктивиты аденовирусной этиологии (17,9 %). Установлена взаимосвязь заболеваемости конъюнктивитами населения с неблагоприятными экологическими, климатогеографическими и производственными факторами. В Белгородской области, по данным Роспотребнадзора за 2011 г., конъюнктивиты составляли 38,1 % от всех внутрибольничных инфекций среди всех возрастов населения.
Особое значение в вирусной патологии глаз принадлежит вирусу простого герпеса. Причем основную роль занимают рецидивирующие случаи столкновений с вирусом простого герпеса Herpessimplex. Первичный герпетический конъюнктивит чаще имеет фолликулярный характер. Для герпетического конъюнктивита характерны следующие признаки: поражен один глаз, в патологический процесс часто вовлекаются края век, кожа и роговица.
Рецидив герпеса может протекать как фолликулярный или везикулярно-язвенный конъюнктивит, но обычно развивается как поверхностный или глубокий кератит.
Вирус герпеса третьего типа (вирус Varicella-Herpes Zoster) является возбудителем двух различных по клинике заболеваний: опоясывающего лишая (герпес зостерконьюнктивит) и ветряной оспы. Герпес зостер вирус вызывает глазные проявления, как правило, при поражении первой ветви тройничного нерва в виде коньюнктивита, склерита, кератита, ирита, иридоциклита. Характерны линейные групповые буллезные односторонние высыпания, возникающие наиболее часто на коже лица. Локальная боль может возникать за несколько дней до появления высыпаний.
Герпес зостер конъюнктивит может протекать с увеличением фолликулов коньюнктивы или петехиями, а также в виде некротизирующего мембранозного конъюнктивита. После появления сыпи постановка диагноза не представляет трудностей. Локализация высыпаний по ходу нервов, одностороннее поражение, выраженные неврологические боли – важные дифференциальные признаки поражения герпес зостер.
На сегодняшний день офтальмогерпес представляет проблему из-за широкой распространенности. По многолетним наблюдениям МНИИ ГБ им. Гельмгольца, у 50-83 % пациентов возникают рецидивы. Согласно статистическим данным Центра по офтальмогерпесу РФ, первое место по распространенности занимают герпетические конъюнктивиты и кератоконъюнктивиты, вызываемые вирусом простого герпеса первого типа, вторую позицию занимают вирусы герпеса второго типа.
Доля цитомегаловируса невелика среди основной массы взрослого населения, однако представляет существенную часть вирусных заболеваний глаз у лиц с ослабленным иммунитетом, например, у лиц, страдающих иммунодефицитами различной природы и геронтологических пациентов. На долю вируса герпес-зостер приходится до 70 % вторичных заболеваний органа зрения у детей.
Сложившаяся ситуация требует проведения активной работы в рамках расширения ассортимента лекарственных препаратов для предупреждения и лечения вирусных конъюнктивитов.
Наибольшее распространение среди лекарственных форм для лечения вирусных конъюнктивитов занимают глазные капли, их число на рынке составляет около 43 %. Вторую позицию удерживают глазные мази – 27 %. Третье место приходится на долю лиофилизатов для интравивитриального введения. Доля остальных лекарственных форм не превышает 3 %. Ведущую роль играют препараты на основе ацикловира, их около 22 %. Несколько меньшее распространение получили препараты на основе интерферона альфа 2b и идоксуридина, 19 и 8 % соответственно, на остальные АФС приходится менее 5 %. В глазных мазях наиболее часто встречается ацикловир около 60 %, доли остальных действующих веществ примерно равны и составляют по 10 %. К ним относят идоксуридин, бромнафтохинон, теброфен, флореналь.
Наиболее распространенной фармацевтической субстанцией для лечения вирусных конъюнктивитов является ацикловир. Вторую позицию занимает идоксуридин. Третье место принадлежит интерферону альфа-2b. Доля остальных противовирусных субстанций для лечения вирусных конъюнктивитов в офтальмологических лекарственных формах незначительна.Согласно данным Центра по офтальмогерпесу, работающему на базе НИИ глазных болезней РАМН, наилучшим образом отвечают современным требованиям, предъявляемым к лечению активных проявлений герпетической болезни глаз, два химиотерапевтических противовирусных препарата: полудан и ацикловир. Характерно, что оба препарата наряду с выраженным ингибирующим воздействием на вирус простого герпеса обладают минимальным побочным действием (токсико-аллергические реакции). Это позволяет применять их достаточно длительно не только местно в виде инстилляций и аппликаций, но и системно, что является основной предпосылкой для успешной терапии тяжелых проявлений офтальмогерпеса. Идоксуридин не может длительно применяться из-за худшей переносимости и возможного тератогенного эффекта, он также является потенциальным канцерогеном и мутагеном.
По результатам проведенного маркетингового исследования установлено, что одной из наиболее эффективных противовирусных субстанций является ацикловир, который практически не растворим в воде, что затрудняет его использование в лекарственной форме – глазные капли [2]. Поэтому разработка методики повышения растворимости ацикловира в воде является актуальной задачей.
Повысить растворимость активных фармацевтических субстанций позволяет использование механохимических подходов в фармацевтической промышленности [3]. Механохимические процессы приводят к разупорядочению, аморфизации и полиморфным переходам кристаллических решеток веществ, конформационным превращениям в составляющих решетки молекулах, что ведет к изменению реакционной способности и биологической активности лекарственных веществ, и могут быть использованы для создания новых эффективных технологий, получения новых активных веществ, изменения свойств лекарственных веществ и лекарственных форм [4].
Вследствие механической обработки некоторых соединений происходит увеличение их растворимости, что обусловливает необходимость использования методов микродиспергирования с целью повышения растворимости активных фармацевтических субстанций.
Целью исследования является разработка методики повышения растворимости ацикловира в воде для создания состава глазных капель комплексного действия для лечения вирусных конъюнктивитов.
Материалы и методы исследования
Материалы исследования: ацикловир AciclovirSuzhouLeaderImp.&Exp. Co., Ltd. (China), СAS59277-89-3 c содержанием ацикловира ≥ 98 %, USP 27/BP2000/BP 1998, бетациклодекстрин ОАО «Леко-Стайл», г. Санкт-Петербург, USP 25, CAS 7585-39-9, ПЭГ-6000 Merck, (Germany), CAS25322-68-3, EPh 5.0, коллидон К-25 CN107443, Merck (Germany), EPh 5.0 Povidone 01/2005:0685, НД 42-8482-98, ДМСО стандартный образец.
Методы исследования: микродиспергирование, ультразвуковая гомогенизация, спектрофотометрический метод.
Результаты исследования и их обсуждение
С целью оптимизации пути решения поставленных задач разработан алгоритм исследования, включающий 3 основных этапа (рисунок).
В соответствии с разработанным алгоритмом исследования на первом этапе проводилось изучение механохимической обработки ацикловира, изучение распределения частиц ацикловира по размерам, определение растворимости ацикловира.
Второй этап алгоритма предполагает исследование с солюбилизаторами: бета-циклодекстрином, полиэтиленгликолем-6000, коллидоном К-25. В рамках данного этапа исследований проводится исследование активности солюбилизаторов для образования легкорастворимых комплексов с ацикловиром.
Третий этап алгоритма исследования предполагает исследование растворимости ацикловира с сорастворителем диметилсульфоксидом, позволяющим повысить растворимость ацикловира и увеличить биодоступность глазных капель.
По результатам первого этапа исследования установлено, что оптимальный режим измельчения ацикловира составляет 10 минут в вибрационной шаровой мельнице МЛ-1, при этом в раствор переходит около 4,2 % ацикловира, что на 0,8 % превышает растворимость неизмельченной субстанции.
На втором этапе исследования определяли растворимость ацикловира при добавлении солюбилизатора, способствующего образованию комплекса с нерастворимой субстанцией. Согласно литературным данным, перспективными солюбилизаторами являются бета-циклодекстрин и полиэтиленгликоль-6000, а также коллидон К-25 [5]. Прежде всего определяли растворимость ацикловира при различных режимах измельчения с солюбилизаторами. При исследовании с бета-циклодекстрином установлено, что оптимальное время измельчения составляет 30 минут. При изучении соотношения активная фармацевтическая субстанция солюбилизатор установлено, что при увеличении количества солюбилизатора растворимость комплекса с ацикловиром снижается. Поэтому оптимальное соотношение ацикловирбета-циклодекстрин составляет 1:1, при этом в растворе обнаружено около 20 % ацикловира.
В ходе изучения растворимости ацикловира с солюбилизаторами была выдвинута гипотеза о том, что совместное измельчение двух вспомогательных субстанций позволит образовать легко растворимый комплекс с активным компонентом. При совместном измельчении бета-циклодекстрина и полиэтиленглиголя-6000 установлено, что оптимальное время измельчения субстанций составляет 20 минут, при этом количество полиэтиленгликоля-6000 должно составлять 1:2 к комплексу ацикловирбета-циклодекстрин.
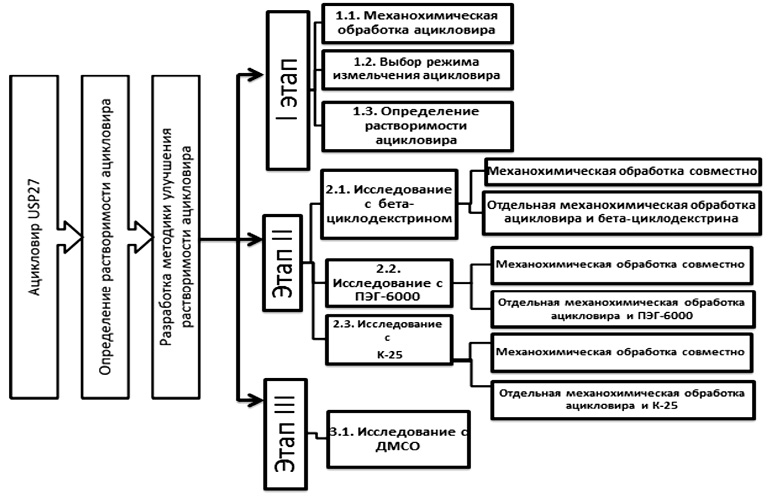
Алгоритм исследования
При дальнейшем исследовании ацикловира с солюбилизаторами проводили изучение растворимости комплекса ацикловирбета-циклодекстрин с коллидоном К-25, способным увеличить растворимость комплексов активных веществ при совместном супрамикроструктурировании. При совместном измельчении бета-циклодекстрина и коллидона К-25 установлено, что оптимальное время измельчения субстанций составляет 20 минут, при этом количество коллидона К-25 должно составлять 1:4 к комплексу ацикловирбета-циклодекстрин.
Согласно результатам второго этапа исследования установлено, что при сочетанном применении двух солюбилизаторов при использовании режима супрамикроструктурирования субстанции в раствор переходит около 94 % ацикловира.
На третьем этапе исследования выдвинута гипотеза, что растворение активного комплекса с солюбилизатором в диметилсульфоксиде, который может быть использован в составе глазных капель, позволит увеличить растворимость ацикловира.
Согласно результатам, полученным на третьем этапе исследования, установлено, что при предварительном растворении комплекса ацикловира с бета-циклодекстрином в диметилсульфоксиде количество ацикловира перешедшего в раствор, превышает на 4, 9 % результаты опыта без введения дополнительного растворителя на втором этапе исследования. Полученные результаты представлены в таблице.
Как видно из таблицы, оптимальным режимом обработки субстанции ацикловира является измельчение в течение 10 минут с бета-циклодекстрином, микродиспергированным совместно с коллидоном К-25 в течение 30 минут ввиду достижения максимального количества перешедшего в раствор ацикловира при использовании этого технологического режима.
Выводы
В ходе исследования достигнуто увеличение растворимости ацикловира на 90,1 % по сравнению с неизмельченной субстанцией, что подтверждает необходимость введения стадии микродиспергирования субстанции и солюбилизаторов для обеспечения повышения растворимости исходного вещества для разработки состава и технологии глазных капель противовирусного действия на основе ацикловира.
Составы водных растворов ацикловира
|
Номер образца |
Способ обработки |
Процент ацикловира, перешедшего в раствор из навески, % |
Стандартное отклонение |
|
I этап 1.1. |
Ацикловир неизмельченный |
3,4 |
±0,03 |
|
1.2.-1.3. |
Ацикловир, измельченный в течение 10 минут |
4,2 |
±0,02 |
|
II этап 2.1. |
Ацикловир, измельченный в течение 10 минут с бета-циклодекстрином, измельченным в течение 30 минут, 1:1 |
20 |
±0,01 |
|
2.2. |
Ацикловир, измельченный в течение 10 минут с бета-циклодекстрином, измельченным в течение 30 минут, с ПЭГ-6000, 1:2 |
70,1 |
±0,0046 |
|
2.3. |
Ацикловир, измельченный в течение 10 минут с бета-циклодекстрином, измельченным в течение 30 минут, с коллидоном К-25, 1:4 |
94 |
±0,007 |
|
IIIэтап 3.1. |
Ацикловир, измельченный с бета-циклодекстрином, измельченным в течение 30 минут при растворении ДМСО |
24,9 |
±0,006 |
Работа выполнена в рамках Задания Министерства образования и науки РФ НИУ БелГУ № 3.2473.2011 по теме «Технологические аспекты разработки новых составов инновационных лекарственных форм на основе супрамикро/наноструктурированных субстанций».
Рецензенты:
Новиков О.О., д.фарм.н., профессор, заведующий кафедрой фармацевтической химии и фармакогнозии, Белгородский государственный национальный исследовательский университет, г. Белгород;
Кочкаров В.И., д.фарм.н., профессор кафедры фармацевтической химии и фармакогнозии, Белгородский государственный национальный исследовательский университет, г. Белгород.
Работа поступила в редакцию 22.04.2013.
Библиографическая ссылка
Жилякова Е.Т., Баскакова А.В., Новикова М.Ю. РАЗРАБОТКА ТЕХНОЛОГИЧЕСКОЙ МЕТОДИКИ ПОВЫШЕНИЯ РАСТВОРИМОСТИ АЦИКЛОВИРА // Фундаментальные исследования. 2013. № 6-3. С. 646-650;URL: https://fundamental-research.ru/en/article/view?id=31565 (дата обращения: 15.05.2026).



