Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
DEVELOPMENT AND RESEARCH COMBINED OINTMENT OPPOSES RHEUMATOID ACTION CONTAINING DMSO
Доминирующими препаратами при лечении ревматоидного артрита являются НПВС, это объясняется тем, что они обладают выраженными свойствами: противовоспалительным и анальгезирующим, однако они способны вызвать побочные эффекты, особенно при их пероральном применении. Альтернативой этому может быть использование наружных лекарственных форм, а также субстанций растительного происхождения, которые также характеризуются противовоспалительной и антиоксидантной активностью [1, 5]. Одним из главных аспектов эффективности действия наружной лекарственной формы является степень высвобождения лекарственного вещества, которая зависит от его проникающей способности
Поэтому усиление пенетрирующей способности для наружных лекарственных форм, на наш взгляд, очень важно. В связи с этим становится актуальным достижение успешного действия лекарственных препаратов; решение этой задачи возможно при усилении пенетрации лекарственного средства, которая возможна в следующих случаях: при использовании пенетраторов, лекарственного электрофореза или каких-либо средств доставки например, липосом [7].
Для предполагаемого усиления пенетрирующего эффекта, на наш взгляд, имело смысл добавить такой сопутствующий компонент, как ДМСО, который наряду с противовоспалительной активностью является пенетратором и не обладает выраженными побочными явлениями при накожных аппликациях в концентрации до 40 %.
В последние годы в качестве составляющих компонентов таких лекарственных форм все чаще используют извлечения из лекарственного растительного сырья. В связи с этим в состав конструируемой мази было включено извлечение из лекарственного растительного сырья – травы горца птичьего. Извлечения получали методом реперколяции 70 % этиловым спиртом в батарее из 3-х перколяторов.
В качестве основного компонента, обладающего противовоспалительным действием, была использована мефенаминовая кислота – производное антраниловой кислоты. Она обладает анальгезирующей, жаропонижающей и противовоспалительной активностью, причем как противовоспалительное средство превосходит по активности салицилаты. По анальгезирующей активности мефенамовая кислота равноценна бутадиону.
Таким образом, был сформирован состав мази: экстракт травы горца птичьего 10 %, ДМСО 15 %, мефенаминовая кислота 1 % [4].
Были проведены биофармацевтические исследования in vitro, методом диффузии в желатиновый гель [2]. Для этого были выбраны следующие основы: эмульсионная основа, основа ПЭГ, ланолин–лецитин, бенецел (метилцеллюлоза, маркаE 15), эмульсионная основа вазелин–натрий лаурил сульфат [3]. Приготовленный 3 % раствор желатина делили на две части. В одну часть в качестве реактива полифенольные структуры вводили раствор хлорида железа, в другую – раствор алюминия хлорида. Наилучшую высвобождаемость показали основы: сплав ПЭГ, эмульсионная основа и бенецел. Результаты исследования представлены в табл. 1.
Для дальнейших фармакологических исследований нами была выбрана основа на сплаве ПЭГ, показавшая наибольшую высвобождаемость действующих компонентов по сравнению с другими основами.
Материалы и методы исследования
Противовоспалительное действие экстракта изучали методом онкометрии [6]. Опыты проводили на белых беспородных крысах-самках массой 150–180 г. Животных отбирали таким образом, чтобы исходный средний объем лапок во всех экспериментальных группах был примерно одинаков.
Таблица 1
Результаты биофармацевтического исследования выбранных основ
|
Мазевая основа |
Зона высвобождения |
|
|
Реактив |
||
|
Железа хлорид (III) |
Алюминия хлорид |
|
|
ПЭГ(сплав) |
19 мм |
17 мм |
|
Эмульсионная основа |
14 мм |
12 мм |
|
Бенецел |
13 мм |
12 мм |
Принцип метода состоит в следующем. Крысам субплантарно (под апоневроз лапки) водили 0,1 мл 10 % суспензии каолина в качестве флогогена. Это вызывало развивающеися во времени отек лапки. Степень отека отражала интенсивность воспаления. Величину отека измеряли по количеству вытесненной из капсулы онкометра воды при погружении в нее лапки. Экспериментальных животных разбивали на 3 группы по 6 особей в каждой.
Первой группе вводили только каолин. Эта группа являлась контрольной. Животным второй группы за 30 мин до введения каолина наносили 5 % мазь бутадиона в количестве 0,1 г. Животным третьей группы за 30 мин до субплантарного введения каолина наносили 1 % мазь мефенаминовой кислоты с ДМСО и экстрактом горца птичьего.
Онкометрическое измерение объема лапки проводили через 1, 2, 3 и 24 часа после введения каолина.
Результаты исследования и их обсуждение
Результаты опытов представлены в табл. 2. Результаты подвергали статистической обработке по методу Стьюдента.
Таблица 2
|
Исходный объем лап |
Объем лап через 1 час |
Объем лап через 2 часа |
Объем лап через 3 часа |
Объем лап через 24 часа |
|
|
Контроль |
0,91 ± 0,05 |
1,16 ± 0,05 |
1,22 ± 0,04 |
1,23 ± 0,04 |
1,47 ± 0,06 |
|
Бутадион |
0,97 ± 0,05 Р > 0,05 |
1,21 ± 0,05 Р > 0,05 |
1,33 ± 0,04 Р > 0,05 |
1,1 ± 0,03 Р < 0,05 |
1,20 ± 0,06 Р < 0,05 |
|
Мефенаминовая к-та |
0,98 ± 0,04 Р > 0,05 Р1 > 0,05 |
1,18 ± 0,02 Р > 0,05 Р1 > 0,05 |
1,23 ± 0,04 Р > 0,05 Р1 > 0,05 |
1,22 ± 0,04 Р > 0,05 Р1 > 0,05 |
1,21 ± 0,04 Р < 0,05 Р1 > 0,05 |
Примечание: Р – достоверность по отношению к контролю, Р1 – достоверность по отношению к бутадиону.
Опыты показали, что исходный объем лапок крыс во всех группах был примерно одинаков и статистически достоверных различий не наблюдалось (Р > 0,05). В группе животных, получавших мазь бутадиона, через 1 час после введения каолина не наблюдалась тенденция к снижению нарастания отека по отношению к контрольной группе (табл. 2). Соответственно в контроле объем лапки составлял 1,16 ± 0,05 мл, в группе с бутадионом – 1,21 ± 0,05 Р > 0,05. В опытной группе, получавшей мазь мефенаминовой кислоты, также не наблюдалось достоверных изменений. Ко второму часу не наблюдалось достоверных различий по сравнению с контрольной группой. К третьему часу исследования достоверные различия по отношению к контролю (Р < 0,05) были зафиксированы в группе сравнения. Причем на второй и третий час опытная группа, которая подвергалась обработке мазью мефенаминовой кислоты, проявляла тенденцию к снижению отека по отношению к группе, получавшей бутадионовую мазь, но достоверности в различиях не наблюдалось (Р > 0,05) . Через 24 часа после введения каолина объем лапок не достигал исходного уровня ни в одной из исследуемых групп животных. Однако наибольший отек оставался в контрольной группе 1,47 ± 0,06, достоверно ниже был в группе, получавшей мазь бутадиона1,20 ± 0,06 (Р < 0,05) и достоверно ниже по отношению к контролю, но недостоверно ниже к бутадиону – в опытной группе 1,21 ± 0,04 (Р > 0,05).
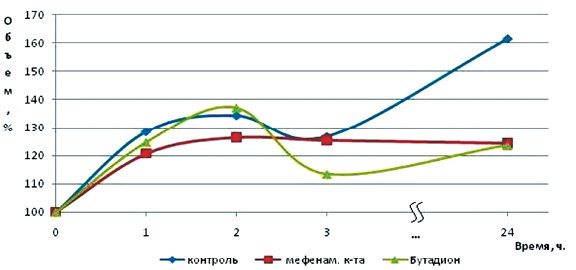
Динамика нарастания отека в % по отношению к исходному объему лапки
Выводы
Таким образом, из результатов проведенного эксперимента видно, что разработанная мазь, содержащая 1 % мефенаминовой кислоты, 15 % ДМСО и экстракта горца птичьего 10 %, обладает противовоспалительным действием, несколько меньшим по сравнению с мазью бутадиона, но показывает более пролонгированное действие и к 24 ч в эксперименте снижает отек сопоставимо с мазью бутадиона. При сравнении с мазью бутадиона 5 % было установлено, что исследуемая мазь обладает более пролонгированным эффектом и к 24 ч в эксперименте снижает отек сопоставимо с препаратом сравнения.
Рецензенты:
Андреева И.Н., д.фарм.н., профессор Российского государственного института туризма и сервиса МГУС, г. Москва;
Маршалкин М.Ф., д.х.н., профессор Северо-Кавказского государственного университета, г. Пятигорск.
Работа поступила в редакцию 11.04.2013.
Библиографическая ссылка
Белов П.М., Степанова Э.Ф., Огурцов Ю.А. РАЗРАБОТКА И ИССЛЕДОВАНИЕ КОМБИНИРОВАННОЙ МАЗИ ПРОТИВОРЕВМАТОИДНОГО ДЕЙСТВИЯ, СОДЕРЖАЩЕЙ ДМСО // Фундаментальные исследования. 2013. № 6-3. С. 638-640;URL: https://fundamental-research.ru/en/article/view?id=31563 (дата обращения: 25.05.2026).



