Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
STATE OF VISUAL ANALYZER WITH THE USE OF DRUGS TIOGAMMA IN DIABETES MELLITUS TYPE 1
Среди патологических состояний нервной системы, возникающих при заболеваниях эндокринных желез, особое место занимают неврологические расстройства при сахарном диабете (СД). Это обусловлено не только распространенностью подобных нарушений, но и их тяжестью, значительным влиянием на прогноз и качество жизни. СД является одним из самых распространенных заболеваний в мире. По мнению экспертов к 2025 году общее число больных диабетом достигнет 324 млн человек [8]. В настоящее время в РФ около 8 миллионов человек страдают СД и их число непрерывно растет [2]. Несмотря на то, что доля СД 1 типа от всех форм диабета составляет не более 10–15 % [2, 3], данная форма является важнейшей медико-социальной проблеме здравоохранения, т.к. это заболевание нередко возникает в детском и юношеском возрасте, характеризуется тяжестью течения, ранней инвалидизацией и нередко смертельным исходом [2].
Сосудистые поражения наблюдаются при всех формах сахарного диабета. Однако при СД 1 типа основной причиной высокой инвалидизации являются именно микроангиопатии, которые приводят к диабетической ретинопатии (ДР) [6,7]. Отмечено, что СД занимает одно из первых мест как причина слепоты и слабовидения во всех возрастных группах. Риск развития слепоты у больных СД в 25 раз выше, чем у людей без СД [4, 5]. В этой связи изучение состояния всего пути зрительного анализатора при сахарном диабете 1 типа имеет особое значение.
Цель исследования: уточнить нейрофизиологическое состояние проводящих путей зрительного анализатора у больных сахарным диабетом 1 типа до и после лечения.
Материалы и методы исследования
Был обследован 31 пациент (12 мужчин и 19 женщин; средний возраст 21,3 ± 2,10 года) с диагнозом «СД 1 типа», находившихся на лечении в эндокринологическом отделении ГКБ № 3 г. Ставрополя. Средняя продолжительность заболевания у них составила 5,1 ± 2,1 лет. Всем больным было проведено клинико-лабораторное обследование, включающее определение антител к основному белку миелина (ОБМ), которые определялись методом иммуноферментного анализа с применением набора реагентов, разработанного Ястребовой Н.Е. и Ванеевой Н.П. (фирма «Навииа», г. Москва).
Большинство обследованных находились в состоянии декомпенсации СД. Клиническое состояние зрительного анализатора у больных изучалось совместно с офтальмологом. Критерием возможности проведения исследования явилось наличие СД 1 типа с начальной стадией диабетической ретинопатии или без изменений на глазном дне. Из числа исследуемых пациентов были исключены лица с анизометропией, миопией выше 1,0 диоптрии, астигматизмом, амблиопией, экзофорией, цветоаномалиями, какими-либо другими (кроме диабетической ретинопатии) глазными заболеваниями или травмами, никому ранее не проводилась фотолазеркоагуляция.
Для оценки зрительного анализатора проводилось нейрофизиологическое исследование на приборе «Нейро-МВП/4» производства фирмы «НейроСофт» с компьютерной обработкой, разработанном в Академии МТН РФ (г. Иваново). Изучался латентный период (ЛП) и амплитуда ответа вызванных зрительных потенциалов (ВЗП) на реверсный черно-белый шахматный паттерн. Достоинством данного исследования является наиболее четкое выделение в графическом отображении основной волны Р100, что соответствует активации 17-го (первичная зрительная кора) и 18-го (зрительная ассоциативная кора) поля по Бродману [1]. Метод позволяет проследить проведение нервного импульса по зрительным волокнам, начиная от клеток сетчатки (палочки), по зрительному нерву, через зрительный тракт и структуры среднего мозга до затылочный доли коры головного мозга [1]. Кроме этого, он даёт количественную оценку скорости проведения по зрительному анализатору. Исследование проводилось по стандартной методике. Активный электрод размещался над затылочной областью в отведении О2, О1 международной схемы «10–20 %» и заземляющим электродом на лбу (в точке Fрz). Ипсилатеральный в точке Сz. Импеданс под электродами составлял не более 5 кОм. Стимуляция проводилась на сменяющийся черно-белый шахматный паттерн поочередно на левый и правый глаз, в затемненной комнате с предварительной адаптацией в положении сидя. Эпоха анализа – 500 мс. Число усреднений – 70–100. Оценивались компоненты ответа N75, P100 и N145 мс. Преимущественно делался упор на изучение основного компонента Р100 и амплитуды волны N75–P100.
Для уточнения состояния биоэлектрической активности (БЭА) корковых структур головного мозга изучалась электроэнцефалограмма (ЭЭГ) на приборе «Нейро-МВП/4». Проводили визуальный и компьютерный анализ 16 монополярных отведений: Fp1, Fp2, F3, F4, F7, F8, C3, C4, P3, P4, O1, O2, T3, T4, T5, T6 по международной схеме «10–20 %» с референтным электродом на мочке ипсилатерального уха. Эпоха анализа составляла 4 с при частоте дискретизации 250 в 1 с. Спектр плотности мощности в каждом отведении, нормированный на собственную мощность суммарной ЭЭГ, анализировали с шагом 0,125 Гц в интервале от 0,5 до 35 Гц. Заземляющий электрод устанавливался на лобный полюс – Fpz при импедансе не более 40 кОм. Определяли следующие частотные диапазоны ЭЭГ: δ – 0,5–3,5 Гц, θ – 4–7 Гц, α – 8–13 Гц, β1 – 14–20 Гц, β2 – 21–40 Гц.
Обследование больных осуществлялось до и после проведенного базового лечения, основу которого составило использование препарата «Тиогамма». Последний вводился в дозе 600 мг внутривенно на 200 мл физиологического раствора в течение 10 дней, после чего повторно проводилось нейрофизиологическое исследование. В лечении больных СД использовали современные принципы терапии: наряду с диетотерапией и медикаментозной терапией применяли обучающие программы. Средняя суточная доза инсулина составила 39,1 ± 2,32 ЕД. Все пациенты получали человеческие инсулины фирм Novo-Nordisk и Eli Lilly по интенсифицированной схеме инсулинотерапии. Контрольную группу составили 15 здоровых взрослых, сопоставимых по возрасту и полу.
Для анализа полученных результатов использовали расчет средних арифметических величин (М) и их ошибок (m), среднеквадратичное отклонение (δ). Достоверность различий средних значений оценивали с использованием критерия Стьюдента (t).
Результаты исследования и их обсуждения
При клиническом обследовании у 18 (58,1 %) больных была диагностирована диабетическая энцефалопатия, проявлением которой явились жалобы астенического характера: общая слабость, повышенная утомляемость, снижение работоспособности, тревожность, эмоциональная лабильность, нарушение концентрации внимания, снижение памяти. В 67,7 % случаев выявлялся цефалгический синдром. Следует отметить, что головная боль чаще носила характер сжимающей, сдавливающей по типу «тесного головного убора».
Симметричная дистальная полинейропатия встретилась у 28 (90,3 %) пациентов. При этом больных беспокоили покалывания, онемение, зябкость стоп и реже кистей или ощущение жжения, боль в конечностях, которое чаще усиливалось в ночное время или в покое. У больных было выявлено снижение болевой, температурной или вибрационной чувствительности по типу «носков» и «перчаток», снижение рефлексов, тонуса в отдельных случаях умеренные двигательные нарушения. Гипостезия постепенно распространялась от дистальных отделов ног и рук к проксимальным.
Во всех случаях пациенты отмечали синдром вегетативной дистонии в виде разлитого дермографизма, диффузного гипергидроза, акроцианоза. В 3 случаях больные отмечали развитие предобморочных состояний. Вследствие поражения вегетативных волокон в 5 (16,1 %) случаях у больных развились вегетативно-трофические расстройства в виде артропатии, проявляющихся прогрессирующей деформацией голеностопного сустава и суставов стопы.
У 11 (35,5 %) пациентов отмечалась депрессия разной степени выраженности, которая, на наш взгляд, являлась следствием болезни.
Проведенное нейрофизиологическое обследование позволило выявить ряд закономерностей (таблица). Так, анализируя результаты ЗВП было установлено, что у больных с СД 1 типа по сравнению с обследованными контрольной группы по показателю волны Р100 отмечалось увеличение ЛП справа и слева до проводимого лечения, которое составило 119,3 ± 2,58 мс против 103,1 ± 1,72 мс в контроле (р < 0,05). Также достоверные изменения в этот период по показателям ЛП были диагностированы у поздних компонентов ВП. Так, ЛП волны N145 составил 172,3 ± 3,66 мс против 151,3 ± 2,22 мкВ в группе контроля (р < 0,05). Следует отметить, что удлинение ЛП волны Р100 наблюдалось у подавляющего большинства обследованных (в 87,1 % случаев).
Динамика количественных показателей ВЗП у обследуемых больных с сахарным диабетом 1 типа до и после лечения (М ± m)
|
Период |
СД 1 типа (n = 31) до лечения |
СД 1 типа (n = 25) после лечения |
Контрольная группа (n = 15) |
|
Латент. период (мс) N75 Р100 N145 Ампл. (мкВ) P100 |
76,1 ± 2,81 119,3 ± 2,58* 172,7 ± 2,73* 4,3 ± 1,63 |
74,3 ± 3,93 110,6 ± 2,74 149,9 ± 2,21 7,2 ± 1,36 |
72,1 ± 2,09 103,1 ± 1,72 151,3 ± 2,22 8,1 ± 1,21 |
Примечание. * – достоверные различия (р < 0,05) – с контрольной группой.
Проведенный курс с использованием в базисной терапии препарата «Тиогамма» позволил выявить тенденцию к восстановлению ЛП (рисунок).
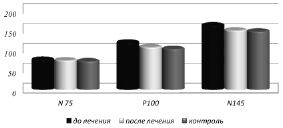
Показатели компонентов ЗВП относительно контрольной группыдо и после лечения Тиогаммой в мс
Анализ амплитуды волны N75-P100 показал, что у больных имело место снижение амплитуды ответа на предъявляемый стимул. Так, у обследованных больных амплитуда волны N75-Р100 составила 4,3 ± 1,63 мкВ, что характеризовало состояние депрессии зрительных корковых структур. Для уточнения полученных данных, в частности, депрессивного характера имеющихся изменений параллельно проводилось исследование ЭЭГ с регистрацией БЭА головного мозга. Результаты исследования позволили отметить, что нейрофизиологические показатели ЭЭГ по частотным и амплитудным характеристикам практически были сопоставимы с данными контрольной группы. Так, у пациентов с СД средние показатели амплитуды альфа-ритма составили 75,8 ± 2,3 мкВ, средняя частота альфа-ритма – 9,6 ± 1,1 Гц, средний индекс – 71 %. Результаты ЭЭГ характеризуют, что БЭА головного мозга в корковых зрительных зонах функционально остаются в состоянии, близком к контрольной группе. Это дает основание считать, что снижение амплитуды ответа по результатам ВЗП связано со снижением импульсного потока по волокнам зрительного анализатора и, как следствие этого, уменьшением числа нейронов, которые активируют ответную реакцию коры на предъявляемый стимул. В этой связи мы считаем, что снижение проводимости по волокнам зрительного анализатора может являться следствием процессов демиелинизации. Для уточнения данных изменений были проведены иммунологические исследования, связанные с уточнением концентрации антител Ig G к основному белку миелина. Было выявлено, что концентрация уровня антител IgG к ОБМ у больных СД до проводимого лечения превышала уровень контрольной группы и составила соответственно 156,2 ± 4,22 и 50 ± 2,1 мкг/мл. Полученные иммунологические изменения дополнительно могут свидетельствовать о процессах демиелинизации, следствием которых являются снижение проводимости по волокнам зрительного анализатора.
Существующая теория о переходном процессе, связанная с оценкой ответа мозга на импульсное воздействие, связана с работой целой системы мозга: корково-подкорковым гомеостазом, ретикулярной формации ствола, ответственной за поддержание процессов сна-бодрствования, внимания и пр. [1]. На наш взгляд, результаты импульсного воздействия и, в частности, ВЗП позволяют дать объективную оценку не только состоянию зрительного анализатора, но и в целом иметь объективное представление о функциональном состоянии головного мозга.
Заключение
Таким образом, полученные результаты указывают, что при СД 1 типа происходят процессы демиелинизации в структурах зрительного анализатора, которые способствуют снижению «потока» проводимости зрительного импульса в корковые структуры зрительного анализатора, что приводит к снижению ответной корковой реакции на предъявляемый стимул. Использование препарата «Тиогамма» в лечении СД 1 типа позволяет значительно улучшить метаболические процессы в структурах зрительного анализатора и тем самым восстановить их функциональное состояние.
Рецензенты:
Cтародубцев А.И., д.м.н., профессор, кафедра неврологии Ставропольского государственного медицинского университета, г. Ставрополь;
Христофорандо Д.Ю., д.м.н., доцент, заведующий отделением челюстно-лицевой хирургии городской клинической больницы скорой медицинской помощи, г. Ставрополь.
Работа поступила в редакцию 04.04.2013.
Библиографическая ссылка
Францева А.П., Карпов С.М., Белякова Н.А., Седакова Л.В., Францева В.О., Чичановская Л.В., Шевченко П.П. СОСТОЯНИЕ ЗРИТЕЛЬНОГО АНАЛИЗАТОРА ПРИ ИСПОЛЬЗОВАНИИ ПРЕПАРАТА «ТИОГАММА» ПРИ САХАРНОМ ДИАБЕТЕ 1 ТИПА // Фундаментальные исследования. 2013. № 5-1. С. 164-167;URL: https://fundamental-research.ru/en/article/view?id=31484 (дата обращения: 11.05.2026).



