Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
IMMUNOHYSTOCEMICAL ANALYSIS OF SOME INDICATORS OF THYMOPOIESIS AT CARCINOGENESIS IN CONDITION OF SECONDARY IMMUNODEFICIENCY
Растущее злокачественное новообразование и иммунная система находятся в сложных многоуровневых перекрестных взаимодействиях, изучение которых открывает новые возможности для иммунотерапии опухолей, однако ее эффективность находится в прямой зависимости от сохранности иммунной реактивности организма [8]. Рост злокачественной опухоли сопровождается продукцией веществ, способных снижать или полностью блокировать противоопухолевый иммунный ответ. Опухоль при этом перестает распознаваться иммунными клетками и становится биологически более агрессивной [13].
В настоящее время известно, что один из ключевых механизмов иммуносупрессии при канцерогенезе опосредован через стимуляцию опухолью дендритных клеток и клеток-регуляторов (T-reg cells), которые способны оказывать как местное, так и системное угнетение иммунного ответа [7]. Другим важным условием формирования иммунной реакции организма на рост опухоли имеет направленность иммунного ответа. Известно, что в зависимости от преобладания в зоне иммунной реакции Т-хелперов 1 или 2 типа опухоль либо распознается и уничтожается иммунными клетками, либо ускользает от иммунного надзора [2]. Среди возможных механизмов иммуносупрессивного влияния опухоли на тимус также различают недостаточное поступление в железу костномозговых предшественников, нарушение дифференцировки тимоцитов и усиление апоптоза, а также повышенную миграцию клеток на периферию [3].
Немаловажное значение в прогрессии злокачественных новообразований принадлежит иммунодефицитам. Хронические иммунодефициты могут способствовать недостаточному иммунному ответу на рост опухоли, а также формированию клинически агрессивных опухолей, что, в частности, наблюдается у больных ВИЧ-инфекцией [9]. Известно, что спленэктомия вызывает комплекс патологических сдвигов со стойким нарушением гуморального и клеточного иммунитета, получивший обозначение «постспленэктомический гипоспленизм» [1, 6, 12].
В наших предыдущих работах описана динамика изменений морфологии и молекулярного фенотипа тимуса в моделях с канцерогенезом, возрастной инволюцией и спленэктомией [4, 6]. Однако в доступной литературе по-прежнему отсутствуют работы по исследованию изменений иммуногистохимического фенотипа тимуса при канцерогенезе на фоне вторичной иммунной недостаточности после спленэктомии.
Цель исследования – оценка молекулярных характеристик тимопоэза у животных с экспериментальным канцерогенезом на фоне вторичной иммунной недостаточности после спленэктомии.
Материалы и методы исследования
Работа выполнена на 60 белых нелинейных крысах-самцах 4 и 5 месяцев массой 180–220 г. Уход и содержание животных проводили в соответствии с «Правилами проведения работ с использованием экспериментальных животных». Крысы были разделены на две группы. Первой группе животных (30 крыс) внутрибрюшинно водили 1,2-диметилгидразин из расчета 20 мг/кг массы 1 раз в неделю в течение 5 недель в соответствии с экспериментальной моделью [10]. Животным второй группы (30 крыс) предварительно выполнялась спленэктомия. Операцию проводили с соблюдением правил асептики и антисептики под местной анестезией. Через 30 суток после спленэктомии крысам водили 1,2-диметилгидразин в дозе и схеме, указанной выше. Выведение животных обеих групп из эксперимента проводилось через 30, 90 и 150 суток после окончания введения канцерогена путем декапитации. Объектом исследования служил тимус. В работе применялись следующие методы:
1. Иммуногистохимический метод с использованием четырех коммерческих моноклональных антител (МКАТ) производства Novo Castra (Великобритания):
– МКАТ к кластеру дифференцировки лимфоцитов 3 типа;
– МКАТ к антиапоптотическому белку bcl-2;
– МКАТ к белку-регулятору апоптоза p-53;
– МКАТ к белку клеточной пролиферации Ki-67.
Материал для исследования методом иммуногистохимии фиксировали 10 % нейтральным забуференным формалином в течение 24 ч, выполняли стандартную спиртово-ксилоловую проводку. Подготовленные образцы тканей заливали в парафин, готовили срезы толщиной 4 мкм, которые наносили на высокоадгезивные стекла и высушивали при температуре 37 °С в течение 18 ч. Демаскировка и иммуногистохимическая окраска проводилась ручным способом с использованием системы визуализации NovoLink polymer (Novo Castra, Великобритания). Контролем иммуногистохимической реакции служила неиммунизированная сыворотка.
2. Окраска срезов тимуса гематоксилином и эозином для изучения общегистологической картины микропрепаратов.
3. Компьютерная морфометрия. Линейные морфометрические измерения выполнены с использованием лицензионной программы Leica Application Sute 3.6.0. Количественные измерения интенсивности мембранных и цитоплазматических иммуногистохимических реакций выполнены с применением лицензионной программы «Микро-Анализ» (Россия), а также демо-версии программы Sigma Scan Pro (Япония). Интенсивность мембранной иммуногистохимической реакции оценена методом автоматического выделения и подсчета площади интересующего цветового спектра, окрашенного диаминобензидином (DAB), по отношению к площади снимка с переводом числовых значений в проценты. Для каждого среза выполнены измерения не менее чем в 10 интересующих полях зрения. При малом количестве окрашенных клеток проводили визуальный подсчет их количества в 10 интересующих полях зрения. Результат ядерной реакции оценивали путем подсчета позитивно окрашенных ядер на 100 клеток в десяти полях зрения при увеличении х400, выражая результаты в процентах.
4. Статистическая обработка с использованием лицензионного пакета программ MS Office 2003, достоверность определялась t-критерием Стьюдента.
Результаты исследований и их обсуждение
Через месяц после окончания введения канцерогена в слизистой оболочке толстой кишки крыс обеих групп формируются очаговые пролифераты крипт без признаков клеточной атипии. Морфологических отличий в строении тимуса при обработке гематоксилином и эозином у животных обеих групп не выявляется. При окраске тимуса антителами к CD 3 отмечается положительная реакция в многочисленных клетках коркового и мозгового вещества, число которых достоверно не отличается. Обработка препаратов тимуса антителами к белкам-регуляторам апоптоза bcl-2 и p-53 выявляет немногочисленные клетки, локализованные в корковом и мозговом веществе. Установлено, что у животных с изолированным введением канцерогена число bcl-2+ не превышает 2,43 ± 0,18 в поле зрения, тогда как у крыс с введением канцерогена на фоне спленэктомии их число значительно возрастает до 6,67 ± 0,16 (P ˂ 0,001). Количество клеток, позитивных к p-53, достоверно не изменяется. Исследование маркера клеточной пролиферации выявляет небольшое, но достоверное снижение (P ˂ 0,01) количества пролиферирующих клеток в структурах коркового и мозгового вещества у животных с введением канцерогена на фоне спленэктомии.
Через три месяца после окончания введения канцерогена в толстой кишке крыс регистрируются признаки предопухолевых изменений. Обработка препаратов тимуса животных обеих групп гематоксилином и эозином демонстрирует начальные признаки инволюции в виде расширения междольковых септ и уменьшения размеров долек. Окраска препаратов тимуса животных со спленэктомией антителами к CD 3 выявляет значительное снижение (P ˂ 0,001) CD 3+ клеток в мозговом веществе, тогда как в корковом веществе достоверные изменения отсутствовали. Обработка антителами к белку-регулятору апоптоза p-53 выявляет более чем двукратное уменьшение p-53+ клеток (P ˂ 0,001) в структурах дольки спленэктомированных животных, тогда как экспрессия bcl-2 не имеет достоверных отличий в двух экспериментальных группах. При исследовании маркера клеточной пролиферации Ki-67 отмечено небольшое, но достоверное уменьшение (P ˂ 0,01) экспрессии этого антигена в структурах коркового вещества (до 23,2 %) у животных со спленэктомией и введением канцерогена, тогда как экспрессия Ki-67 в структурах мозгового вещества достоверно не изменяется.
Через пять месяцев после окончания введения канцерогена в толстой кишке животных обеих групп формируется опухоль, имеющая морфологию дифференцированной аденокарциномы. У спленэктомированных крыс на этом сроке тимус значительно уменьшен в размерах, дряблый, желтоватого цвета. Большая часть паренхимы железы подвержена атрофии и замещена жировой тканью. Сохранившиеся дольки значительно уменьшены в размерах, граница коркового и мозгового вещества едва различима. Иммуногистохимическое исследование тимуса у крыс этой группы выявляет достоверные и существенные отличия экспрессии антигенов во всех исследуемых структурах. Обработка препаратов тимуса антителами к CD 3 выявляет значительное (P ˂ 0,001) снижение количества зрелых тимоцитов в корковом (до 22,3 %) и мозговом (до 15,59 %) веществе (рис. 1, 2). Исследование маркеров апоптоза выявляет двукратное снижение (P ˂ 0,001) экспрессии bcl-2 и более чем двукратное повышение (P ˂ 0,001) экспрессии p-53 в структурах тимуса спленэктомированных крыс. Обработка препаратов антителами к Ki-67 выявляет двукратное (P ˂ 0,001) снижение экспрессии этого маркера в корковом веществе и более чем пятикратное (P ˂ 0,001) снижение в мозговой зоне (рис. 3, 4).
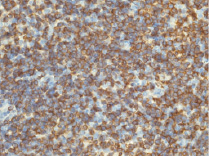
Рис. 1. Тимус крысы через 5 месяцев после введения канцерогена. Экспрессия CD3 в тимоцитах мозгового вещества. Иммуногистохимическая реакция с CD3, ув.400
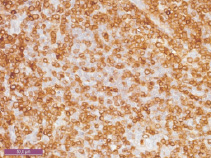
Рис. 2. Тимус спленэктомированной крысы через 5 месяцев после введения канцерогена. Уменьшение CD3 + тимоцитов в мозговом веществе. Иммуногистохимическая реакция с CD3, ув.400
Наши исследования показали, что через один месяц после введения канцерогена достоверные отличия морфологии тимуса у животных двух групп отсутствуют. Однако в молекулярном фенотипе тимуса отмечаются небольшие, но достоверные отличия. Раньше других изменяются показатели клеточной пролиферации, а также экспрессия антиапоптотического белка bcl-2. Вероятно, эти изменения следует расценивать как последствия спленэктомии.
Существенные отличия молекулярного фенотипа тимуса в двух группах регистрируются через три месяца после введения канцерогена и проявляются в снижении количества CD3+ тимоцитов мозгового вещества, экспрессии белка p-53 и Ki-67 в структурах дольки у животных со спленэктомией. На стадии формирования карциномы через пять месяцев достоверные отличия морфологии и молекулярного фенотипа вилочковой железы у животных двух групп регистрируются во всех исследуемых структурах. При этом у спленэктомированных крыс отмечается снижение числа зрелых тимоцитов, которое сочетается со снижением клеточной пролиферации и изменением соотношения белков апоптоза, что может указывать на угнетение тимопоэза.
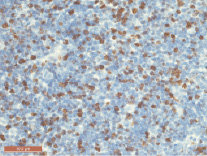
Рис. 3. Тимус крысы через 5 месяцев после введения канцерогена. Экспрессия Ki-67 в клетках мозгового вещества. Иммуногистохимическая реакция с Ki-67, ув.400
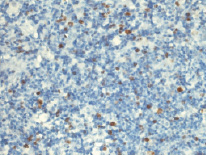
Рис. 4. Тимус спленэктомированной крысы через 5 месяцев после введения канцерогена. Снижение экспрессии Ki-67 в клетках мозгового вещества дольки. Иммуногистохимическая реакция с Ki-67, ув. 400
По данным литературы удаление селезенки сопровождается активацией пучковой зоны надпочечников и повышением уровня глюкокортикоидов в крови [5, 6]. Известно, что глюкокортикоидные гормоны способны угнетать продукцию клеток костным мозгом, и, следовательно, поступление предшественников тимопоэза в тимус [11]. Мы считаем, что регистрируемое угнетение тимопоэза у животных с канцерогенезом на фоне спленэктомии может быть обусловлено как токсическим влиянием самой опухоли, так и нарушением поступления клеток–предшественников в железу вследствие влияния повышенного уровня глюкокортикоидов.
Таким образом, наши исследования показали, что развитие экспериментальной злокачественной опухоли толстой кишки на фоне вторичной иммунной недостаточности после спленэктомии изменяет и усугубляет течение инволютивных изменений в тимусе по сравнению с изолированным введением канцерогена. При этом в железе на фоне атрофии большей части паренхимы регистрируются признаки выраженного угнетения тимопоэза.
Рецензенты:
Валькович Э.И., д.м.н., профессор, заведующий кафедрой гистологии и эмбриологии ГБОУ ВПО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава РФ, г. Санкт-Петербург;
Ямщиков Н.В., д.м.н., профессор, заведующий кафедрой гистологии и эмбриологии, ГБОУ ВПО «Самарский государственный медицинский университет» Минздрава РФ, г. Самара.
Работа поступила в редакцию 04.04.2013.
Библиографическая ссылка
Москвичев Е.В ИММУНОГИСТОХИМИЧЕСКИЙ АНАЛИЗ НЕКОТОРЫХ ПОКАЗАТЕЛЕЙ ТИМОПОЭЗА ПРИ КАНЦЕРОГЕНЕЗЕ В УСЛОВИЯХ ВТОРИЧНОЙ ИММУННОЙ НЕДОСТАТОЧНОСТИ // Фундаментальные исследования. 2013. № 5-1. С. 101-105;URL: https://fundamental-research.ru/en/article/view?id=31468 (дата обращения: 16.05.2026).



