Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
EFFECT OF HYDROGEN PEROXIDE ON CA2+-DEPENDENT POTASSIUM PERMEABILITY OF THE MEMBRANE OF HUMAN ERYTHROCYTES UNDER COMPRESSION CELLS
Долгое время активные формы кислорода (АФК) рассматривались исключительно в качестве агентов, отрицательно влияющих на жизнедеятельность клетки. В частности, это обусловлено их ведущей ролью в патогенезе многих заболеваний: избыточная и неконтролируемая продукция АФК приводила к активации процессов перекисного окисления липидов, что, в конечном итоге, вызывало изменение физико-химических свойств мембраны и связанного с этим транспорта ионов через клеточную мембрану.
В последнее время все чаще появляются работы, в которых АФК рассматриваются в качестве регуляторов внутриклеточных процессов. Активные формы кислорода либо сами выступают в роли вторичных посредников [1;2], либо модулируют действие известных регуляторных каскадов клетки [10]. Один из регуляторных путей связан с влиянием АФК на ионтранспортные системы клеток.
Мембрана эритроцитов содержит Са2+-активируемые калиевые каналы (К+(Са2+)-каналы) средней проводимости или Gardos-каналы. Их открывание приводит к утечке ионов К+ и, вследствие этого, к гиперполяризации мембраны эритроцитов. Относительно недавно была установлена физиологическая роль К+(Са2+)-каналов: они вносят определенный вклад в программируемую гибель эритроцитов – эриптоз [11;12], изменение объема клеток [8]. Кроме того, показано их участие в деформируемости клеток: Са2+-индуцируемое снижение деформируемости эритроцитов устраняется при их блокировании или выравнивании градиента ионов калия [7].
Один из путей регуляции К+(Са2+)-каналов эритроцитов связан с белками цитоскелета клеток без участия протеинкиназ [5; 6].
В процессе своего функционирования эритроциты подвергаются действию активных форм кислорода, продуцируемых как внутри них, так и другими клетками (эндотелиоцитами, иммунокомпетентными клетками). Таким образом, АФК могут влиять на регуляторные пути красных клеток крови [9].
Целью настоящего исследования явилось изучение влияния перекиси водорода на Са2+-зависимую калиевую проницаемость мембраны эритроцитов в условиях сжатия клеток.
Материал и методы исследования
Исследования проводили на венозной крови практически здоровых доноров-добровольцев в возрасте 20–25 лет. Для исследования Са2+-зависимой калиевой проницаемости был применен метод регистрации мембранного потенциала в суспензии эритроцитов по изменениям рН среды инкубации в присутствии протонофора, основанный на том, что в этих условиях распределение протонов зависит от мембранного потенциала. [3]. В качестве параметров, характеризующих Са2+-зависимую калиевую проницаемость, использовали ΔE – амплитуду гиперполяризационного ответа (ГО), значение мембранного потенциала, соответствующие максимальному уровню гиперполяризации мембраны в ответ на добавление А23187 (мВ).
Для выяснения влияния АФК на Са2+-зависимую калиевую проницаемость мембраны эритроцитов в суспензию клеток добавляли перекись водорода в конечных концентрациях 1, 2, 3, 4, 5, 8 мкМ.
Для сжатия клеток упакованные эритроциты помещали в среду N (150 мМ NaCl, 1 мМ KCl, 1 мM MgCl2, 10 мM глюкозы, 10 мкМ СаСl2), содержащую 100 или 200 мМ сахарозы. Для регистрации изменений объёма эритроцитов в условиях варьирования осмолярности среды использовался метод оценки светорассеяния суспензий клеток, основанный на способности эритроцитов рассевать световой поток при длинах волн больше 600 нм, исходя из того, что оптическая плотность взвеси обратно пропорциональна объему исследуемых частиц [4]. Математическую обработку результатов проводили с использованием пакета программ SPSS for Windows 11.5. Для каждого параметра определяли значения медианы (М) и квартилей (Q2-Q3). Достоверность различия между группами определяли по непараметрическому критерию Вилкоксона.
Результаты исследования и их обсуждение
Добавление перекиси водорода в использованных концентрациях к суспензии эритроцитов не изменяло амплитуду ГО по сравнению с контролем. Использование более высоких концентраций перекиси водорода вызывало повреждение эритроцитов. Сжатие эритроцитов вследствие помещения их в среды с повышенной осмолярностью (в присутствии 100 или 200 мМ сахарозы) вызывало достоверное увеличение амплитуды ГО, что указывает на повышение Са2+-зависимой калиевой проницаемости мембраны эритроцитов (рис. 1).
Ранее было показано, что обнаруженный эффект связан с возможным влиянием белков цитоскелета на проводимость Са2+-зависимых калиевых каналов [6].
Внесение перекиси водорода (1 мкМ) в среды инкубации с повышенной осмолярностью вызывало статистически значимое снижение амплитуды ГО по сравнению с результатами, полученными при сжатии клеток в отсутствие перекиси водорода (рис. 2).
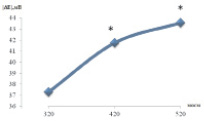
Рис. 1. Амплитуда ГО в условиях варьирования осмолярности среды инкубации. Примечание: * – достоверность изменений параметра DЕ по сравнению с контролем (р < 0,05)
Возможно, снижение Са2+-зависимой калиевой проницаемости мембраны эритроцитов в условиях повышенной осмолярности среды в присутствии перекиси водорода обусловлено непосредственным влиянием перекиси водорода на белки Са2+-активируемых калиевых каналов, либо на системы, регулирующие их активность. Однако, как было показано выше, в изоосмотической среде перекись водорода не оказывала влияния на исследуемый параметр. Другой причиной обнаруженного эффекта могло быть набухание эритроцитов в присутствии перекиси водорода. Так, в работе [13] показано, что третбутиловая перекись приводила к увеличению объема эритроцитов на 15 %.
Исследование светорассеяния суспензии эритроцитов показало, что внесение эритроцитов в гиперосмолярную среду повышает оптическую плотность раствора до 1,81 (1,78–1,88) по сравнению с изоосмолярной средой (1,60 (1,58–1,61)), что свидетельствует о сжатии эритроцитов. Добавление перекиси водорода (1 мкМ) в гиперосмотический раствор, содержащий 200 мМ сахарозы, не изменяло исследуемый показатель (таблица). Следовательно, перекись водорода не влияет на изменение объема эритроцитов, а действует, видимо, на более тонкие механизмы регуляции Са2+-зависимых калиевых каналов.
Таким образом, в настоящем исследовании обнаружено, что добавление микромолярных концентраций перекиси водорода в изоосмотическую среду инкубации эритроцитов не приводит к изменению амплитуды гиперполяризационного ответа. Сжатие эритроцитов вследствие помещения их в среды с повышенной осмолярностью (420 и 520 мосм) вызывает достоверное увеличение Са2+-зависимой калиевой проницаемости мембраны эритроцитов. Внесение перекиси водорода в среды инкубации с повышенной осмолярностью вызывает статистически значимое снижение амплитуды гиперполяризационного ответа по сравнению с результатами, полученными при сжатии клеток в отсутствие перекиси водорода, и этот эффект не связан с изменением объема эритроцитов. На основании проведенных исследований выдвинуто предположение, что регулирующее влияние перекиси водорода на Са2+-зависимую калиевую проницаемость мембраны эритроцитов в условиях сжатия клеток, вероятно, обусловлено ее воздействием на белки цитоскелета эритроцитов.
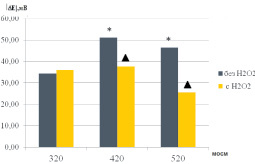
Рис. 2. Амплитуда ГО в условиях варьирования осмолярности среды инкубации в присутствии Н2О2. Примечание: * – достоверность изменений параметра DЕ по сравнению с контролем (р < 0,05)
Оптическая плотность среды инкубации (D) в условиях варьирования осмолярности и присутствия перекиси водорода (Ме (Q1-Q3))
|
№ п/п |
Условия инкубирования клеток |
n |
D |
|
1 |
320 мосм (контроль) |
8 |
1,6037 (1,5853–1,6077) |
|
2 |
320 мосм + Н2О2 (1 мкМ) |
16 |
1,5628 (1,5569–1,5912) |
|
4 |
520 мосм |
6 |
1,8180 (1,7835–1,8792) P1,2 < 0,05 |
|
5 |
520 мосм + Н2О2 (1 мкМ) |
6 |
1,771 (1,657–1,7922) P1,2 < 0,05 |
Примечание: р1,2 – показатель достоверности различий по сравнению с условиями 1 и 2.
Рецензенты:
Степовая Е.А., д.м.н., профессор кафедры биохимии и молекулярной биологии, ГБОУ ВПО СибГМУ Минздравсоцразвития России, г. Томск;
Ласукова Т.В., д.б.н., профессор кафедры медико-биологических дисциплин, ГБОУ ВПО «Томский государственный педагогический университет» Министерства образования и науки Российской Федерации, г. Томск.
Работа поступила в редакцию 19.02.2013.Библиографическая ссылка
Трубачева О.А., Петрова И.В. ВЛИЯНИЕ ПЕРЕКИСИ ВОДОРОДА НА СА2+-ЗАВИСИМУЮ КАЛИЕВУЮ ПРОНИЦАЕМОСТЬ МЕМБРАНЫ ЭРИТРОЦИТОВ ЧЕЛОВЕКА В УСЛОВИЯХ СЖАТИЯ КЛЕТОК // Фундаментальные исследования. 2013. № 3-2. С. 382-385;URL: https://fundamental-research.ru/en/article/view?id=31348 (дата обращения: 17.05.2026).



