Частично ненасыщенные N,О-содер-жащие пятичленные гетероциклы неароматической природы (пиррол-2-оны и фуран-2-оны), имеющие арилметиленовый заместитель в положении С-3 гетероцикла, занимают особое место в современной органической химии в связи с обнаружением их представителей в составе природных соединений, а также получение на их основе сложнопостроенных веществ с различного вида биологической (антибиотической, бактерицидной, кардиотонической, а также выявленной сравнительно недавно противоопухолевой) активностью. Интерес к алифатическим диазосоединениям обусловлен особенностью их строения, а также большой и чрезвычайно разнообразной реакционной способностью. Они играют важную роль при получении циклических соединений, конденсированных и каркасных структур, природных соединений, в том числе алкалоидов, гормонов и т. д. Таким образом, так как и алифатические диазосоединения, и производные пиррол(фуран)-2-она являются многоцентровыми соединениями, обладающими биологической активностью, то изучение особенностей их взаимодействия представляет значительный интерес как в теоретическом, так и в прикладном аспектах.
Арилметиленовые производные пиррол-2-онов и фуран-2-онов является чрезвычайно интересными в химическом отношении соединениями.
В структуре изучаемых соединений содержится несколько реакционных центров, способных подвергаться атаке диазоуксусного эфира: экзо- и эндоциклическая двойные углерод-углеродные связи, карбонильная группа, лабильные связи цикла (С-О и С-Н). В связи с этим можно было ожидать разнообразных превращений: диполярное циклоприсоединение по двойной углеродной связи гетероцикла, атака по карбонильной группе с образованием эпокси производных, атака по экзоциклической двойной углеродной связи, расщепление цикла за счет внедрения в наиболее лабильные связи цикла.
Проведение взаимодействия между арилметиленовыми производными пиррол-2-она и фуран-2-она и диазоуксусным эфиром при 60°С (кипячение в хлороформе при соотношении реагентов 1:1) позволило выделить продукт, который по данным элементного анализа, ИК- и ЯМР1Н спектроскопии был определен нами как 2-карбэтокси-4-(арилметилен)-6-арил-пирид(пиран) -3-оны.
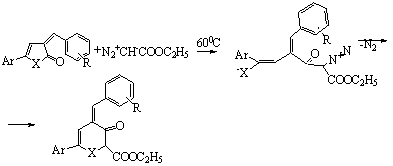
Х=NН Ar=4H3C-C6H4 R=H; 2-NO2; 3-NO2.
X=O Ar=C6H5; 4-H3CJ-C6H4 R= 2-Cl; 2-NO2; 3-NO2.
Образование полученных продуктов можно представить как атаку нуклеофильного центра диазоуксусного эфира на атом углерода субстрата, имеющий наибольший дефицит электронной плотности. Нами проведен квантово-химический расчет методом РМ3, на основании данных которого показано, что наибольший d+ на атоме углерода карбонильной группы субстрата, на который направлена атака нуклеофильного центра диазоуксусного эфира, что приводит к расщеплению цикла по связи О-С2 с последующей стабилизацией промежуточной структуры элиминированием молекулы азота и дальнейшей гетероциклизацией цвиттер-иона в пирид (пиран)-3-он.
При изменении условий протекания реакции (смена растворителя) возможно получение других продуктов реакции. Известно, что в реакциях с диазосоединениями на структуру продукта сильно влияет полярность растворителя. При замене хлороформа на неполярный тетрахлорметан можно было надеяться на сохранение азота диазокомпоненты и образование гетероспирановой структуры. Протекание реакции в тетрахлорметане сопровождалось образованием продуктов, отличающихся от полученных ранее.
Таким образом, проведенные экспериментальные исследования показали, что диазоуксусный эфир с 3-арилметилен-3Н-пиррол(фуран)-2-онами, не затрагивая другие реакционные центры и без образования гетероспирановых структур, селективно реагирует по карбонильной группе лактонного цикла, что сопровождается расщеплением цикла и образованием пиридоновой и пираноновой структур.
Работа выполнена при финансовой поддержке Российского Фонда Фундаментальных Исследований (грант № 05-03-32196).



