Идентификация генотипов пшеницы по аллельным вариантам HMW субъединиц глютенинов является важным звеном в маркер-вспомогательной селекции сортов с высокими мукомольно-хлебопекарными качествами зерна [1, 2, 3, 4, 5].
Наиболее высокоточными подходами к оценке аллельного полиморфизма HMW субъединиц глютенинов служат способы идентификации на основе молекулярно-генетических методов исследования [1, 2, 3, 4, 5].
Так, одним из подходов к идентификации аллельных вариантов HMW-GS пшеницы является способ проведения ПЦР с праймерами: UMN19F + UMN19R (Ax1/Axnull- и Ax2*-аллели), UMN25F + UMN25R (Dx2- и Dx5-аллели) и UMN26F + UMN26R (Dy10- и Dy12-аллели) с последующей детекцией результатов реакции преимущественно методами капиллярного или вертикального гель-электрофореза в ПААГ [4].
Цель настоящей работы – молекулярная идентификация генотипов яровой пшеницы селекции ТатНИИСХ по аллельным вариантам HMW субъединиц глютенинов и апробация разработанного нами способа проведения ПЦР-ПДРФ-генотипирования с электрофорезной детекцией в агарозном геле.
Материалы и методы исследования
Молекулярно-генетическая оценка 70 образцов яровой пшеницы преимущественно селекции ТатНИИСХ на предмет идентификации генотипов по аллельным вариантам HMW субъединиц глютенинов (HMW-GS) проведена методами ПЦР- и ПЦР-ПДРФ-анализа на основе общеизвестного [4] и разработанного нами способов генотипирования.
Экстракция геномной ДНК из зерновок яровой пшеницы молочно-восковой спелости урожая 2012 г. осуществлена коммерческим набором «ДНК-сорб С» («ЦНИИ эпидемиологии», Россия).
Амплификация геномной ДНК проведена на термоциклере «PTC-200» (MJ Research) с использованием праймеров [4, 5], перечень которых представлен в табл. 1.
Таблица 1
Условия проведения ПЦР- и ПЦР-ПДРФ-анализа для идентификации аллельных вариантов HMW субъединиц глютенинов пшеницы
|
Праймеры |
Последовательности праймеров (5/-3/) |
Локус (аллели) |
Режим амплификации |
ПДРФ-анализ |
|
UMN19F |
CGAGACAATATGAGCAGCAAG |
Glu-A1 (Ax1/Axnull, Ax2*) |
×1:94 °С – 4 мин ×40:94 °С – 30 с, 60 °С – 30 с, 72 °С – 30 с ×1:72 °С – 5 м |
HaeIII 37 °C – 2 часа |
|
UMN19R |
CTGCCATGGAGAAGTTGGA |
|||
|
UMN25F |
GGGACAATACGAGCAGCAAA |
Glu-D1 (Dx2, Dx5) |
×1:94 °С – 4 мин ×40:94 °С – 30 с, 60 °С – 30 с, 72 °С – 30 с ×1:72 °С – 5 мин |
HaeIII 37 °C – 2 часа |
|
UMN25R |
CTTGTTCCGGTTGTTGCCA |
|||
|
UMN26F |
CGCAAGACAATATGAGCAAACT |
Glu-D1 (Dy10, Dy12) |
×1:94 °С – 4 мин ×40:94 °С – 30 с, 60 °С – 30 с, 72 °С – 30 с ×1:72 °С – 7 мин |
HaeIII 37 °C – 2 часа |
|
UMN26R |
TTGCCTTTGTCCTGTGTGC |
|||
|
Axnull-F |
ACGTTCCCCTACAGGTACTA |
Glu-A1 (Axnull) |
×1:94 °С – 4 мин ×40:94 °С – 1 мин, 58 °С – 1 мин, 72 °С – 1 мин ×1:72 °С – 7 мин |
|
|
Axnull-R |
TATCACTGGCTAGCCGACAA |
Детекция результатов ПЦР- и ПЦР-ПДРФ-анализа выполнена методом горизонтального электрофореза в 3 % агарозном геле в буфере ТBE (рН 8,0), содержащем этидий бромид с последующей визуализацией результатов в ультрафиолетовом трансиллюминаторе (λ = 310 нм).
Размеры фрагментов ДНК оценены по подвижности в сравнении со стандартными ДНК маркерами. В работе использованы реактивы для молекулярно-биологических исследований производства ООО «СибЭнзим» (Россия).
Выравнивание частичных нуклеотидных последовательностей аллелей HMW субъединиц глютенинов: CLUSTAL W (v. 1.83). ПЦР-ПДРФ-моделирование: NEBcutter v.2.0.
Результаты исследования и их обсуждение
По результатам практических исследований, направленных на апробацию предложенного способа проведения ПЦР-ПДРФ, нами получен обеспечиваемый заявленным способом технический результат, выраженный в эффективной идентификации аллельных вариантов HMW-GS, ввиду корректной интерпретации при электрофорезной детекции в агарозном геле генерируемых ПЦР-ПДРФ-фрагментов (рис. 2, 4, 6), сопоставимых с расчетными данными (рис. 1, 3, 5).
Отличительным признаком предложенного способа генотипирования от прототипа [4] является дополнительное введение этапа ПДРФ-анализа с эндонуклеазным расщеплением ампликонов рестриктазой HaeIII с последующей детекцией результатов анализа методом горизонтального электрофореза в агарозном геле.
В результате молекулярно-генетической оценки на предмет идентификации генотипов по аллельным вариантам Glu-A1-локуса HMW субъединиц глютенинов установлено, что из 70 происследованных образцов яровой пшеницы 13 растений (18,6 %) имели субъединицу Ax1, кодируемую аллельным вариантом Glu-A1a (Ax1-аллель), а 57 образцов (81,4 %) – субъединицу Ax2*, кодируемую аллельным вариантом Glu-A1b (Ax2*-аллель) (табл. 2).
При оценке этих же образцов яровой пшеницы по Glu-D1-локусу HMW-GS выяснено, что 44 растения (62,9 %) характеризовались наличием комбинации субъединиц Dx5 и Dy10 (5 + 10), кодируемой аллельным вариантом Glu-D1d (Dx5- и Dy10-аллели), а 26 образцов (37,1 %) имели комбинацию субъединиц Dx2 и Dy12 (2 + 12), кодируемую аллельным вариантом GluD1a (Dx2- и Dy12-аллели) (см. табл. 2).
Распределение же исследуемых генотипов по совокупной комбинации Glu-A1-/Glu-D1-локусов HMW субъединиц глютенинов было следующим: Ax1/5 + 10 = 12 (17,1 %); Ax1/2 + 12 = 1 (1,4 %); Ax2*/5 + 10 = 32 (45,7 %); Ax2*/2 + 12 = 25 (35,7 %) образцов яровой пшеницы; с преобладанием желаемой для селекции на мукомольно-хлебопекарные качества зерна комбинацией субъединиц Ax2*/5 + 10.
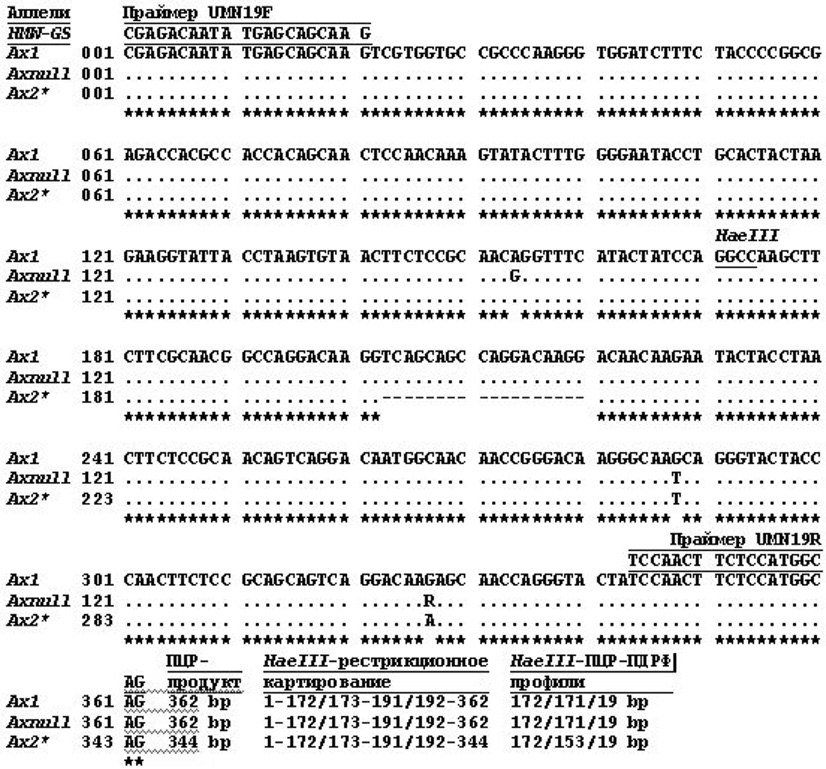
Рис. 1. Выравнивание фланкируемых с праймерами UMN19F + UMN19R нуклеотидных последовательностей Ax1-, Axnull- и Ax2*-аллелей Glu-A1-локуса HMW субъединиц глютенинов пшеницы, HaeIII-рестрикционное картирование и моделирование HaeIII-ПЦР-ПДРФ-профилей
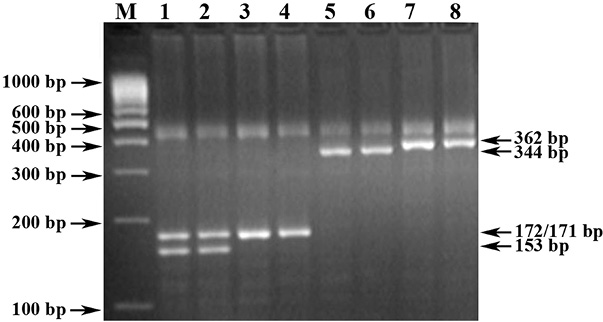
Рис. 2. Электрофореграмма технического результата предложенного способа проведения ПЦР-ПДРФ и прототипа в постановке ПЦР (праймеры UMN19F + UMN19R) для идентификации аллельных вариантов (Ax1/Axnull и Ax2*) HMW субъединиц глютенинов пшеницы
Обозначения: М) ДНК-маркеры 100 bp (СибЭнзим). 1-4) HaeIII-ПЦР-ПДРФ-анализ (предложенный способ): 1-2) Ax2*-аллель (172/153/19 bp); 3-4) Ax1/Axnull-аллели (172/171/19 bp). 5-8) ПЦР-анализ (прототип): 5-6) Ax2*-аллель (344 bp); 7-8) Ax1/Axnull-аллели (362 bp).

Рис. 3. Выравнивание фланкируемых с праймерами UMN25F + UMN25R нуклеотидных последовательностей Dx2- и Dx5-аллелей Glu-D1-локуса HMW субъединиц глютенинов пшеницы, HaeIII-рестрикционное картирование и моделирование HaeIII-ПЦР-ПДРФ-профилей
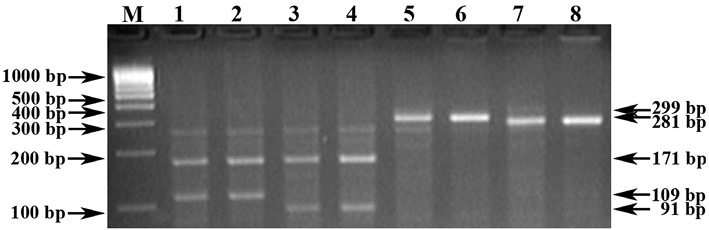
Рис. 4. Электрофореграмма технического результата предложенного способа проведения ПЦР-ПДРФ и прототипа в постановке ПЦР (праймеры UMN25F + UMN25R) для идентификации аллельных вариантов (Dx2 и Dx5) HMW субъединиц глютенинов пшеницы
Обозначения: М) ДНК-маркеры 100 bp (СибЭнзим). 1-4) HaeIII-ПЦР-ПДРФ-анализ (предложенный способ): 1-2) Dx2-аллель (171/109/19 bp); 3-4) Dx5-аллель (171/91/19 bp). 5-8) ПЦР-анализ (прототип): 5-6) Dx2-аллель (299 bp); 7-8) Dx5-аллель (281 bp).
Заключение
Учитывая общеизвестный факт положительного влияния аллельных вариантов Glu-D1d и Glu-A1b на повышение мукомольно-хлебопекарных качеств и отрицательного влияния аллельных вариантов Glu-D1a и Glu-A1a HMW-GS, приводящих к снижению хлебопекарных свойств пшеницы, можно констатировать, что из 70 исследованных образцов яровой пшеницы 32 генотипа Triticum aestivum имеют ассоциированную с высокими качествами зерна комбинацию субъединиц Ax2*/5 + 10 и могут рассматриваться как наиболее перспективные генотипы для дальнейшей селекционной работы по созданию сортов с высокими мукомольно-хлебопекарными качествами зерна.

Рис. 5. Выравнивание фланкируемых с праймерами UMN26F + UMN26R нуклеотидных последовательностей Dy10- и Dy12-аллелей Glu-D1-локуса HMW субъединиц глютенинов пшеницы, HaeIII-рестрикционное картирование и моделирование HaeIII-ПЦР-ПДРФ-профилей
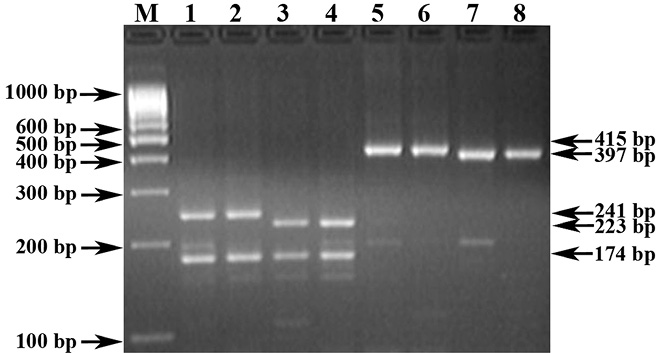
Рис. 6. Электрофореграмма технического результата предложенного способа проведения ПЦР-ПДРФ и прототипа в постановке ПЦР (праймеры UMN26F + UMN26R) для идентификации аллельных вариантов (Dy10 и Dy12) HMW субъединиц глютенинов пшеницы
Обозначения: М) ДНК-маркеры 100 bp (СибЭнзим). 1-4) HaeIII-ПЦР-ПДРФ-анализ (предложенный способ): 1-2) Dy12-аллель (241/174 bp); 3-4) Dy10-аллель (223/174 bp). 5-8) ПЦР-анализ (прототип): 5-6) Dy12-аллель (415 bp); 7-8) Dy10-аллель (397 bp).
Таблица 2
Молекулярно-генетическая оценка образцов яровой пшеницы на предмет идентификации генотипов по HMW субъединицам глютенинов
|
№ п/п |
Сорт/линия |
HMW-глютенины |
№ п/п |
Сорт/линия |
HMW-глютенины |
||||||
|
Glu-D1-локус |
Glu-A1-локус |
Glu-D1-локус |
Glu-A1-локус |
||||||||
|
5 + 10 |
2 + 12 |
Ax1 |
Ax2* |
5 + 10 |
2 + 12 |
Ax1 |
Ax2* |
||||
|
1 |
Казанская Юбилейная |
– |
+ |
– |
+ |
36 |
К-27/00-2 |
+ |
– |
– |
+ |
|
2 |
К-109/02-5 |
– |
+ |
– |
+ |
37 |
К-23/00-3 |
+ |
– |
– |
+ |
|
3 |
Экада 97 |
– |
+ |
– |
+ |
38 |
К-414/01-1 |
+ |
– |
+ |
– |
|
4 |
К-100/03-2 |
+ |
– |
– |
+ |
39 |
К-21/00 |
+ |
– |
– |
+ |
|
5 |
К-18/03-8 |
+ |
– |
– |
+ |
40 |
К-58/01-2 |
+ |
– |
– |
+ |
|
6 |
К-68/04-5 |
+ |
– |
– |
+ |
41 |
K-48/04-2 |
+ |
– |
– |
+ |
|
7 |
К-130/04-10 |
+ |
– |
– |
+ |
42 |
K-106/01-2 |
– |
+ |
– |
+ |
|
8 |
Злата |
+ |
– |
– |
+ |
43 |
K-101/04-3 |
+ |
– |
– |
+ |
|
9 |
К-88/02-19 |
+ |
– |
– |
+ |
44 |
K-112/04-2 |
+ |
– |
+ |
– |
|
10 |
К-6/01-2 |
+ |
– |
– |
+ |
45 |
K-134/04-19 |
+ |
– |
+ |
– |
|
11 |
К-5/03-6 |
– |
+ |
– |
+ |
46 |
К-51/00-3 |
+ |
– |
+ |
– |
|
12 |
К-48/03 |
+ |
– |
+ |
– |
47 |
K-133/05-5 |
+ |
– |
– |
+ |
|
13 |
К-100/03-8 |
– |
+ |
– |
+ |
48 |
K-57/05-6 |
+ |
– |
+ |
– |
|
14 |
К-21/02-5 |
– |
+ |
– |
+ |
49 |
К-117/04-4 |
+ |
– |
– |
+ |
|
15 |
К-46/04-9 |
+ |
– |
– |
+ |
50 |
К-12/04 |
– |
+ |
– |
+ |
|
16 |
К-68/04-1 |
+ |
– |
– |
+ |
51 |
К-99/05-2 |
– |
+ |
– |
+ |
|
17 |
К-23/04-1 |
+ |
– |
– |
+ |
52 |
Кк-8/06-1 |
– |
+ |
– |
+ |
|
18 |
К-49/04 |
+ |
– |
+ |
– |
53 |
Кк-71/06-3 |
+ |
– |
– |
+ |
|
19 |
К-7/04-2 |
+ |
– |
– |
+ |
54 |
Кк-8/06-6 |
– |
+ |
– |
+ |
|
20 |
Экада 113 |
– |
+ |
– |
+ |
55 |
Кк-75/06-3 |
+ |
– |
– |
+ |
|
21 |
Экада 109 |
+ |
– |
– |
+ |
56 |
Кк-11/06-11 |
+ |
– |
– |
+ |
|
22 |
К-93/05-2 |
+ |
– |
+ |
– |
57 |
Кк-11/06-10 |
+ |
– |
– |
+ |
|
23 |
К-29/02-5 |
+ |
– |
+ |
– |
58 |
Кк-69/06-4 |
– |
+ |
– |
+ |
|
24 |
К-109/02-13 |
+ |
– |
+ |
59 |
Кк-6/07-2 |
+ |
– |
– |
+ |
|
|
25 |
К-20/02-2 |
+ |
– |
– |
+ |
60 |
Кк-69/06-1 |
– |
+ |
– |
+ |
|
26 |
К-73/03-4 |
+ |
– |
– |
+ |
61 |
Кк-71/06-8 |
+ |
– |
– |
+ |
|
27 |
К-68/04-4 |
+ |
– |
– |
+ |
62 |
Кк-75/06-5 |
– |
+ |
– |
+ |
|
28 |
К-100/03-9 |
– |
+ |
– |
+ |
63 |
О-192/03-5 |
– |
+ |
– |
+ |
|
29 |
К-7/04-1 |
– |
+ |
– |
+ |
64 |
О-25/05-2 |
– |
+ |
+ |
|
|
30 |
К-65/05-2 |
+ |
– |
+ |
– |
65 |
О-206/05-2, д.515-10 |
+ |
– |
+ |
– |
|
31 |
К-11/04-8 |
– |
+ |
– |
+ |
66 |
О-186/04-1 |
+ |
– |
– |
+ |
|
32 |
Экада 66 |
+ |
– |
– |
+ |
67 |
О-464/02-2 |
– |
+ |
– |
+ |
|
33 |
Казанская Юбилейная (неполег.) |
– |
+ |
– |
+ |
68 |
О-513/00-21 |
– |
+ |
+ |
– |
|
34 |
К-65/05-1 |
+ |
– |
+ |
– |
69 |
Эр.255/00-3-1 |
– |
+ |
– |
+ |
|
35 |
Симбирцит |
+ |
– |
– |
+ |
70 |
О-28/05-2 |
– |
+ |
– |
+ |
|
Примечание: |
+ |
‒ наличие соответствующих субъединиц HMW-глютенинов |
|
– |
‒ отсутствие соответствующих субъединиц HMW-глютенинов |
Выражаем благодарность Вафину Ришаду Абдулфартовичу за оказанную финансовую поддержку.
Рецензенты:
Абрамова З.И., д.б.н., профессор кафедры биохимии Института фундаментальной медицины и биологии Казанского (Приволжского) федерального университета, г. Казань;
Багаева Т.В., д.б.н., профессор, зав. кафедрой биотехнологии Института фундаментальной медицины и биологии Казанского (Приволжского) федерального университета, г. Казань.
Работа поступила в редакцию 14.02.2013.



