Острое повреждение почек (ОПП) является серьезным и частым осложнением у больных острым инфарктом миокарда и наблюдается у 10-55 % пациентов [12, 1]. К сожалению, вышеперечисленные данные трудно сравнивать, поскольку они основаны на различных критериях диагностики ОПП. С целью стандартизации диагностики и оценки тяжести ОПП экспертами Acute Dialysis Quality Initiative (ADQI) group (2004) была предложена система стратификации тяжести ОПП - классификация RIFLE (Risk, Injury, Failure, Loss, End-stage renal disease). В 2007 году критерии RIFLE были модифицированы - предложено деление ОПП на 3 стадии. Критерии получили название AKIN (Acute Kidney Injury Network). В 2012 году опубликованы Рекомендации KDIGO [9], в основу которых положены критерии RIFLE и AKIN.
Развитие ОПП связано с увеличением смертности, повышением стоимости и увеличением длительности лечения после ОИМ [3]. Отдаленные результаты лечения больных зависят от тяжести почечного повреждения в остром периоде инфаркта миокарда: при легком ОПП риск смерти на протяжении 10 лет составляет 15 %, умерен- ном - 23 % и тяжелом - 33 % [14].
В основе лечения больных острым инфарктом миокарда с подъемом сегмента ST (ОИМпST) лежит реперфузионная терапия: чрезкожное коронарное вмешательство (ЧКВ) или тромболитическая терапия (ТЛТ) [2]. ЧКВ предполагает выполнение коронарографии, которая в 2-25 % случаев осложняется контраст-индуцированной нефропатией [13], в этой связи у больных, которым выполнялась коронарография, трудно оценить истинную частоту ОПП, обусловленную острым инфарктом миокарда.
Целью исследования явилась оценка частоты и тяжести ОПП, диагностированного согласно Рекомендациям KDIGO у больных ОИМпST, которым выполнялась ТЛТ, а также уточнение связи ОПП с внутригоспитальной летальностью.
Материалы и методы исследования
Обследовано 247 больных ОИМпST, которым в отделении неотложной кардиологии Центральной городской клинической больницы г. Ульяновска была выполнена ТЛТ. Мужчин было 196 (79 %), женщин - 51 (21 %), средний возраст больных составил 57,2 ± 10,74 лет. Характеристика больных представлена в таблице.
Характеристика больных острым инфарктом миокарда с подъемом сегмента ST
|
Показатель |
Значение |
|
Больные: Мужчины Женщины |
247 196 (79 %) 51 (21 %) |
|
Возраст, лет |
57,2 ± 10,74 |
|
Тромболитик: Стрептокиназа Проурокиназа Актилизе |
162 (66 %) 15 (6 %) 70 (28 %) |
|
Сахарный диабет в анамнезе |
28 (11 %) |
|
ИБС в анамнезе |
100 (41 %) |
|
Длительность анамнеза ИБС, лет |
4 (ИКР:2-10) |
|
Инфаркт миокарда в анамнезе |
36 (15 %) |
|
Артериальная гипертензия в анамнезе |
175 (71 %) |
|
Длительность артериальной гипертензии, лет |
10 (ИКР: 3-15) |
|
Тяжесть ОСН по Killip T. I класс II класс III класс IV класс |
121 (49 %) 106 (43 %) 5 (2 %) 15 (6 %) |
|
Креатинин сыворотки, мкмоль/л Скорость клубочковой фильтрации, мл/мин/1,73 м2 Скорость клубочковой фильтрации < 60 мл/мин/1,73 м2 |
105,3 ± 36,02
72,0 ± 26,75
82 (33 %) |
Диагностику ОИМпST, наличие показаний и противопоказаний для проведения ТЛТ, оценку ее эффективности осуществляли согласно Рекомендациям ВНОК (2007) [2]. Тяжесть острой сердечной недостаточности оценивали по T.Killip (1967). Острое повреждение почек диагностировали и классифицировали по критериям KDIGO [9].
Мы не располагали информацией о креатинине сыворотки до заболевания, в этой связи исходным считали креатинин, соответствующий расчетной скорости клубочковой фильтрации 75 мл/мин/1,73 м2 (базальный креатинин) [9]. Ни у одного из обследованных нами больных не было показаний для катетеризации мочевого пузыря, поэтому диурез определяли, основываясь на самостоятельном мочеиспускании больных.
Статистическая обработка данных проводилась с использованием программы Statistica for Windows 6.0. Достоверность различий между группами больных определяли при их нормальном распределении анализируемых параметров по t-критерию Стьюдента, для несвязанных переменных, или по критерию Вилкоксона, если распределение отличалось от нормального. Проводился однофакторный корреляционный анализ (в зависимости от вида распределения - Pearson или Kendall tau). Для сравнения двух групп по качественному признаку использовали χ2 Пирсона. Для исследования связи бинарного признака с несколькими количественными и качественными признаками использовали логистический регрессионный анализ. В случае приближенно нормального распределения данные представлены в виде M ± SD, где M - среднее арифметическое, SD - стандартное отклонение, в противном случае данные представлены в виде Me (ИКР), где Me - медиана, ИКР - интерквартильный размах: 25 процентиль - 75 процентиль. Различие считали достоверным при р < 0,05.
Результаты исследования и их обсуждение
От появления клинической картины заболевания до момента госпитализации в среднем прошло 2,5 (ИКР: 1,67-3,96) ча- са, в срок до 6 часов госпитализированы 222 (90 %) больных. ТЛТ была эффективна у 181 (73 %) больных. Суточный диурез составил 0,54 (ИКР: 0,39-0,74) мл/кг/ч. Согласно Рекомендациям KDIGO ОПП по критерию диурез наблюдалось у 84 (34 %) пациентов. Концентрация креатинина в сыворотке крови составила 105,3 ± 36,02 мкмоль/л. ОПП по критерию базальный (расчетный) креатинин диагностировано у 152 (62 %) пациентов. Все больные с олигурией имели ОПП по критерию креатинин сыворотки. На рисунке представлена тяжесть острого повреждения почек у больных острым инфарктом миокарда с подъемом сегмента ST. Гемодиализ проводили только 1 больному, у которого была 3-я стадия ОПП.
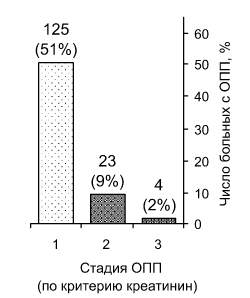
Тяжесть острого повреждения почек у больных острым инфарктом миокарда с подъемом сегмента ST
Пациенты с ОПП не отличались от больных без ОПП по возрасту: 56,3 ± 11,11 лет с ОПП и 58,5 ± 9,46 лет без ОПП (p = 0,26).
Умерло в период госпитализации 13 (5 %) больных. Внутригоспитальная летальность больных ОИМпST с ОПП, диагностированным по базальному креатинину, достоверно не различалась (χ2 = 0,29, p = 0,59), в то же время летальность была выше среди больных с олигурией (χ2 = 15,9, p = 0,0001). Логистический регрессионный анализ показал, что внутригоспитальная летальность была независимо от пола, возраста и времени от возникновения клинической картины до момента госпитализации ассоциирована с наличием ОПП по критерию диурез (относительный риск 27; 95 % ДИ 3,38-222,36; p = 0,002).
В многочисленных исследованиях продемонстрирована возможность использования критериев RIFLE и AKIN для диагностики и оценки прогноза больных с ОПП различной этиологией [8]. Как критерии RIFLE, так и AKIN предполагают оценку функции почек по двум параметрам - креатинину сыворотки и (или) диурезу [9]. Мнения о том, какой критерий использовать предпочтительней, противоречивы. В одном из исследований возможности диагностики ОПП по критерию креатинин сыворотки и по критерию диурез были изучены у больных реанимационного отделения, при этом обязательным условием включения больного в исследование было наличие постоянного катетера в мочевом пузыре. При тщательном мониторировании почасового диуреза диагностика ОПП по диурезу оказалась более точной, при этом авторы отмечают, что принятая в клинике оценка суточного диуреза не позволяет адекватно оценить почасовой диурез [11].
Ни у одного из обследованных нами больных ОИМ не было показаний для катетеризации мочевого пузыря, поэтому точное измерение почасового диуреза было невозможно. В этой связи нам не кажется неожиданной низкая чувствительность диагностики ОПП по диурезу у больных ОИМ. Учитывая высокую частоту мочевой инфекции, ассоциированной c катетеризацией мочевого пузыря [6], диагностика ОПП по диурезу у больных без четких показаний к катетеризации мочевого пузыря затруднена.
ОПП диагностировано нами у 152 (62 %) больных, если за базальный брали креатинин, соответствующий заданной СКФ 75 мл/мин/1,73 м2 [9]. Следует учесть, что у госпитализированных с инфарктом миокарда нельзя исключить наличие хронической болезни почек, частота которой среди больных кардиологических отделений нашей клиники составляет 34 % [3]. В ряде публикаций приводятся значительно более низкие показатели частоты острого повреждения почек по критерию креатинин, это связано с тем, что используя в диагностике те же критерии, авторы не учитывают больных с 1 стадией ОПП [4]. Только 11 % наших больных имели 2-3 стадию ОПП (см. рисунок).
В последние годы активно обсуждается роль биомаркеров (Neutrophil gelatinase-associated lipocalin - NGAL и др.) для диагностики и оценки прогноза ОПП [10], при этом проводятся параллели с острым коронарным синдромом, при котором определение маркеров повреждения кардиомиоцитов (тропонин) является общепринятым. Повышение тропонина является ключевым при определении тактики ведения больного с ОКС. При ОПП решение о заместительной почечной терапии будет основываться на клинических данных и вряд ли биомаркеры раннего повреждения почек повлияют на это решение. Тем не менее, маркеры могут обеспечить раннюю диагностику ОПП, что важно с целью предотвращения развития тяжелого ОПП, требующего проведения заместительной почечной терапии. В частности, для кардиологических больных крайне важно оценить состояние гидратации и характер проводимой диуретической терапии.
Так, несмотря на многообещающие результаты, полученные в ряде исследований, имеются важные ограничения при применении новых биомаркеров. Во-первых, эти исследования были проведены на небольших группах пациентов. Во-вторых, прогностическая значимость биомаркеров зависит от этиологии заболевания. ОПП часто развивается в рамках полиорганной недостаточности, что затрудняет подбор сопоставимых групп больных и требует проведения крупных исследований. В-третьих, следует учесть, что при снижении функции почек у больных ХБП, уровень биомаркеров также повышается [15].
Заключение
Более половины больных ОИМпST, которым проводилась тромболитическая терапия, имеют острое повреждение почек по критериям KDIGO. Частота ОПП, диагностированного по диурезу, почти вдвое меньше по сравнению с оценкой по базальному (расчетному) креатинину. Среди больных с ОПП, которые имеют олигурию, внутригоспитальная летальность выше, чем у больных ОИМпST без острого повреждения почек.Работа выполнена при поддержке федеральной программы «Научные и научно-педагогические кадры России» 2009-2013 г. Соглашение № 14.В37.21.1119.
Рецензенты:
Гноевых В.В., д.м.н., заведующий кафедрой пропедевтики внутренних болезней медицинского факультета Ульяновского государственного университета, г. Ульяновск;
Рузов В.И., д.м.н., профессор, заведующий кафедрой факультетской терапии медицинского факультета Ульяновского государственного университета, г. Ульяновск.
Работа поступила в редакцию 26.11.2012.
Библиографическая ссылка
Мензоров М.В., Шутов А.М., Макеева Е.Р., Серов В.А., Саенко Ю.В., Страхов А.А. ОСТРОЕ ПОВРЕЖДЕНИЕ ПОЧЕК И ВНУТРИГОСПИТАЛЬНАЯ ЛЕТАЛЬНОСТЬ У БОЛЬНЫХ ОСТРЫМ ИНФАРКТОМ МИОКАРДА С ПОДЪЕМОМ СЕГМЕНТА ST // Фундаментальные исследования. 2012. № 12-1. С. 100-103;URL: https://fundamental-research.ru/en/article/view?id=30771 (дата обращения: 15.04.2026).



