Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
NEW COMPOSITE MATERIALS BASED ON MICROCRYSTALLINE CELLULOSE AND ACRYLATE GUANIDINE DERIVATIVES
Среди структурных модификаций целлюлозы все большее значение приобретает микрокристаллическая целлюлоза (МКЦ). МКЦ обладает структурой и свойствами, отличающими ее от традиционных волокнистых или порошковых целлюлоз [6] и позволяющими ее дальнейшую химическую модификацию с целью получения биологически активных производных. Перспективными химическими структурами для получения целлюлозных материалов с биоцидными свойствами являются производные гуанидина различного строения. Присутствие в исходных ионогенных гуанидинсодержащих мономерах и полисахаридной матрице функциональных групп, способных к различного рода модификациям и взаимной иммобилизации, значительно увеличивает возможности макромолекулярного и композитного дизайна.
В то же время новые производные целлюлозы, обладающие такими ценными свойствами, как биологическая активность, термоустойчивость, ионообменность и другие, синтезируют через диальдегидцеллюлозу (ДАЦ) [2], электрофильные группы которой могут вступать во взаимодействие с широким классом нуклеофильных соединений.
В данной работе исследовано взаимодействие микрокристаллической целлюлозы (МКЦ) и ее окисленной формы (ДАЦ) с акрилатом и метакрилатом гуанидина методами рентгенодифрактометрии и ИК-спектроскопии.
Экспериментальная часть
Характеристика объектов исследования:
1) МКЦ – целлюлоза хлопковая микрокристаллическая марки «хч», содержание карбонильных групп ≈ 0,65 %, степень полимеризации (СП, n ≈ 150);
2) ДАЦ – диальдегидцеллюлоза хлопковая (МКЦ окисленная периодатом натрия) [5];
3) АГ и МАГ, полученные по методике приведенной в работе [4];
4) инициатор радикальной полимеризации ПСА –
персульфат аммония (NH4)2S2O8 марки «ч.д.а.» (перекристаллизован из бидистиллированной воды, высушен в вакууме до постоянной массы).
Все использованные реактивы по своим характеристикам соответствовали литературным данным. Количество СНО-групп в МКЦ и ДАЦ определяли по методу Соболкса [3] и титриметрически по методике [1]. ИК-спектры образцов сняты на ИК-спектрофотометре SPECORD M82 в области от 4000 до 400 см–1. Образцы для ИК-спектроскопии готовили в виде таблеток с КBr или суспензии в вазелиновом масле.
Рентгенодифракционные данные получены при комнатной температуре на автоматизированном дифрактометре ДРОН-6 (36 кВ, 20 мА, λСuКα, графитовый монохроматор на вторичном пучке, съемка по Бреггу‒Брентано в интервале углов 2θ от 5 до 75°, шаг 0,05°, скорость сканирования 1 град./мин).
Методика получения
композиционных материалов
Композиционные материалы получали обработкой МКЦ или ДАЦ мономерными водорастворимыми производными гуанидина – АГ или МАГ, имеющими цвиттер-ионную делокализованную структуру с последующей их полимеризацией.
К водной суспензии МКЦ или ДАЦ с содержанием альдегидных групп до 33 % (максимальная содержание альдегидных групп в элементарном звене 36 %) при перемешивании добавляют водный раствор АГ или МАГ и ПСА, нагревают смесь до 60 ºС и проводят полимеризацию в течение 5–20 часов. Соотношение ДАЦ:Н2О = 1:30 масс, концентрация (АГ) МАГ в воде – 1,0–3,5 %, соотношение АГ (МАГ):ПСА = 1:0,001 мас. Полученный продукт отделяют от маточного раствора и сушат.
Результаты исследования
и их обсуждение
Результаты рентгенографических и спектроскопических исследований свидетельствуют о существовании структурных различий образцов целлюлозы и ее модифицированных форм. Кривые рассеяния рентгеновских лучей исследованных образцов отличаются друг от друга положением, количеством рефлексов, относительной интенсивностью, что указывает на значительные структурные изменения МКЦ и ДАЦ после модификации гуанидинсодержащими соединениями.
На рис. 1 приведены спектры исходной МКЦ и окисленной 0,1 н раствором NaIO4. Как видно из рисунка, ДАЦ представляет собой полностью аморфизованный продукт, плотность полученных образцов также соответствует плотности аморфной целлюлозы.
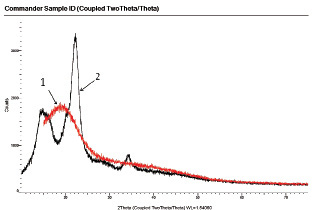
Рис. 1. Дифрактограммы ДАЦ (1) и МКЦ (2)
Интенсивность рассеяния рентгеновских лучей образцом целлюлозы, модифицированной АГ и МАГ (рис. 2), ниже, чем образцом исходной МКЦ, что указывает на снижение степени кристалличности.
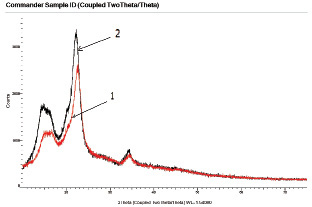
Рис. 2. Дифрактограммы МКЦ, модифицированной МАГ (1) и МКЦ (2)
Радикальная сополимеризация ДАЦ с АГ и МАГ также сопровождается уменьшением степени кристалличности (рис. 3) и значительно снижается устойчивость гликозидных связей ДАЦ по сравнению с МКЦ. Причем в случае акрилата гуанидина это приводит к тому, что часть ковалентно-связанного АГ/полиакрилатгуанидин (ПАГ) может переходить в раствор вследствие гидролитической деструкции носителя как в виде растворимых, так и нерастворимых высокомолекулярных коллоидных конгломератов. Например, чем выше степень окисления ДАЦ и чем более щелочное значение рН среды, тем легче и быстрее идет процесс гидролитической деструкции.
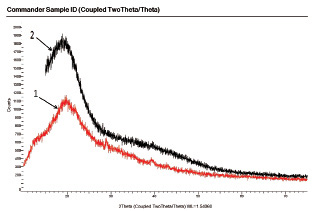
Рис. 3. Дифрактограммы ДАЦ, модифицированной МАГ (1) и ДАЦ (2)
Простая обработка МКЦ и ДАЦ водным раствором ПАГ или полиметакрилатгуанидином (ПМАГ), наоборот, приводит к увеличению степени кристалличности образцов. Видимо, выдерживание в растворе полимера приводит к частичной рекристаллизации целлюлозы.
Спектральным тестом наличия или отсутствия двойной связи в исследованных образцах является полоса поглощения в области 860–850 см–1, характерная для неплоских деформационных колебаний в узле СН2 = С < , которая позволила наблюдать не только за процессами получения ПАГ и ПМАГ и иммобилизации АГ и МАГ на МКЦ/ДАЦ, но и за исчезновением двойных связей при полимеризации гуанидинсодержащих мономеров in situ в внутри- и межфибриллярных порах целлюлозных материалов. Появление новых или исчезновение имеющихся полос в ИК-спектрах указывает на процесс взаимной модификации МКЦ/ДАЦ и мономерных и полимерных производных гуанидина, а уширение полос и сдвиг частот спектра, которые отражают локальное окружение функциональных групп, свидетельствует о взаимной иммобилизации исходных компонентов (рис. 4).
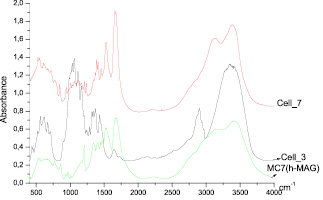
Рис. 4. Сравнение спектров ПМАГ (МС7), ДАЦ (Cell-3), ДАЦ/МАГ in situ (Cell-7)
При полимеризации МАГ в ДАЦ in situ (рис. 4, кривая Cell-7) на спектрах меняется соотношение интенсивности полос как целлюлозы (область 1000–1100 см–1), так и МАГ, кроме того, исчезает полоса в области 860 см–1, свидетельствующая о наличии двойной связи. Наблюдается расщепление полосы С = О связей ПМАГ в области 1250 см–1, что явно указывает на сильное взаимное влияние ДАЦ и МАГ/ПМГ и свидетельствует об образовании биматричных систем. Увеличение интенсивности пика 1660 см–1 в спектре ДАЦ-МАГ указывает на образование альдиминовой связи, дающей сигнал в этой области. Увеличение ширины характеристических полос поглощения в ДАЦ-МАГ в области 1450–1680 см–1, вероятно, связано с образованием относительно прочных связей МАГ с активными центрами ДАЦ.
При полимеризации АГ в ДАЦ in situ в ИК-спектрах появляется пик в области 1523 см–1 характерный для ионизованного координационно-связанного карбоксила АГ, а пик в области 1100–1160 см–1, присутствующий в ДАЦ исчезает. Очевидно, что концевые СНО-группы ДАЦ и АГ прореагировали между собой. Образование водородных связей между группами –ОН ДАЦ и С = О группами АГ сопровождается изменением относительной интенсивности полос 3500–3000 см–1.
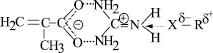
Видимо, в рассматриваемом случае катион гуанидиния взаимодействует с нуклеофильной составляющей -Xd–, в качестве которой может выступить атом кислорода альдегидной (-СНО) или гидроксильной (-ÖН) групп ДАЦ.
Для механической смеси ДАЦ-ПАГ и ДАЦ – ПМАГ на ИК-спектрах наблюдаются слабо выраженные полосы поглощения, характерные для ПАГ и ПМАГ, т.е. можно предположить, что ПАГ и ПМАГ незначительно встраивается в цепь ДАЦ. Результаты элементного анализа на азот подтвердили, что при механической обработке ДАЦ водными растворами полимеров в широком интервале концентраций степень прививки ПАГ не превышает 5 %, а ПМАГ 3 %.
Выбор ДАЦ и полимерных гуанидинсодержащих цвиттер-ионных делокализованных резонансных структур для получения новых модифицированных моно- и биматричных композиционных материалов, в которых имеются ковалентные, ионные или координационные связи целлюлозы с солями четвертичных аммониевых оснований, открывает перспективу создания наноструктур и нанокомпозитов с трансформерной полимерной матрицей, представляющих существенный научный и практический интерес. Изделия на их основе можно использовать для изготовления одежды, упаковки, перевязочных материалов медицинского назначения, а также фильтрующих мембран для стерилизации воздуха и обеззараживания речной воды, обладающих одновременно пролонгированными биоцидными и легко регенирируемыми адсорбционными свойствами, поскольку в состав гуанидинсодержащих мономеров и полимеров входят ионогенные группы.
Работа выполнена с использованием оборудования ЦКП «Рентгеновская диагностика материалов» КБГУ в рамках выполнения госконтракта № 16.552.11.7074.
Рецензенты:
Борукаев Т.А., д.х.н., профессор, зав. лабораторией ФГБОУ ВПО «Кабардино-Балкарский государственный университет
им. Х.М. Бербекова», г. Нальчик;
Лигидов М.Х., д.х.н., профессор, декан химического факультета ФГБОУ ВПО «Кабардино-Балкарский государственный университет им. Х.М. Бербекова»,
г. Нальчик.
Работа поступила в редакцию 26.10.2012.
Библиографическая ссылка
Тлупова З.А., Жанситов А.А., Эльчепарова С.А., Хаширова С.Ю. НОВЫЕ КОМПОЗИЦИОННЫЕ МАТЕРИАЛЫ НА ОСНОВЕ МИКРОКРИСТАЛЛИЧЕСКОЙ ЦЕЛЛЮЛОЗЫ И АКРИЛАТНЫХ ПРОИЗВОДНЫХ ГУАНИДИНА // Фундаментальные исследования. 2012. № 11-3. С. 739-743;URL: https://fundamental-research.ru/en/article/view?id=30607 (дата обращения: 13.05.2026).



