Введение
Для решения технологических задач, связанных с получением высокочистых веществ, в процессах разделения, извлечения, концентрирования редких и цветных металлов необходимо использовать комплексообразующие иониты, обладающие большим сродством к поливалентным и тяжелым металлам. Такими катионитами являются карбоксильные. Карбоксильный катионит КБ-4Пх2 в своей структуре содержит одну ионогенную группу - карбоксильную группу СООН.
Исследования кинетики ионного обмена позволяют установить скорость достижения равновесия, максимальную рабочую емкость ионита для определенного состава раствора и заданной температуры, механизм взаимодействия ионов с ионитом при ионном обмене, рассчитываются коэффициенты диффузии внешнего и внутреннего массопереноса.
В настоящем сообщении с использованием метода ограниченного объема [5] изучена кинетика сорбции ионов меди (II), бария, иттрия из водных растворов катионитом КБ-4Пх2. Показано влияние размера зерна ионита, скорости перемешивания и температуры. По результатам проведенного эксперимента рассчитаны коэффициенты взаимодиффузии и энергии активации суммарного процесса.
Экспериментальная часть
При исследовании кинетики ионного обмена использовался метод ограниченного объема и установка, включающая в себя термостат и реактор с мешалкой вместимостью 1 литр. В реактор помещали заранее приготовленный раствор в количестве 1 л с концентрацией компонентов 0,2 моль/л. При постоянной крупности зерен набухших ионитов в опытах менялась температура: 250С, 450С, 600С. В раствор помещался 1г набухшей смолы. Анализ всех растворов на содержание элементов проводился трилонометрическим титрованием [6]. Объем отобранных проб за время опыта не превышал 2% от общего.
Обсуждение результатов
Установление механизма кинетики сорбции является сложной задачей и требует учета всех факторов влияющих на скорость обмена (размера зерен ионита, скорости перемешивания, температуры и т.д.). Надежные сведения о механизме диффузии дает метод прерывания или "кинетической памяти". На рис. 1 представлены кинетические кривые ионов меди в опытах с прерыванием.
В случае диффузии в геле градиенты концентрации в зерне выравниваются в течение времени прерывания контакта ионита и раствора, то есть, когда обмена ионами нет. Поэтому после возобновления контакта скорость обмена оказывается большей по сравнению со скоростью, которая была до прерывания. Возрастание скорости, таким образом, служит доказательством внутридиффузионнной кинетики. Это хорошо видно на рис.1.
Внутридиффузионный характер кинетики подтверждается также отсутствием влияния на скорость сорбции ионов изменения скорости вращения мешалки реактора в пределах от 59 до 500 об/мин. Время, необходимое для достижения определенной степени завершенности процесса ионного обмена, пропорционально квадрату радиуса зерна ионита. Последнее является характерным признаком внутридиффузионнной (гелевой) кинетики. На рис. 2 представлены кинетические кривые сорбции ионов иттрия в зависимости от крупности зерен.
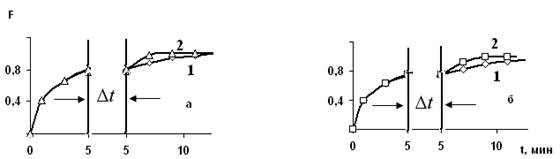
Рис. 1. Кинетические кривые сорбции ионов бария (а) и иттрия (б) из 0,2 М ![]() и
и ![]() катионитом КБ-4Пх2
катионитом КБ-4Пх2
1 - опыты без прерывания контакта фаз, 2 - опыты с прерыванием контакта фаз ![]() мин.
мин.
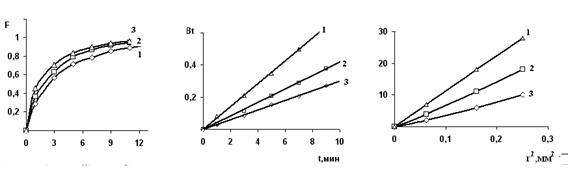
Рис. 2. Кинетические кривые сорбции ионов иттрия в зависимости от крупности зерен.
Радиус зерна ионита, мм: 0,25(1), 0,4(2) и 0,5(3).
Из данных рис. 2 видно, что с уменьшением диаметра частиц ионита скорость процесса возрастает. Это объясняется тем, что ионы исследованных металлов распределены в массе зерна неравномерно. На поверхности катионит полностью переходит в форму сорбированного металла, а в объеме зерна существует диффузионное распределение ионов с градиентом концентрации по радиусу зерна. По мере уменьшения размера зерен катионита происходит все более полный обмен. Кроме того, скорость обмена ионов иттрия обратно пропорциональна квадрату радиуса зерна. Таким образом, несколькими независимыми методами установлено, что скорость определяющей стадией сорбции является гелевая диффузия.
Обработка первичных кинетических кривых проводилась с использованием уравнения Бойда-Адомсона для внутридиффузионнной кинетики [1, 3]:
![]() ,
,
где ![]() и
и ![]() - соответственно степень насыщения ионита через t секунд и бесконечное время; F - степень обмена или степень достижения равновесия; D - коэффициент диффузии (взаимодиффузии), см2/с; r - радиус зерна ионита, мм; t - время, с; n - ряд целых чисел 1,2,3,4,5...;
- соответственно степень насыщения ионита через t секунд и бесконечное время; F - степень обмена или степень достижения равновесия; D - коэффициент диффузии (взаимодиффузии), см2/с; r - радиус зерна ионита, мм; t - время, с; n - ряд целых чисел 1,2,3,4,5...; ![]() - безразмерный параметр или критерий гомохронности Фурье;
- безразмерный параметр или критерий гомохронности Фурье;
Значения параметров Bt для различных F табулированы.
Прямолинейный характер зависимости Bt от t для всех исследованных систем указывает на то, что приведенное выше уравнение хорошо описывает экспериментальные данные.
Коэффициенты диффузии после определения значения Bt для определенного F рассчитывались по уравнению:
![]() .
.
Энергия активации суммарного диффузионного процесса определялась из зависимости ![]() путем графического решения уравнения
путем графического решения уравнения
![]() ,
,
которое является уравнением прямой линии, с применением метода наименьших квадратов.
На рис. 3 представлены зависимости скорости сорбции ионов меди от температуры.
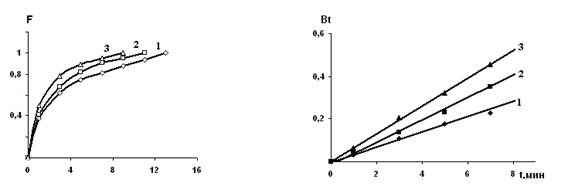
Рис. 3. Кинетические кривые и зависимость Bt от t сорбции ионов меди из 0,2М раствора ![]() катионитом КБ-4Пх2 в
катионитом КБ-4Пх2 в ![]() -форме
-форме
Температура 0С: 25(1), 45(2), 60(3).
Повышение температуры увеличивает скорость сорбции ионов. На основании кинетических данных вычислены коэффициенты диффузии при различных температурах. Коэффициенты диффузии обобщены в таблицу 1.
Величина энергии активации определяется высотой потенциального барьера, преодолеваемого диффундирующим ионом в фазе ионита. Она зависит от следующих факторов:
- энергии взаимодействия диффундирующих ионов с фиксированными группами ионита;
- работы образования пустот в диффузионной среде, которая определяется подвижностью молекул воды в обменнике, то есть энергией взаимодействия воды с ионами в ионите;
- величины активированного скачка, определяемого расстоянием между фиксированными группами.
Таблица 1. Коэффициенты диффузии при различных температурах
|
Сорбируемый элемент |
Форма |
Значение |
кДж/моль |
||
|
25 |
45 |
60 |
|||
|
Иттрий |
H+ |
3.45 |
4.86 |
5.71 |
12 |
|
NH4+ |
2.61 |
3.36 |
4.5 |
16.63 |
|
|
Барий |
H+ |
2.44 |
2.95 |
3.77 |
10.04 |
|
NH4+ |
1.997 |
2.69 |
4.09 |
16.5 |
|
|
медь |
H+ |
5.61 |
6.78 |
7.8 |
7.7 |
|
NH4+ |
3.34 |
4.11 |
6.11 |
14.52 |
|
Большие ионы при диффузии в глубь зерна частично раздвигают подвижные звенья набухшего катионита и забирают значительное количество воды находящиеся в катионите. При этом возрастает работа образования пустот в диффузионной среде. Все эти факторы увеличивают энергию активации и тем самым уменьшают скорость ионного обмена.
На скорость диффузии ионов металла в катионите оказывают влияние такие факторы, как радиус иона, его заряд и подвижность. Если ионы отличаются незначительно, то скорость их перемещения в фазе катионита и скорость сорбции практически одинаковы. С увеличением кристаллографических радиусов значения коэффициентов диффузии катионов уменьшаются [2].
Приведенные данные таблицы показывают, что скорость диффузии зависят от формы ионита и величин кристаллографических радиусов [4], то исследованные катионы по значению ![]() должны располагаться в ряд:
должны располагаться в ряд:
![]()
Чем меньше радиус иона, тем меньше энергия активации, тем больше скорость сорбции ионов.
При диффузии вглубь зерна большое значение имеет размер иона в водном растворе, из которого происходит сорбция. Зависимость скорости от величины гидратированного радиуса можно объяснить двумя причинами:
- при входе иона в поры катионита снимается вся гидратационная вода без больших затрат энергии[6];
- согласно теории гидратации [8], по которой ближняя гидратация в разбавленных растворах сводится к более или менее сильному взаимодействию иона с ближайшими молекулами воды, число которых в разбавленных растворах определяется структурой воды. Число гидратации в водных растворах примерно одинаково.
Если числа гидратации в водных растворах примерно одинаковы для всех ионов, то на скорость сорбции гидратная вода влиять на должна, поэтому скорость сорбции зависит от размеров кристаллохимических радиусов ионов.
Полученные результаты по кинетике ионного обмена сорбции двух- и трехзарядных катионов на карбоксильном катионите КБ-4Пх2 согласуются с данными по сорбции.
Высокие кинетические характеристики для исследованных катионитов указывают на перспективность их использования в технологических процессах извлечения, концентрирования ионов металлов, а так же в технологии получения сложных оксидов.
Выводы
- Исследована кинетика обмена ионов меди, бария и иттрия на катионите КБ-4Пх2 в азотнокислых растворах. Показано влияние размера зерна ионита, концентрации внешнего раствора по металлу, скорости перемешивания, химического состава раствора, температуры на скорость процесса сорбции.
- Установлено, что скорость определяющей стадией процесса сорбции катионов всех исследованных элементов является внутренняя диффузия. С использованием уравнения, описывающего внутридиффузионную кинетику, рассчитаны значения коэффициентов взаимодиффузии. Из температурных зависимостей определены значения кажущихся энергий активации диффузионного процесса.
- На основании количественных характеристик рассмотрен механизм и химизм ионного обмена, и его изменение в соответствии с химическим составом исходных растворов. Показано, что изменение скорости процесса связано с сорбируемостью металла, изменением ионного состояния раствора.
- Установлено, что скорость процесса, значения коэффициентов диффузии и энергии активации изменяются в соответствии со свойствами изученных соединений исследованных элементов и поведения их ионов при сорбции.
СПИСОК ЛИТЕРАТУРЫ:
- Бойд И., Адамсон А., Майерс Л.В. Хроматографический метод разделения ионов. - М.: ИЛ, 1969.- 333 с.
- Елькин Т.Э., Пасечник В.А., Самсонов Т.В. Термодинамика ионного обмена. - Минск, 1968.- с.111-135.
- Кокотов Ю.А., Пасечник В.А. Равновесие и кинетика ионного обмена. - Л.: Химия, 1960.- 336с.
- Лурье Ю.Ю. Справочник по аналитической химии, - М.:Химия, 1979. - 480 с.
- Полянский Н.Г., Горбунов Г.В., Полянская Н.Л. Методы исследования ионитов. - М., Химия, 1976.-286 с.
- Пришибл Р. Комплексоны в химическом анализе. - М.: ИЛ, 1960.
- Салдадзе К.М., Копылова-Валова В.Д. Комплексообразующие иониты. - М.: Химия, 1980. - 336 с.
- Цундель Г. Гидратация и межмолекулярное взаимодействие. - М.: Мир, 1972. - 404 с.
Библиографическая ссылка
Пимнева Л.А., Нестерова Е.Л. ИССЛЕДОВАНИЕ КИНЕТИКИ СОРБЦИИ И МЕХАНИЗМА ВЗАИМОДЕЙСТВИЯ ИНОВ МЕДИ, БАРИЯ И ИТТРИЯ В ФАЗЕ КАРБОКСИЛЬНОГО КАТИОНИТА КБ-4Пх2 // Фундаментальные исследования. 2008. № 4. С. 24-28;URL: https://fundamental-research.ru/en/article/view?id=2835 (дата обращения: 23.04.2026).



