Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
FORECASTING OF RISK OF DEVELOPMENT OF THE UNCONTROLLABLE CURRENT OF THE BRONCHIAL ASTHMA AT CHILDREN
Бронхиальная астма (БА) - это мультифакторное заболевание, формируемое совокупностью генетических и средовых факторов [6]. Большое значение в качестве фактора, предрасполагающего к развитию БА, имеет неблагоприятная наследственность по атопическим заболеваниям. При этом во всех существующих моделях прогнозирования фактор наследственной отягощенности имеет качественную характеристику, не позволяющую объективно оценить вклад наследственности в прогнозирование развития атопического заболевания у ребенка. Поэтому поиск критериев количественной оценки влияния наследственной предрасположенности позволит модернизировать и дополнить модели прогнозирования, повысить точность и достоверность прогноза. Наиболее информативными для выявления факторов риска развития неконтролируемого течения БА являются популяционные и семейные исследования, которые наряду с молекулярно-генетическим анализом получили широкое распространение в последнее десятилетие. Нами была предложена методика оценки генотипических значений параметров дыхательной функции ребенка на основании фенотипических показателей его родителей. Данная модель прогнозирования имеет преимущества перед существующими методами оценки наследственной предрасположенности[6], поскольку позволяет количественно оценить генотипический риск развития неконтролируемого течения БА.
Целью исследования явилось формирование системы прогнозирования риска развития неконтролируемого течения БА, направленное на повышение точности прогноза и оптимизацию противовоспалительной терапии за счет привлечения данных о генетической детерминации показателей функции внешнего дыхания у детей.
Материалы и методы исследования
В рамках популяционно-генетического исследования нами были обследованы 147 детей в возрасте от 8 до 15 лет с установленным диагнозом БА, а также 294 их кровных родственника 1-й степени родства. Средний возраст больных составлял 12,9 ± 3,1 лет. В группе обследованных преобладали мальчики - 96 человек (65,3 %), девочек было - 51 (34,7 %).
Комплекс обследований включал в себя опрос и изучение данных медицинской документации, анализ антропометрических данных, а также пиковой скорости выдоха (ПСВ) утром, ПСВ вечером и вариабельности ПСВ. Анализировались такие факторы риска, как наличие сопутствующих аллергических заболеваний (аллергический ринит, атопический дерматит, крапивница, пищевая и лекарственная аллергия), частота ОРИ, отягощенная по атопии наследственность по материнской и отцовской линии, наличие животных в доме, курение и экологическое неблагополучие жилища.
Статистическая обработка проводилась с помощью набора прикладных программ «MicrosoftOffice 2000Pro» forWindows OSR 2 на ЭВМ PC Intel Pentium-166 (MicrosoftOffice 97 Professional, 1997). Также для статистического анализа применялась компьютерная программа «STATISTICA 6.0». Анализ включал в себя определение средних арифметических величин, коэффициентов корреляции. В исследовании был использован однофакторный и множественный линейный регрессионный анализ, а также логистический регрессионный анализ [7]. Достоверность различий между группами по среднеарифметическим величинам, а также достоверность коэффициента корреляции определялась по критерию Стьюдента - t. Достоверным считался результат при t > 2, при котором р < 0,05. Достоверность коэффициента регрессии определялась по критерию F. Достоверным считался результат при р < 0,05 [3,4]. Определение генотипических значений признаков осуществлялось по определённому алгоритму. Сначала определялся коэффициент наследуемости (h2) корреляционным методом путём удвоения коэффициента корреляции по изучаемому признаку в паре родитель-потомок [1]:
h2 = 2·rр-n,
где r р-n - коэффициент корреляции в группе родитель - потомок.
Для большинства изученных в работе признаков h2 были нами ранее рассчитаны (табл. 1).
Таблица 1
Коэффициенты наследуемости для показателей, оказывающих влияние на течение бронхиальной астмы
|
Показатель |
h2 |
|
ПСВ утром |
0,37 |
|
ПСВ вечером |
0,61 |
|
Вариабельность ПСВ |
0,55 |
|
ИН 1 |
0,22 |
|
ИН2/ИН1 |
0,18 |
|
ИМТ |
0,78 |
|
Площадь поверхности тела |
0,36 |
|
Окружность грудной клетки |
0,61 |
Расчёт генотипических значений признаков проводился с помощью математических моделей прогнозирования. Эти модели позволяют рассчитать генотипические уровни факторов риска пробанда по данным фенотипических уровней факторов риска его кровных родственников [2]. В основу моделей положены уравнения регрессии генотипического отклонения пробанда на фенотипические отклонения его родственников и собственное фенотипическое отклонение [1]. Фенотипическое отклонение от среднепопуляционной величины признака (М) у обследованного (О) определяется по формуле:
ХО = ФО - М,
где ХО - фенотипическое отклонение; ФО - фенотипическая величина признака у обследованного О;
М - среднепопуляционная величина признака.
Генотипическое отклонение от среднепопуляционной величины признака (М) у обследованного (О) определяется по формуле:
Х1 = ГО - М, (А)
где Х1 - генотипическое отклонение; ГО - генотипическая величина признака у обследованного О; М - среднепопуляционная величина признака.
Таким образом определить ГО можно, преобразовав формулу (А):
ГО = Х1 + М.
Известно 59 комбинаций расчёта Х1, охватывающих большинство вариантов семейного генеалогического анализа. Данные комбинации оценок являются классическими и доказали свою биологическую значимость в селекционных исследованиях, методы их расчёта, а также данные об эффективности различных комбинаций освещены в научной литературе [1, 2].
В исследовании нами использована комбинация расчёта Х1 на основании собственных данных, данных отца и матери (Р + О + М):
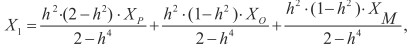
где h2 - коэффициент наследуемости изучаемого признака, ХР, ХО и ХМ - фенотипические отклонения признака от среднепопуляционной величины у пробанда, его отца и матери.
Нами оценивались генотипические значения таких параметров, как ПСВ утром и вечером, а также вариабельность ПСВ.
Для построения моделей прогнозирования использован двухфакторный анализ с построением уравнений регрессии.
Результаты исследования и их обсуждение
При анализе факторов риска было отмечено, что сопутствующие аллергические заболевания отмечались у 101 человека, {атопический дерматит - у 41 человека (27,9 %), аллергический ринит - 101(68,7 %), крапивница - 18 (12,2 %), пищевая аллергия - 42 (28,6), лекарственная аллергия - 16 (10,9 %)}. Наличие отягощенного атопического анамнеза наблюдалось у 111 детей, (75,5 %). Такой фактор риска, как табакокурение присутствует в 56 (38,1 %) семьях.
При анализе данных пикфлоуметрии было установлено, что ПСВ утром составила в среднем 92,7 ± 3,1 %, ПСВ вечером - 91,3 ± 5,1 %, а вариабельность ПСВ - 8,18 ± 3,5 %.
В ходе популяционно-генетического исследования было выявлено 103 ребенка с неконтролируемым течением бронхиальной астмы и 47 детей с контролируемым. С целью оценки степени влияния генотипической составляющей факторов риска на течение бронхиальной астмы применялся логистический регрессионный анализ. По данным Ребровой О.Ю. [4], логит-преобразование позволяет вместо значений признака (Р), определённых на интервале [0; 1] перейти к интервалу [-∞; +∞]. Вследствие этого возрастает чувствительность данной функции к изменению прогностического признака.
В ходе анализа были построены уравнения логистической регрессии, с помощью которых представляется возможным определить логит-преобразование признака (вероятности неконтролируемого течения бронхиальной астмы):
-ln (P) = ln [P/(1 - P)],
где Р - признак.
При анализе влияния фактора риска на риск развития неконтролируемого течения заболевания была выявлена статистическая достоверность (р < 0,001) в отношении Гп ПСВ утром, Гп ПСВ вечером и Гп вариабельности ПСВ (табл. 2).
Таблица 2
Коэффициенты корреляции генотипических показателей, используемых для прогнозирования течения бронхиальной астмы
|
Показатели, % |
R |
Р |
|
Гп ПСВ утром |
0,44 |
< 0,001 |
|
Гп ПСВ вечером |
0,31 |
< 0,001 |
|
Гп вариабельности ПСВ |
-0,60 |
< 0,001 |
Для полученных показателей были разработаны уравнения логистической регрессии:
Вероятность неконтролируемого течения
БА = exp(36,12 - 0,38x)/[1 + exp(36,12 - 0,38x)],
где х - Гп ПСВ утром, (р < 0,00001).
Вероятность неконтролируемого течения
БА = exp(13,88 - 0,14x)/[1 + exp(13,88 - 0,14x)],
где х - Гп ПСВ вечером, (р < 0,00001).
Вероятность неконтролируемого течения
БА = exp(3,17 - 0,57х)/[1 + exp(3,17 - 0,57x)],
где х - Гп вариабельности ПСВ, (р < 0,00001)
Уравнения логистической регрессии дают возможность количественно определять возможный риск развития неконтролируемого течения бронхиальной астмы при известной величине фактора риска, который в нашем случае колеблется от 0 до 100 %.
При проведении корреляционного анализа также была выявлена достоверная зависимость между течением бронхиальной астмы и такими показателями, как ПСВ ребенка вечером, утром и вариабельностью ПСВ (табл. 3).
Таблица 3
Коэффициенты корреляции фенотипических показателей, используемых для прогнозирования течения бронхиальной астмы
|
Показатели |
R |
Р |
|
ПСВ ребенка утром, % |
0,46 |
< 0,001 |
|
ПСВ ребенка вечером, % |
0,32 |
< 0,001 |
|
Вариабельность ПСВ, % |
-0,57 |
< 0,001 |
|
ИН1, ед. |
-0,02 |
> 0,05 |
|
ИН2/ИН1 , ед. |
0,13 |
> 0,05 |
Так, между значениями утренней ПСВ ребенка и контролируемым течением заболевания выявлена прямая корреляционная связь (r = 0,46, р < 0,001). Такой же силы и направленности существует взаимосвязь между вечерней ПСВ и течением болезни (r = 0,32, р < 0,001). Обратная корреляционная зависимость подтверждена для значений вариабельности ПСВ (r = -0,57, р < 0,001). Полученные результаты подтверждают важную роль ежедневного мониторинга ПСВ как инструмента оценки стабильности состояния пациента с бронхиальной астмой.
Учитывая известный факт о том, что у многих пациентов обострение заболевания чаще отмечается в ночное время, нами была проверена возможность привлечения в качестве фактора риска одних из наиболее значимых показателей оценки вегетативного статуса и вегетативной реактивности - индекса напряжения миокарда(ИН1 и ИН2/ИН1). Однако полученные результаты не выявили достоверной корреляционной зависимости между этими показателями и течением заболевания (см. табл. 3). Таким образом, из полученных результатов следует, что использовать эти показатели в качестве оценки возможного риска неконтролируемого течения заболевания нецелесообразно.
Для показателей (утренняя и вечерняя ПСВ, вариабельность ПСВ) с достоверными значениями корреляционной зависимости с течением бронхиальной астмы были построены уравнения логистической регрессии:
Вероятность неконтролируемого течения
БА = exp(-16,04 + 0,18x)/(1 + exp(-16,04+0,18x)),
где х - ПСВ ребенка утром, (р < 0,0001).
Вероятность неконтролируемого течения
БА = exp(-9,25 + 0,09x)/(1 + exp(-9,25 + 0,09x)),
где х - ПСВ ребенка вечером, (р < 0,0001).
Вероятность неконтролируемого течения
БА = exp(1,73 - 30,48x)/(1 + exp(1,73 - 30,48 х)),
где х - вариабельность ПСВ ребенка, (р < 0,0001)
Формулы расчета величин риска позволяют определить риск возможного развития неконтролируемого течения бронхиальной астмы, выраженный в процентах, при помощи как генотипических факторов риска, так и фенотипических данных.
Заключение. Популяционно-генетический и генеалогический анализ позволили нам выработать критерии количественной оценки наследственной отягощенности по риску развития неконтролируемого течения бронхиальной астмы, которые выражаются генотипическими значениями ПСВ утром, ПСВ вечером, вариабельности ПСВ. Эти критерии в профилактической пульмонологии (аллергологии) позволят усовершенствовать программы прогнозирования неконтролируемого течения бронхиальной астмы. Соотношение наследственного и средового фактора является основным в разработке новой стратегии профилактики и лечения БА.
Разработанная методика оценки риска развития неконтролируемого течения бронхиальной астмы может быть использована в качестве дополнения к существующей системе прогнозирования и направлена на оптимизацию её функционирования.
Список литературы
- Лепер П.Р., Никоро З.С. Генетико-математические основы оценки племенных качеств животных. - Новосибирск: Наука, 1966. - 140 с.
- Медико-генетическое прогнозирование в кардиологии / Н.В. Михайлов, Д.В. Сафонов, С.В. Шлык, В.П. Терентьев. - Ростов-на-Дону: РостГМУ, 1996. - 67 с.
- Петри А., Сэбин К. Наглядная статистика в медицине / пер. с англ. В.П. Леонова. - М.: ГЭОТАР-МЕД, 2003. - 144 с.
- Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA. - М.: Медиа Сфера, 2003. - 312 с.
- Терентьев В.П., Батюшин М.М., Михайлов Н.В. Медико-генетическое прогнозирование и первичная профилактика сердечно-сосудистых заболеваний. - Ростов-на/Д: РГМУ, 1999. - 29 с.
- Генетика бронхиальной астмы / М.Б. Фрейдин, Л.М. Огородова, А.Н. Цой, Н.Г. Бердникова. - М.: Атмосфера, 2010. - 78 с.
- Юнкеров В.И., Григорьев С.Г. Математико-статистическая обработка данных медицинских исследований. - СПб.: ВМедА., 2002. - 266 с.
Рецензенты:
Соколов О.Ю., д.м.н, доцент кафедры фармакологии и клинической фармакологии ГОУ ВПО «Ростовский государственный медицинский университет», г. Ростов-на-Дону;
Тараканов А.В., д.м.н., профессор, заведующий кафедрой скорой и неотложной помощи ФПК и ППС ГОУ ВПО «Ростовский государственный медицинский университет» Росздрава, г. Ростов-на-Дону.
Библиографическая ссылка
Сависько А.А., Батюшин М.М., Лебеденко А.А., Семерник О.Е. ПРОГНОЗИРОВАНИЕ РИСКА РАЗВИТИЯ НЕКОНТРОЛИРУЕМОГО ТЕЧЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ У ДЕТЕЙ // Фундаментальные исследования. 2011. № 6. С. 154-157;URL: https://fundamental-research.ru/en/article/view?id=21353 (дата обращения: 17.05.2026).



