Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
KINETICS OF NANODISPERSED TIN OXIDES ALTERNATING CURRENT ELECTROCHEMICAL SYNTHESIS PROCESS
Введение. Исследования в области синтеза дисперсных оксидов олова направлены в основном на изучение методов осаждения [10], гидротермальной обработки [9] и механохимического синтеза [7]. Имеются сведения о формировании и исследовании структуры и свойств пленок оксидов олова [2]. Вместе с тем актуальным является получение нанодисперсных порошков оксидов олова для создания высокочувствительных датчиков и селективных сорбентов [3].
Ранее нами была показана возможность электрохимического синтеза с помощью переменного тока промышленной частоты ряда оксидов металлов [5]. Установлено, что наибольшее влияние на скорость процесса образования фазовых оксидов металлов оказывают следующие факторы: состав и концентрация электролита, температура электролиза и плотность переменного тока.
Целью настоящей работы является исследование кинетики электрохимического синтеза на переменном токе нанодисперсных оксидов олова.
Экспериментальная часть
Исследования кинетики электрохимического синтеза оксидов олова с использованием переменного тока промышленной частоты проводились согласно методике, изложенной в работе [6]. Методика, основанная на хроматографическом определении количества водорода, выделяющегося в эквивалентном соотношении окисленному металлу, апробирована на объектах с различными химическими свойствами и имеет более высокую точность определения скорости окисления металлов (q), чем другие методы. В работе в качестве электролитов были использованы соли, имеющие различный катионный и анионный состав (NaCl, NH4Cl, CH3COONa). Электроды изготавливались из металлического олова марки ХЧ.
Результаты и их обсуждение
Результаты экспериментов представлены в виде кинетических кривых, описывающих ход процесса при заданных параметрах электролиза. На рис. 1 в качестве примера приведена зависимость q = f(t) для процесса электрохимического окисления олова, полученная в растворе хлорида натрия с концентрацией 3 мас. % при 80 °С и плотности тока 1,0 А/см2.
Резкий рост количества окисленного олова в начальный момент времени связан с тем, что поверхность электродов свободна от загрязнений (продуктов коррозии) и быстро окисляется. Последующее уменьшение скорости окисления обусловлено, по-видимому, образованием барьерного оксидного слоя на поверхности электродов [1, 8]. В дальнейшем, в соответствии с двухслойной теорией, начинается рост гидроксидной пленки на покрытой оксидом поверхности металла, и скорость процесса возрастает. В стационарном режиме скорость процесса меньше зафиксированной на всплеске. Это связано с соотношением скоростей образования барьерного оксидного слоя и его растворения с последующей адсорбцией, кристаллизацией и растворением гидроксидных форм. При этом состав электролита не влияет на вид кинетической кривой. Время релаксации до достижения стационарного режима для процессов окисления олова в различных электролитах колеблется от 2-х до 3-х часов. Подобные зависимости описывают процессы, протекающие при различных значениях плотности тока и температуры во всех исследуемых растворах выбранных электролитов. Несмотря на то, что вид кривых q = f(t) сохраняется, значения интегральной скорости электрохимического окисления олова в конкретных условиях существенно отличаются. По кинетическим кривым рассчитывалась интегральная скорость окисления олова при различных параметрах электролиза. Зависимости, полученные в растворах электролитов различной концентрации при температуре 100 °С и плотности тока 2,0 А/см2, представлены на рис. 2.
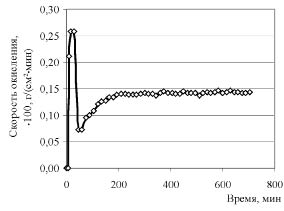
Рис. 1. Кинетическая кривая окисления олова при электролизе на переменном токе
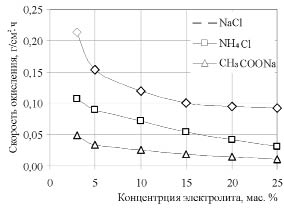
Рис. 2. Зависимость скорости окисления олова от концентрации электролита
Из рис. 2 видно, что в целом с ростом концентрации в интервале 3-25 мас. % скорость окисления уменьшается. Максимальная скорость окисления олова наблюдается в растворах хлорида натрия. Она примерно в 2 раза выше, чем в растворах хлорида аммония и более чем в 4 раза выше, чем при использовании растворов ацетата натрия, т.е. активность слабых электролитов в данном процессе (CH3COONa) существенно ниже. Следовательно, для электрохимического синтеза оксидов олова в качестве электролита целесообразно использовать раствор хлорида натрия.
Влияние температуры электролиза и плотности переменного тока на скорость процесса изучалось в растворе хлорида натрия различной концентрации. Полученные зависимости приведены на рис. 3 и 4. Эксперименты, проведенные при плотности тока 1,0 А/см2, показали, что с ростом температуры скорость процесса увеличивается практически линейно (см. рис. 3), и наиболее высокий градиент достигается при концентрации хлорида натрия 3 мас. %. В интервале 40-100 °С скорость возрастает более, чем в 7 раз.
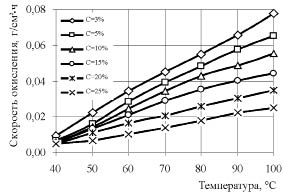
Рис. 3. Зависимость скорости окисления олова от температуры электролиза
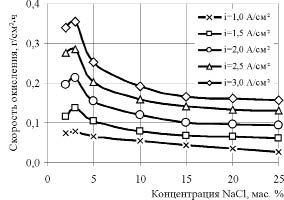
Рис. 4. Зависимость скорости окисления олова от концентрации хлорида натрия
при различной плотности тока
Вместе с тем наибольшее влияние на скорость процесса оказывает, как это отмечалось ранее для других металлов [5], плотность переменного тока (см. рис. 4). Зависимости иллюстрируют увеличение скорости окисления олова с ростом плотности тока во всем интервале концентраций NaCl. Характерный максимум скорости при концентрации NaCl, равной 3 мас. %, сохраняет свое положение при всех значениях плотности тока.
Подобного рода зависимости можно объяснить конкурирующим влиянием при адсорбции на поверхности электрода ионов Cl-, по сравнению с кислородсодержащими ионами, такими как О2- , ОН- . Вид полученных зависимостей обусловлен увеличением концентрации гидроксильных групп, способных участвовать во взаимодействии с ионами металлов в плотной части ДЭС [8] в анодный полупериод. Это приводит либо к образованию ОНадс, либо к возникновению ионов О2- , либо к пересыщению растворов гидратированными ионами металлов [4]. Во всех рассмотренных авторами случаях скорость процесса разрушения металла и образования оксидной фазы возрастает.
Полученные результаты не укладываются в рамки представлений о возможности или невозможности разряда собственных ионов олова в катодный полупериод. Барьерный слой в катодный полупериод не претерпевает существенных изменений и функционирует в режиме псевдоравновесия. Вместе с тем разряд ионов водорода и его выделение способствуют разрыхлению пленки. Кардинальные превращения при смене полярности электродов происходят в оксидных и адсорбционных слоях - в условиях, далеких от состояния равновесия (высокая плотность тока) формируются более рыхлые и дефектные слои, обладающие меньшим сопротивлением диффузии. Как следствие, скорость процесса возрастает.
Исследования показали, что процесс в целом контролируется диффузией (вычисленные значения кажущейся энергии активации варьируют в интервале 17-20 кДж/моль), скорость которой зависит в основном от состояния оксидной пленки (барьера) и пористой структуры фазового оксидного слоя. Адсорбционный слой в меньшей мере оказывает влияние на скорость диффузии.
Заключение
Процесс окисления олова при электролизе с использованием переменного тока промышленной частоты наиболее интенсивно протекает в растворе NaCl с концентрацией 3 мас. %. Скорость разрушения зависит от химической природы образующихся на поверхности электрода оксидов и растет с увеличением температуры.
Плотность переменного тока является технологическим параметром, интенсифицирующим процесс электролиза, и её увеличение приводит к возрастанию скорости разрушения при всех исследуемых температурных режимах.
Список литературы
- Алексеев Ю.В., Колотыркин Я.М. Учет влияния структуры двойного электрического слоя (ДЭС) на растворение (коррозию) пассивного металла в рамках самосогласованной кинетико-электростатической модели. Влияние адсорбционного заряда и состава электролита // Электрохимия. ‒ 1998. ‒ Т. 34, № 3. ‒ С. 263-271.
- Структура и свойства пленок диоксида олова / В.М. Анищик, Л.И. Конюшко, В.А. Ярмолович, Д.А. Горбачевский, Т.Г. Герасимова // Неорганические материалы. - 1995. ‒ Т. 31, № 3. ‒ С. 337-341.
- Гаськов А.М., Румянцева Н.М. Выбор материалов для твердотельных газовых сенсоров // Неорганические материалы. - 2000. ‒ Т. 36, № 3 ‒ С. 369-378.
- Влияние скорости анодного окисления кадмиевого электрода на приэлектродную концентрацию гидроксокомплексов кадмия в растворах KOH различных концентраций / Т.Г. Дмитриенко, Е.А. Хомская, Н.Ф. И.А. Бурданова, Казаринов // Электрохимия. ‒ 1998. ‒ Т. 34, № 5. - С. 473-479.
- Получение геля гидроксида алюминия электролизом на переменном токе / В.В. Коробочкин, В.И. Косинцев, Л.Д. Быстрицкий, Е.П. Ковалевский // Неорганические материалы. ‒ 2002. ‒ Т. 38, № 9. ‒ С. 1087-1090.
- Коробочкин В.В., Ханова Е.А. Определение количества окисленных титана, кадмия и меди при электролизе на переменном токе // Заводская лаборатория. Диагностика материалов. ‒ 2005. ‒ №6, Т.71. ‒ С. 20-23.
- Механохимический синтез наноразмерных порошков на основе диоксида олова / А.А. Магаева, О.Г. Терехова, В.И. Итин, Н.И. Радишевская, Е.П. Найден, Л.А. Егорова, И.И. Иванчук, А.Г. Першина // Журнал прикладной химии. ‒ 2009. ‒ Т. 82, Вып. 2. ‒ С. 220-223.
- Попов Ю.А., Сидоренко С.Н., Давыдов А.Д. Основы теории пассивности металлов. Механизм стабильного стационарного пассивирующего слоя, термодинамически неравновесного по своей природе // Электрохимия. ‒ 1997. ‒ Т. 33, № 11. ‒ С. 1269-1278.
- Нанокристаллические порошки SnO2, синтезированные гидротермальным методом, для сенсоров / Д.С. Торхов, А.А. Барухин, Б.Р. Чурагулов, М.Н. Румянцева, В.Д. Маскимов // Неорганические материалы. ‒ 2003. ‒ Т. 39, № 11. ‒ С. 1342-1346.
- Исследование кристаллизации SnO2, полученного золь-гель методом из солей олова разной степени окисления / Л.Ф. Чепик, Е.П. Трошина, Т.С. Мащенко, Д.П. Романов, А.И. Максимов, О.Ф. Луцкая // Журнал прикладной химии. ‒ 2001. ‒ Т. 74, Вып. 10. ‒ С. 1569-1572.
Рецензенты:
Сваровский А.Я., д.т.н., профессор, Северский технологический институт - филиал Федерального государственного бюджетного образовательного учреждения высшего профессионального образования «Национальный исследовательский ядерный университет МИФИ», Северск;
Буйновский А.С., д.т.н., профессор, Северский технологический институт - филиал Федерального государственного бюджетного образовательного учреждения высшего профессионального образования «Национальный исследовательский ядерный университет МИФИ», Северск;
Полещук О.Х., д.х.н., профессор, зав. кафедрой органической химии ГОУ ВПО «Томский государственный педагогический университет», Томск.
Библиографическая ссылка
Коробочкин В.В., Балмашнов М.А., Горлушко Д.А., Усольцева Н.В., Бочкарёва В.В. КИНЕТИКА ПРОЦЕССА ЭЛЕКТРОХИМИЧЕСКОГО СИНТЕЗА НАНОДИСПЕРСНЫХ ОКСИДОВ ОЛОВА НА ПЕРЕМЕННОМ ТОКЕ // Фундаментальные исследования. 2011. № 4. С. 89-93;URL: https://fundamental-research.ru/en/article/view?id=21236 (дата обращения: 04.05.2026).



