Хронический пиелонефрит (ХПл) является наиболее частой причиной терминальной хронической почечной недостаточности (ТХПН), прежде всего, в силу распространенности заболевания. Поэтому, хотя не пиелонефриту, а гломерулопатиям отводится фатальная роль в формировании ТХПН, вклад ХПл в статистику «почечной смерти» более велик. Нефросклероз, развивающйся на фоне ХПл, провоцируется прогредиентным воспалительным процессом в интерстиции почек, который в конечном итоге приводит к замещению паренхимы соединительной тканью.
Однако далеко не каждый случай заболевания ХПл завершается тотальным сморщиванием почек и ТХПН. Известно, что большинство аутопсий сопровождается находками пиелонефрита, протекавшего латентно. Такие варианты ХПл характеризуются ограниченными склеротическими изменениями. Очевидно, поэтому серьезных нарушений функций почек не происходит. Также не менее известны факты позднего обнаружения ТХПН по причине латентно протекавшего ХПл. По всей видимости, имеет место влияние различных факторов. Одни из них являются стабилизирующими в отношении почек. Другие, напротив, могут запускать неконтролируемое прогрессирование нефросклероза при латентном клиническом варианте ХПл. В этой связи актуальным является изучение механизмов прогрессирования латентного пиелонефрита [1-3].
Сложные взаимодействия, возникающие в ходе общего инфекционно-воспалительного процесса, сопровождаются изменениями клеточного метаболизма, цитохимической активности иммунной и опсоно-фагоцитарной систем [4], что может приводить к нарушению локального почечного иммунитета и запускать процессы дестабилизации во внутренних средах организма. Это имеет непосредственное отношение к почкам как органу, ответственному за гомеостаз. Поэтому представляют особый интерес структурно-функциональные изменения в различных биологических жидкостях, в частности в плазме крови. Морфологическое исследование жидких сред, как известно, позволяет оценить особенности архетипов структурной организации [5,6] и динамику процессов, вносящих вклад в дестабилизацию метаболизма.
Целью работы стало исследование морфотипов тезиограмм плазмы крови больных хроническим пиелонефритом.
Материалы и методы
В качестве объекта исследования использовали плазму крови 32 пациентов с хроническим пиелонефритом в возрасте от 20 до 25 лет, в том числе 12 мужчин и 20 женщин. Диагноз ХПл выставлялся на основании клинического исследования и дополнительных данных, полученных в ходе лабораторных тестов мочи и крови и при ультразвуковом обнаружении признаков деформации, уплотнения, расширения чашечно-лоханочного комплекса почек. Пациенты распределены в три группы. Первую составили молодые люди (n=5), страдающие пиелонефритом латентного течения в стадии неполной ремиссии: имели место незначительные дизурические явления, показатели СОЭ были нормальными, в моче не обнаруживались лейкоциты. Вторая группа обследованных (n=20) характеризовалась минимальной степенью активности пиелонефрита: показатель СОЭ не превышал нормы, в моче при общем анализе обнаруживалось от 2 до 6-8 лейкоцитов. Дизурических явлений не наблюдалось. В третью группу вошли 7 пациентов со средней степенью активности ХПл. У пациентов отмечались никтурия, поллакиурия. В отдельных порциях утренней мочи обнаруживались до 10-12 лейкоцитов и следы белка. Контрольную группу составили здоровые лица.
Тезиографическое исследование плазмы крови проводили по методу Шабалина В.Н. и Шатохиной С.Н. [6]. Статистический анализ полученных данных проводился с использованием пакета прикладных программ STATISTICA версия 7.0 с учетом вычислительных методов, рекомендуемых для биологии и медицины.
Результаты и обсуждение
Типичная тезиограмма плазмы крови здорового донора представлена на рис. 1.

Рис. 1. Тезиограмма плазмы крови здорового донора (контроль)
Тезиограммы плазмы крови здоровых доноров характеризовались наличием трех зон: краевой, промежуточной и центральной. Краевая зона является прозрачным кольцом органических веществ преимущественно белкового происхождения. Центральная зона представлена в виде пленки, содержащей липиды, минеральные вещества, и небольшое количество белков. Промежуточная зона представлена преимущественно белками и нормальными белковыми комплексами с минеральными веществами. Также наблюдались высокая густота растрескивания и большое количество конкреций в центральной зоне капли, при этом явно сохранена радиальная структура растрескивания. В краевой зоне отмечается наличие небольшого количества аморфных областей, а характер растрескивания приобретает аркадно-петельную структуру.
Типичная тезиограмма плазмы крови больного ХПл 1-й группы представлена на рис. 2.
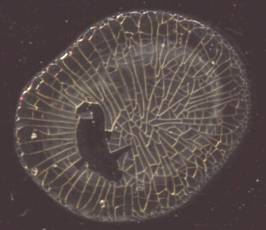
Рис. 2. Типичная тезиограмма плазмы крови больного с ХПл 1-й группы
В тезиограммах плазмы крови больных ХПл 1-й группы также выделялись три зоны. Центральная и промежуточная зоны характеризовались высокой густотой растрескивания, в краевой зоне густота растрескивания снижена, с преобладанием аркадно-листового типа. Характер растрескивания близок к радиальному, с нарушением симметрии в центральной зоне капли. Количество конкреций сильно снижено по сравнению с контролем, конкреции представлены только в краевой зоне
Типичная тезиограмма плазмы крови больного ХПл 2-й группы представлена на рис. 3.
В тезиограммах плазмы крови больных данной группы отмечалось сохранение радиальной структуры растрескивания, однако границы между зонами были нечеткими, промежуточной зоны практически не было. Густота растрескивания была снижена, характер растрескивания близок к радиальному. При сохранении радиальности растрескивания, отмечались нарушения в формировании системных структур фации. Отдельности были более крупными, чем в образцах контрольной группы и формировали «радиальные спицы», направленные от центра к периферии.
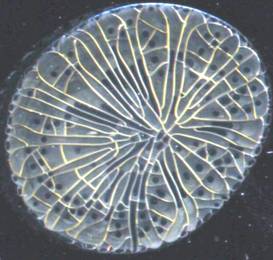
Рис. 3. Типичная тезиограмма плазмы крови больного ХПл 2-й группы
В центральной зоне конкреции были в основном неправильной формы, занимали большую часть отдельности, с нечетко выраженными краями. Такие изменения в формировании подсистемных структур свидетельствуют об уменьшении онкотической активности белков плазмы крови и нарушении их взаимодействия с минеральными веществами.
Данные признаки могут свидетельствовать об уменьшении содержания в плазме крови минеральных компонентов, что может объясняться усиленным связыванием натрия модифицированными белками и продуктами их окислительной модификации, а также молекулами средней массы.
Типичная тезиограмма плазмы крови больного ХПл 3-й группы представлена на рис. 4.

Рис. 4. Типичная тезиограмма плазмы крови больного ХПЛ 3-й группы
В данной группе тезиограммы отличались нарушением радиальности растрескивания, отсутствием четких границ между зонами, изменением количества и расположения конкреций. Отмечалось сглаживание промежуточной зоны, снижение густоты растрескивания и уменьшение количества конкреций в краевой зоне. Также наблюдалось преобладание аркадно-петельного характера растрескивания в периферической зоне с сохранением радиальной структуры фации.
Густота растрескивания в центральной зоне также была снижена, характер растрескивания близок к радиальному, но без сохранения долевой симметрии. Отмечалось большое количество отдельностей с затемнением в центре, но без формирования четких конкреций.
Таким образом, выявлены существенные различия в структуре и формах тезиограмм плазмы крови молодых больных латентным ХПл в зависимости от активности процесса и степени эндогенной интоксикации. Предположительно, найдены отличительные морфотипы тезиограмм, характерные для различных фаз воспалительного процесса в почках, что отражает различную степень дисбаланса внутренних сред организма. Очевидно, дальнейшее изучение особенностей структурно-фунциональных изменений в плазме крови и, по-видимому, в моче больных позволит установить факторы, способствующие активизации и прогредиентному течению латентного ХПл.
СПИСОК ЛИТЕРАТУРЫ
1. Павлов С.Б. // Клиническая лабораторная диагностика.- 1997.- №11.-С. 21-24
2. Сейсембеков Т.З., Айтпаев Б.К., Муравлева Л.Е., Молотов-Лучанский В.Б. // Центрально-Азиатский медицинский журнал. -1996. Том II, № 4. - С. 41-48
3. Милютина Н.П., Ананян А.А., Шугалей B.C. // Бюл. эксперим. биол.и мед. – 1990. - № 9. - С. 263 – 265
4. Flavahan N.A. // Circulation. 1992. - Vol. 85, № 5. - P. 1927-1938
5. Савченко Р.П., Гордюшина И.В. // Клиническая лабораторная диагностика.- 2002.- № 9.-С. 34-35.
6. Шабалин В.Н., Шатохина С.Н. //Клиническая лабораторная диагностика.- 2002.- №3.- С.25-29.
Библиографическая ссылка
Л.Е. Муравлева, В.Б. Молотов-Лучанский, Д.А. Клюев, Д.С. Кусаинова, Н.У. Танкибаева, Г.А.Омарова МОРФОТИПЫ ТЕЗИОГРАММ ПЛАЗМЫ КРОВИ БОЛЬНЫХ ХРОНИЧЕСКИМ ПИЕЛОНЕФРИТОМ // Фундаментальные исследования. 2009. № 10. С. 21-24;URL: https://fundamental-research.ru/en/article/view?id=2072 (дата обращения: 21.04.2026).



