Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THERMODYNAMIC CONSTANTS OF DISSOCIATION OF PROTONATED FOUR ACID BASES
Термодинамические константы диссоциации протонированного основания определяются следующими соотношениями [11,12]:
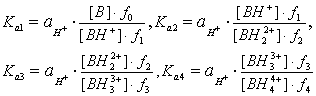 (1)
(1)
В уравнении (1) ![]() - активность ионов лиония, то есть сольватированного иона водорода, в последующем примем обозначение а(лиония), в любой точке потенциометрического титрования;
- активность ионов лиония, то есть сольватированного иона водорода, в последующем примем обозначение а(лиония), в любой точке потенциометрического титрования; ![]() ,
, ![]() - равновесные концентрации нейтрального и протонированного четырехкислотного основания в процессе титрования сильной кислотой;
- равновесные концентрации нейтрального и протонированного четырехкислотного основания в процессе титрования сильной кислотой; ![]() - коэффициенты активности нейтральной и протонированных форм полиоснования.
- коэффициенты активности нейтральной и протонированных форм полиоснования.
Как отмечалось ранее [10,12], известные методы оценок ионной силы при кислотно-основном равновесии [2,4,13,14] основаны на использовании концентрации первой ионизированной частицы, например, [ВH+] для двухкислотного основания. Было показано [3,9,10,11], что в расчетах констант диссоциации не следует пренебрегать равновесными концентрациями остальных ионов, так как их величины в различных точках титрования сопоставимы с концентрацией первого протонированного иона, а из данных табл. 2 и рис. 1 видно, что в процессе протонирования концентрации последующих ионов (например, даже ![]() ) превышают таковые иона [ВH+].
) превышают таковые иона [ВH+].
Наиболее приемлемым способом оценки ионной силы, определяемой с учетом равновесных концентраций всех заряженных частиц, является представление кривой титрования основания в логарифмических координатах [9,10,11,12]. При этом равновесные концентрации всех частиц ![]() ,
, ![]() , образующихся при титровании четырехкислотного основания сильной одноосновной хлорной кислотой, могут быть определены на диаграммах -lg а(лиония) - lgC. Оценка значений коэффициентов активности f0, f1, f2, f3 и f4 проводится по более оптимальному методу Дэвиса [13]:
, образующихся при титровании четырехкислотного основания сильной одноосновной хлорной кислотой, могут быть определены на диаграммах -lg а(лиония) - lgC. Оценка значений коэффициентов активности f0, f1, f2, f3 и f4 проводится по более оптимальному методу Дэвиса [13]:
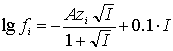 (2)
(2)
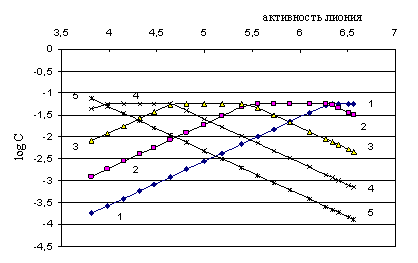
Рис. 1. Логарифмическая диаграмма процесса титрования 0,05652н. раствора 3,3´4,4´-тетрааминодифенилоксида 0.1295 н. раствором хлорной кислоты в среде ДМФ, дающая возможность определения концентраций равновесных частиц:
1-1: lg [B], 2-2: lg[BH+], 3-3: lg[BH22+], 4-4: lg[BH33+], 5-5: lg[BH44+]
Измерения ЭДС и потенциометрическое титрование в среде диметилформамида (ДМФ) осуществляли при 25.0 ± 0.20С на рН-метре-милливольтметре METROHM-632 (Швейцария). Растворитель очищен и обезвожен по известным методикам [5,6]. Содержание воды, определенное модифицированным методом К.Фишера [8], не превышало для ДМФ ±0.02 мас.%.
В табл. 1 приведены данные измерения ЭДС цепи (I) в среде ДМФ в зависимости от моляльной концентрации хлорной кислоты, а также результаты оценки степени диссоциации HClО4 и исходные величины для расчета стандартного потенциала цепи.
Таблица 1. Изменение ЭДС цепи (I) в зависимости от моляльной концентрации хлорной кислоты (m, моль HClO4/1000г ДМФ) и данные для определения Е0 цепи (I)
|
m |
E, B |
α (HClO4) |
-0.0581×lg (mα) |
(m×α)0.5 |
E´ |
|
0.1371 |
0.340 |
0.3694 |
1.2954 |
0.2250 |
0.4164 |
|
0.06855 |
0.330 |
0.5342 |
1.4363 |
0.1913 |
0.4147 |
|
0.03427 |
0.320 |
0.6559 |
1.6482 |
0.1499 |
0.4172 |
|
0.01713 |
0.309 |
0.7358 |
1.8995 |
0.1123 |
0.4211 |
|
0.008565 |
0.295 |
0.7719 |
2.1797 |
0.0813 |
0.4236 |
|
0.004282 |
0.275 |
0.7511 |
2.4927 |
0.0567 |
0.4221 |
Степень диссоциации хлорной кислоты может быть оценена по уравнению (3) [1,9,10,11,12].
![]() (3)
(3)
Величина ![]() , равная разности
, равная разности ![]() (
( 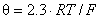 ), определена по программе «mnk» (метод наименьших квадратов) по зависимости
), определена по программе «mnk» (метод наименьших квадратов) по зависимости ![]() при lg m = 0. Получена величина
при lg m = 0. Получена величина ![]() = 0.3791 с коэффициентом регрессии r = 0.9895.
= 0.3791 с коэффициентом регрессии r = 0.9895.
Значение стандартного потенциала цепи (I) определено по авторской компьютерной программе «parab» по приближению функции ![]() при
при ![]() , где
, где ![]() .
.
![]() , r = 0.9090.
, r = 0.9090.
Таким образом, получена величина стандартного потенциала цепи (I) в среде ДМФ, равная Ео = 0.4272 В.
Стандартный потенциал цепи (I), наряду с равновесными концентрациями нейтральной молекулы основания и заряженных частиц ![]() ,
, ![]() , образующихся в процессе титрования основания, оцененных по табл. 2 и рис. 1, и их коэффициентами активностей
, образующихся в процессе титрования основания, оцененных по табл. 2 и рис. 1, и их коэффициентами активностей ![]() и f4 дают возможность определения термодинамических констант кислотности протонированных полиоснований в среде органических растворителей.
и f4 дают возможность определения термодинамических констант кислотности протонированных полиоснований в среде органических растворителей.
Оценка активности лионий-ионов в процессе титрования основания возможна по уравнению Нернста:
![]() .
.
Рассматриваемая методика, отличающаяся от известных применением логарифмических зависимостей при оценке ионной силы и коэффициентов активности ионов, как отмечалось в [12], была апробирована на примере 1,3-дифенилгуанидина (ДФГ) в среде ДМФА. В литературе [7] известна величина рКа (ДФГ/ДМФА) = 9.1. Нами было [11] получено значение рКа (ДФГ/ДМФА) = 9.15 ± 0.03, свидетельствующее о достаточной надежности и воспроизводимости предлагаемого метода.
В табл. 2 сведены все исходные данные для расчета констант диссоциации по уравнениям (1) и (2) при титровании 0.01413М (0.05652н.) раствора 3,3´4,4´-тетрааминодифенилоксида, широко применяемого в синтезе полибензимидазолов, 0.1295 н. раствором хлорной кислоты в среде ДМФ.
Таблица 2. Расчет констант диссоциации протонированного 3,3´4,4´-тетрааминодифенилоксида в среде ДМФ по ур.(1) и (2)
|
V, мл |
E, B |
-lg a (лиония) |
[B] |
[BH+] |
[BH22+] |
[BH33+] |
[BH44+] |
|
0.3 |
0.040 |
6.5593 |
0.05652 |
0.03183 |
0.00460 |
0.00071 |
0.00013 |
|
0.5 |
0.043 |
6.5085 |
0.05652 |
0.03578 |
0.00517 |
0.00080 |
0.00015 |
|
1.0 |
0.053 |
6.3390 |
0.05652 |
0.05287 |
0.00764 |
0.00118 |
0.00022 |
|
1.5 |
0.067 |
6.1017 |
0.03498 |
0.05652 |
0.01319 |
0.00204 |
0.00038 |
|
2.0 |
0.079 |
5.8983 |
0.02190 |
0.05652 |
0.02108 |
0.00326 |
0.00061 |
|
2.5 |
0.089 |
5.7288 |
0.01482 |
0.05652 |
0.03114 |
0.00482 |
0.00090 |
|
3.0 |
0.099 |
5.5593 |
0.01003 |
0.05652 |
0.04601 |
0.00713 |
0.00132 |
|
3.5 |
0.109 |
5.3898 |
0.00679 |
0.04699 |
0.05652 |
0.01053 |
0.00196 |
|
4.0 |
0.121 |
5.1864 |
0.00425 |
0.02942 |
0.05652 |
0.01681 |
0.00313 |
|
4.5 |
0.132 |
5.0000 |
0.00276 |
0.01915 |
0.05652 |
0.02583 |
0.00481 |
|
5.0 |
0.143 |
4.8135 |
0.00180 |
0.01246 |
0.05652 |
0.03968 |
0.00740 |
|
5.5 |
0.153 |
4.6440 |
0.00122 |
0.00844 |
0.05448 |
0.05652 |
0.01091 |
|
6.0 |
0.163 |
4.4745 |
0.00082 |
0.00571 |
0.03688 |
0.05652 |
0.01613 |
|
6.5 |
0.172 |
4.3220 |
0.00058 |
0.00402 |
0.02595 |
0.05652 |
0.02291 |
|
7.0 |
0.182 |
4.1525 |
0.00039 |
0.00272 |
0.01757 |
0.05652 |
0.03385 |
|
7.5 |
0.192 |
3.9830 |
0.00026 |
0.00184 |
0.01189 |
0.05652 |
0.05002 |
|
8.0 |
0.202 |
3.8135 |
0.00018 |
0.00124 |
0.00805 |
0.04322 |
0.07390 |
|
8.5 |
0.213 |
3.6271 |
0.00012 |
0.00081 |
0.00524 |
0.02814 |
0.11352 |
Продолжение табл. 2
|
V, мл |
f1 |
f2 |
f3 |
f4 |
рК1 |
рК2 |
рК3 |
pK4 |
|
0.3 |
0.5801 |
0.3342 |
0.1925 |
0.1109 |
6.073 |
- |
- |
- |
|
0.5 |
0.5644 |
0.3162 |
0.1771 |
0.0992 |
6.061 |
- |
- |
- |
|
0.8 |
0.5327 |
0.2811 |
0.1483 |
0.0782 |
6.036 |
- |
- |
- |
|
1.0 |
0.5114 |
0.2586 |
0.1308 |
0.0661 |
6.019 |
- |
- |
- |
|
1.2 |
0.4965 |
0.2434 |
0.1193 |
0.0585 |
6.006 |
- |
- |
- |
|
1.5 |
0.4682 |
0.2158 |
0.0995 |
0.0458 |
5.980 |
- |
- |
- |
|
2.0 |
0.4280 |
0.1794 |
0.0752 |
0.0315 |
- |
5.092 |
- |
- |
|
2.5 |
0.3905 |
0.1484 |
0.0563 |
0.0214 |
- |
5.049 |
- |
- |
|
3.0 |
0.3513 |
0.1189 |
0.0402 |
0.0136 |
- |
4.999 |
- |
- |
|
3.5 |
0.3271 |
0.1022 |
0.0319 |
0.0100 |
- |
4.964 |
- |
- |
|
4.0 |
0.3116 |
0.0921 |
0.0272 |
0.0080 |
- |
4.941 |
- |
- |
|
4.5 |
0.2905 |
0.0792 |
0.0216 |
0.0059 |
- |
- |
4.095 |
- |
|
5.0 |
0.2652 |
0.0648 |
0.0158 |
0.0038 |
- |
- |
4.048 |
- |
|
5.5 |
0.2434 |
0.0534 |
0.0117 |
0.0025 |
- |
- |
4.001 |
- |
|
6.0 |
0.2425 |
0.0529 |
0.0115 |
0.0025 |
- |
- |
3.999 |
- |
|
6.5 |
0.2370 |
0.0501 |
0.0106 |
0.0022 |
- |
- |
3.985 |
- |
|
7.0 |
0.2265 |
0.0451 |
0.0090 |
0.0018 |
- |
- |
- |
3.229 |
|
7.5 |
0.2131 |
0.0388 |
0.0071 |
0.0013 |
- |
- |
- |
3.191 |
|
8.0 |
0.2028 |
0.0342 |
0.0057 |
0.0010 |
- |
- |
- |
3.273 |
|
8.5 |
0.1893 |
0.0282 |
0.0042 |
0.0006 |
- |
- |
- |
3.405 |
Как видно из табл. 2 и рисунка, равновесные концентрации частиц, находящихся в титруемом растворе, вполне сопоставимы.
Поэтому подчеркнем, что в расчетах рКа все концентрации должны быть учтены. Протонированные четырехкислотные основания характеризуются близостью констант кислотности, подтверждаемой одним совместным скачком потенциала на кривой потенциометрического титрования, которую мы здесь не приводим.
Рассчитанные в соответствующих буферных областях величины термодинамических констант диссоциации протонированного 3,3´4,4´-тетрааминодифенил-оксида в среде ДМФ равны: рК1 = 6.03 ± 0.05, рК2 = 5.01 ± 0.08, рК3 = 4.03 ± 0.06, рК4 = 3.27 ± 0.12.
Разработанная методика определения термодинамических констант кислотности полиоснований в среде органических растворителей вполне приемлема при экспериментальном определении рКа любых четырехкислотных оснований при многостадийном протонировании (равно как и трехкислотных оснований [12]).
СПИСОК ЛИТЕРАТУРЫ:
- Александров В.В., Лебедь В.И., Шихова Т.М., Заславский Б.Г. // Электрохимия.-1968. -Т.4.- №6.- С.711.
- Альберт А., Сержент Е. Константы ионизации кислот и оснований.- М.-Л.: -Химия.- 1964.- 262 с.
- Анорганикум. -М.: Мир.-1984. -Т.2. -С.120.
- Бейтс Р. Определение рН. Теория и практика. -Л.: Химия.- 1972.- 400 с.
- Вайсбергер А., Проскауэр Э., Риддик Дж., Тупс Э. Органические растворители /Пер. с англ. М.: Издатинлит.- 1958.- 519 с.
- Гордон А., Форд Р. Спутник химика. -М.: Мир.-1976.- 541 с.
- Крешков А.П. Аналитическая химия неводных растворов. -М.: Химия.- 1982.-120 с.
- Танганов Б.Б. Химия и хим. технология. Деп. ОНИИТЭХим.1984. №976 хпД84).
- Танганов Б.Б. Химические методы анализа: Уч. пособ.-Улан-Удэ.- 2005.-550 с.
- Танганов Б.Б., Алексеева И.А. //ЖОХ.-2005.-Т.75.- Вып.11.-С.1775.
- Танганов Б.Б., Алексеева И.А. //ЖОХ.-2006.-Т.76.- Вып.11.-С. 1800.
- Танганов Б.Б., Ангапов В.Д., Багаева Т.В., Алексеева И.А. //Успехи современного естествознания.-2008.-№11.-С.12.
- Davies C.W. // J.Chem.Soc.-1938.- P.2093.
- Speakman J.C. //J.Chem.Soc.-1940.- P.855.
Библиографическая ссылка
Танганов Б.Б. ТЕРМОДИНАМИЧЕСКИЕ КОНСТАНТЫ ДИССОЦИАЦИИ ПРОТОНИРОВАННЫХ ЧЕТЫРЕХКИСЛОТНЫХ ОСНОВАНИЙ // Фундаментальные исследования. 2009. № 2. С. 15-19;URL: https://fundamental-research.ru/en/article/view?id=1795 (дата обращения: 01.05.2026).



