Актуальность ревматоидного артрита (РА) – для общественного здравоохранения обусловлена высокой смертностью больных, прежде всего, связанной кардиоваскулярной патологией [7]. Сочетание классических факторов риска (оксидативный стресс на фоне хронического воспаления, атерогенная дислипидемия, симпатикотония) c внутринозологическми факторами риска (серопозитивность по ревматоидному фактору) создает прочную платформу кардиоваскулярного континуума при РА [6; 8; 11; 12; 13]. Поражение сосудистого русла у больных РА происходит на всех его уровнях, включая конечное звено – регионарную микроциркуляцию и гемореологию [2; 3].
Перспективной с позиции понимания патогенеза кардиоваскулярных катастроф при РА видится концепция нейрогуморальных факторов риска, в которой главенствующую роль отводят абсолютному или относительному избытку катехоламинов у больных РА [9].
Таким образом, мониторирование вегетативной дисфункции и состояния конечного звена гемодинамики является актуальным с целью выделения групп риска по сосудистым осложнениям РА.
Перспективным в области исследования микроциркуляции видится метод лазерной допплеровской флуометрии (ЛДФ), основанный на оптическом сканировании ткани лазерным лучом и восприятии его отражения датчиком по законам эффекта Допплера. Полученый сигнал подвергается сложному компьютерному анализу частотного спектра света лазера, который отражается от движущихся в микроциркуляторном регионе эритроцитов. Поглощение излучения молекулами гемоглобина приводит к сканированию зондируемого слоя ткани от 0,5 до 2 мм. Амплитуда сигнала, отраженного от гемоглобина эритроцитов формируется от эритроцитов, движущихся с разными скоростями и в разном количественном соотношении представленных в микроциркуляторном русле. Поэтому при формировании ЛДФ-грамм применяется алгоритм усреднения, который позволяет получить средний допплеровский сдвиг частоты по всей совокупности эритроцитов, попадающих в зондируемую область. Соответственно аппарат ЛДФ показывает результат флоуметрии — сигнал, амплитуда которого пропорциональна скорости и количеству эритроцитов в единице объема ткани. [4;5;10].
Материалы и методы исследования
В исследование включены две группы пациентов: основная и контрольная. В основную группу вошли лица женского пола, находившиеся на стационарном лечении в городском ревматологическом центре г. Барнаула с диагнозом РА (n = 75), длительностью заболевания более одного года, серопозитивные по ревматиодному фактору и антителам к циклическому цитруллинированному пептиду, II–III степенью активности и II–III рентенологической стадией. Средний возраст их составил 57,04 ± 5,24 лет.
В группу контроля вошли лица женского пола, не имеющие по данным расспроса, анамнеза и объективного осмотра клиники суставных заболеваний (n = 85). Средний возраст в данной группе составил 53,21 ± 2,11 года. Обе группы статистически значимо не различались по возрасту (р > 0,05).
Критериями исключения из обеих групп стали возраст старше 65 лет, наличие злокачественных опухолей, декомпенсация сопутствующей сердечно-сосудистой, бронхолегочной и эндокринной патологии, беременность.
Микроциркуляторный статус оценивали при помощи ЛДФ на аппарате «ЛАКК-2» (НПП «Лазма», Россия) с соблюдением стандартных параметров исследования для методики лазерной допплеровской флоуметрии [4].
Исследования проводились в одно и то же время суток. Перед исследованием испытуемым было запрещено принимать пищу и напитки, изменяющие состояние микроциркуляции (кофеинсодержащие продукты в частности), курить. Микроциркуляцию оценивали в коже левого предплечья в зоне Захарьина-Геда для сердца, расположенной по срединной линии на 4 сантиметра выше основания шиловидных отростков локтевой и лучевой костей (индикаторная зона «общей» микроциркуляции).
Оценивались показатель микроциркуляции (ПМ), дающий представление о потоке эритроцитов в единицу времени через единицу объема ткани, флакс – среднеквадратическое отклонение амплитуды колебаний кровотока от ПМ (величина временной изменчивости микроциркуляции). Кроме того, при помощи расчетных методик был вычислен микрососудистый тонус (МСТ), индекс флаксомоций (ИФМ) и внутрисосудистое сопротивление (ВСС) микроциркуляторного русла, рассчитываемый с помощью вейвлет-анализа. Данные ЛДФ-метрии получены в виде перфузионных единиц (пф.ед.), поскольку при калибровке метода ЛДФ in vitro и in vivo возникают принципиальные трудности, и поток крови, определяемый как ПМ, не может быть выражен в абсолютных единицах, например, в мл/c/куб.мм, так как при окклюзии регистрируется броуновское движение остаточной крови, так называемый «биологический ноль», который учесть при калибровке не представляется возможным. При калибровке in vitro организуется, как правило, движение эритроцитов в трубках малого диаметра, что увеличивает силу допплеровского сдвига частоты в результате эффектов многократного рассеяния фотона на гемоглобине эритроцитов. Кроме того, из-за неустойчивости калибровочной системы: так как в трубках малого диаметра происходит агрегация эритроцитов, что приводит к изменению динамической ситуации. [4; 5].
Интерпритация полученных данных микроциркулятрных нарушений проводилась по В.И. Козлову, 2006, с разделением полученных данных на типы нарушений микроциркуляции (см. табл. 1) [4].
Исследования проводились при одинаковой температуре окружающей среды от 20 до 25 °С. В течение 15 минут перед исследованием, ЛДФ-метрии лица, включенные в исследование, находились в положении лежа на спине для психо-эмоциональной и физической релаксации. ЛДФ-граммы регистрировались в течение 10 минут в положении испытуемых лежа на спине.
Для вычисления коэфициента вегетативной регуляции кровообращения (КВР) подсчитывали число сердечных сокращений за минуту и делили полученное значение на параметры микроциркуляции по специальной формуле, позволяющей произвести градацию тонуса вегетативной регуляции кровообращения.
Интерпритация полученного КВР производилась по градациям: 24,50–35,77 – выраженная симпатикотония, 19,50–24,99 – легковыраженная ваготония, 16,20–1949 – эйтония, 12,50–16,19 – легковыраженная ваготония, 8,55–12,49 – выраженная ваготония [1].
Статистическая обработка данных проводилась с помощью пакета программ MS Excell 2003 и программы Statistica-6.0. Для проверки нормальности распределения количественных показателей использовали критерий Шапиро–Уилка. Так как выборка не соответствовала критериям нормального распределения, для статистического расчета применялся непараметрический метод Манна–Уитни: критический уровень значимости при проверке статистических гипотез принимался р < 0,05.
Работа локальным биоэтическим комитетом при Алтайском государственном медицинском университете признана соответствующей стандартам Хельсинской декларации.
Результаты исследования и их обсуждение
В группе больных РА нами получены статистически значимые по сравнению с группой контроля различия вегетативной регуляции деятельности системы кровообращения (табл. 2).
Исходя из полученных различий вегетативной регуляции деятельности системы кровообращения у больных РА можно сделать вывод о статистически значимом преобладании симпатикотонии разной степени выраженности: от легкой до выраженной (р < 0,05). Ваготония легкой степени выраженности, напротив, статистически значимо чаще встречалась у обследуемых группы контроля (р = 0,0045).
При исследовании микроциркуляции в группе больных РА ПМ составил 16,19 ± 3,16 пф.ед., что оказалось статистически значимо ниже по сравнению с группой контроля (р < 0,05). При проведении анализа флаксограммы в группе РА выявлено статистически значимое по сравнению с группой контроля снижение флакса до 2,05 ± 0,12 пф.ед. и МСТ до 0,85 ± 0,21 пф.ед. (р < 0,05). Кроме того, в группе больных РА выявлено статистически значимое повышение ИФМ до 5,18 ± 1,13 пф.ед. и ВСС до 4,05 ± 0,11 пф.ед. по сравнению с группой контроля при р < 0,05 (рисунок).
Таблица 1
Формы нарушений микроциркуляции по В.И. Козлову, 2006, с дополнениями
|
Форма нарушений микроциркуляции |
Описание |
ПМ |
флакс |
ИФМ |
Типовой патологический процесс |
|
Норма |
– |
= контрольной группе |
= контрольной группе |
= контрольной группе |
– |
|
Гиперемическая |
повышение числа функционирующих капилляров, повышение проницеамости сосудистой стенки, расширение микрососудов |
повышен |
снижен |
снижен |
острые воспалительные процессы |
|
Спастическая |
агрегация эритроцитов, снижение числа функционирующих капилляров |
снижен |
снижен |
снижен |
окклюзия микрососудистого русла |
|
Спастико-атоническая |
выраженное нарушение артериоло-венулярных соотношений: уменьшение притока крови в сочетании с затруднением оттока |
значимо снижен |
значимо снижен |
снижен |
хронические воспалительные процессы, в частности, РА (?) |
|
Застойная |
венозная гиперемия |
повышен |
значимо снижен |
снижен |
затруднения венозного оттока и лимфатического дренажа |
|
Стазическая |
резкое снижение кровотока в микроциркуляторном русле и повышенная агрегация эритроцитов |
выраженное снижение |
выражен-ное снижение |
значимо снижен |
прекращение венозного оттока и лимфатического дренажа |
Таблица 2
Вегетативная регуляция кровообращения у больных РА
|
Вегетативная регуляция деятельности системы кровообращения |
Группа РА (n = 75) |
Группа контроля (n = 85) |
р |
|
Выраженная симпатикотония |
7 % |
4 % |
0,0052 |
|
Легковыраженная симпатикотония |
21 % |
12 % |
0,0022 |
|
Эйтония |
41 % |
43 % |
0,064 |
|
Легкая ваготония |
18 % |
30 % |
0,0045 |
|
Выраженная ваготония |
13 % |
11 % |
0,041 |
Полученные данные о кожной микроциркуляции крови у больных свидетельствуют о наличии у больных РА нарушений микроциркуляции по спастико-атоническому типу.
Вывод
В группе РА статистически значимая дисрегуляция деятельности кровообращения на фоне нарушения микроциркуляторного статуса по спастико-атоническому типу. Полученные данные требуют дальнейшего изучения как роли описанных нарушений в развитии кардиоваскулярной патологии при РА, так и их взаимосвязей между собой.
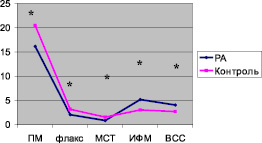
Микроциркуляторный статус больных РА по сравнению с группой контроля
Рецензенты:
Котовщикова Е.Ф., д.м.н., профессор кафедры пропедевтики внутренних болезней, ГБОУ ВПО «Алтайский государственный медицинский университет Министерства здравоохранения России», г. Барнаул;
Федоров Д.В., д.м.н., профессор, зав. кафедрой сестринского дела ГБОУ ВПО «Алтайский государственный медицинский университет Министерства здравоохранения России», г. Барнаул.
Работа поступила в редакцию 15.01.2014.
Библиографическая ссылка
Андриенко А.В., Бубликов Д.С. ВЕГЕТАТИВНО-МИКРОЦИРКУЛЯТОРНЫЕ НАРУШЕНИЯ У БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ // Фундаментальные исследования. 2013. № 12-2. С. 163-166;URL: https://fundamental-research.ru/ru/article/view?id=33296 (дата обращения: 17.05.2026).



