Восстановление костной ткани человека после перенесенной тяжелой травмы и устранение массивных дефектов костей остается актуальной проблемой современной медицины [1, 10].
В нормальных условиях репарация костной ткани происходит за счет остеобластов надкостницы, которые проникают в зону перелома и восстанавливают целостность кости [4, 6]. Несмотря на достаточно активную способность к репарации, костная и хрящевая ткань иногда не в состоянии полностью устранить дефицит тканей, возникший в результате действия повреждающего фактора, что является серьезной проблемой в реконструктивной хирургии и ортопедии. Попытки восстановить утраченную часть кости или хряща предпринимались с давних пор и сводились, прежде всего, к аллотрансплантации или использованию синтетических материалов [11, 17]. Однако у этих широко применяемых, и ставших уже рутинными технологий есть множество недостатков: от наличия иммунологического барьера и дефицита пластического материала до остаточного ограничения качества жизни даже после установки синтетических протезов).
Основную часть биоматериалов для восстановления костных дефектов до недавнего времени получали из хрящевой и/или костной тканей человека и животных, а также компонентов кожи, сухожилий, мозговой оболочки [3, 8, 12]. Однако такие материалы должны готовиться непосредственно перед трансплантацией, либо клиника должна иметь банк для хранения такого материала, что доступно крупным специализированным медицинским центрам; возможности получения значительных количеств аутоматериала весьма ограничены. Все это существенно ограничивает широкое применение аутотрансплантатов.
Значительную роль в ортопедии и травматологии играют металлы [2, 5, 16]. Однако применение при лечении переломов трубчатых костей металлических аппаратов внешней фиксации (АВФ), крепежных элементов в виде винтов, спиц и стержней требует повторного хирургического вмешательства для удаления конструкции и часто сопровождается возникновением эндопротез-ассоциированных осложнений (металлозы, аутоиммунные реакции, асептическое воспаление), а также выделением из металлической конструкции токсических компонентов (никель, хром и др.) [7, 13]. Несмотря на широкое распространение биокерамики, в основном гидроксиапатита, в хирургической стоматологии, ортопедии и травматологии, недостатками такого материала являются его низкая резорбция, что порой приводит к «замуровыванию» имплантированного материала на стадиях in vivo или очень длительному процессу восстановления костной ткани – более 1–2 года, а также низкие остеоиндуктивные свойства материала [9, 15].
В настоящее время наиболее перспективными являются биоразрушаемые полиэфиры монокарбоновых кислот, таких как полилактиды, полигликолиды, полигидроксиалканоаты и т.д. Эти полиэфиры, при свойственном им высоком уровне биосовместимости, распадаются в организме и в окружающей среде на безвредные фрагменты, метаболизирующиеся в конечном случае до воды и углекислого газа, а в некоторых случаях сами являются естественными метаболитами организма [14].
Полигидроксиалканоаты (ПГА) представляют огромный интерес для восстановительной хирургии кости в силу их медленной биорезорбции и высокой биосовместимости. Перспективность ПГА для реконструктивного остеогенеза связана также с наличием у ПГА пьезоэлектрического эффекта.
Цель настоящей работы: исследование остеопластических свойств пористого имплантата на основе поли-3-гидроксибутирата в экспериментальной модели дефекта трубчатой кости кролика.
Материалы и методы исследования
Конструирование ПГБ имплантатов
Для исследований был использован высокоочищенный, измельченный до порошкообразного состояния гомополимер 3-гидроксимасляной кислоты (П3ГБ). Пористые полимерные объемные матриксы получали с использованием техники выщелачивания. Кусочки сахарозы, предварительно спрессованные до размера (1×1×1 см) на лабораторном автоматизированном прессе Carver Auto Pellet 3887, пропитывали раствором полимера в хлороформе, затем сушили при температуре 30 °С. После испарения растворителя матриксы промывали в дистиллированной воде для растворения и удаления сахарозы. Полученный пористый каркас из полимера обрезали до нужных размеров (0,5×0,5×0,5 см3) и использовали в эксперименте.
Свойства имплантатов
Микроструктуру поверхности полимерных композитов и матриксов исследовали с применением сканирующей электронной микроскопии (микроскоп ТМ-3000, Hitachi, Япония). Суммарную пористость и влагопоглощение матриксов определяли методом предельной адсорбции воды. Физико-механические характеристики образцов регистрировали на универсальной электромеханической испытательной машине Instron 5565,5 KN (Великобритания).
Исследование пористых матриксов in vitro
Изоляция культуры ММСК
ММСК выделены из бедренных и большеберцовых костей умерщвленных передозировкой эфирной ингаляции лабораторных крыс. Костный мозг выделяли в асептических условиях после удаления шейки кости; в открытый костномозговой канал с помощью шприца вводили 1 мл среды α-МЕМ с добавлением 20 % телячьей сыворотки и 50 ед. гепарина, костный мозг вымывали и тщательно суспендировали, затем дважды центрифугировали и промывали питательной средой, суспензию клеток переносили в чашку Петри диаметром 90 мм и помещали в СО2-инкубатор.
Посев ММСК на матриксы
П3ГБ пористые матриксы были простерилизованы Н2О2-плазмой (медицинский стерилизатор Sterrad N.X., Jh.&Jh., США) и помещены в 24-луночные культуральные планшеты. После 3 пассажей проводили рассев клеток на стерильные матриксы из расчета 100 000 клеток/мл. Культивирование клеток на матриксах проводили в течение 21 дня в среде ДМЕМ с добавлением 10 % ЭТС, раствора антибиотиков, 0,15 мМ аскорбиновой кислоты, 10 нМ дексаметазона и 10мМ β-глицерофосфата (реактивы Sigma-Aldrich) в 5 %-й атмосфере СО2 при 37 °С с заменой среды на каждый третий день.
Активность щелочной фосфатазы
Для подтверждения дифференцировки клеток в остеобластоподобные использовали один из биохимических маркеров формирования костной ткани – активность фермента костной щелочной фосфатазы, выделяемой остеобластами и предположительно участвующей в минерализации остеоидов. Щелочную фосфатазу оценивали с помощью Alkaline Phosphatase Detection Kit (Sigma) согласно приложенному протоколу.
Исследование пористых матриксов in vivo
Остеопластические свойства П3ГБ исследованы на модели костного дефекта бедренной кости диафизарной зоны у кроликов-самцов породы шиншилла 4–5-месячного возраста. В эксперименте использовано 12 животных, по 4 в каждой группе (n = 3). Костный дефект в первой экспериментальной группе закрывали пористым матриксом на основе П3ГБ, во второй группе – композитным материалом гидроксиапатит/коллаген (препарат «Коллапол», ЗАО Полистом, Москва). В группе сравнения восстановление дефекта осуществляли аутокостью (рис. 1).
Под ксилазиновым наркозом после обработки операционного поля 70 % спиртовым раствором хлоргексидина по переднемедиальной поверхности бедра животным производили разрез кожи длиной 5 см. Мышцы тупым способом разводили и фиксировали. С помощью остеотома на передней поверхности бедра кролика моделировали костный дефект размером 3×4 мм. Далее в костную полость имплантировали матриксы на основе П3ГБ и «Коллапол» (экспериментальные группы), при этом пластика выполнена таким образом, чтобы вся полость дефекта кости была заполнена. Поверх дефекта выполняли периостальную пластику надкостницы ультратонкой пленкой из ПГА. Рана послойно ушивалась наглухо. Накладывалась асептическая повязка. Для профилактики переломов дополнительно проводили иммобилизацию конечности гипсовой лонгетой. Перевязку проводили один раз в сутки в течение семи дней. На протяжении первых трех суток с целью обезболивания вводили в/м Sol. Ketonali 0,1. В послеоперационном периоде осуществляли динамическое наблюдение за состоянием животных (аппетит, двигательная активность, состояние оперированных конечностей). Рентгенологическое исследование оперированных конечностей опытных животных выполняли на аппарате РУМ-20 в режиме 44 mA 0,1 kB с экспозицией в 1 с. Проводили сравнительный анализ рентгенографических данных на 60-е, 90-е, 120-е сутки после пластики костной полости. Оценивались размеры костного дефекта, его форма, однородность структуры регенерата, состояние надкостницы, кортикальной пластины и костномозгового канала, а также переломы в месте формирования дефекта.
Для морфологического исследования образцы костной ткани подвергались декальцинации в растворе «Трилона-Б» с последующей парафиновой проводкой. Гистологические срезы толщиной 5–7 мкм окрашивали гематоксилином и эозином. При микроскопическом исследовании оценивали состояние окружающих кость мягких тканей, надкостницы, кортикального слоя, костномозгового канала.
Результаты исследования и их обсуждение
Сконструированы и исследованы 3D пористые матриксы на основе П3ГБ диаметром 4 мм, высотой 5 мм, весом 0,0552 г. Анализ микроструктуры носителей, выполненный с применением морфологического анализа (программа обработки данных Scanmaster), показал, что кроме основных крупных пор в носителе сформирована система более мелких пор по границе контактов между полимерными ячейками; приведены соответствующие дифференциальные и интегральные кривые распределения пор по размерам. Суммарная площадь всех выделенных пор составляет около 87,3 %. При этом крупные поры размером 104–120 мкм составляют в носителе до 90 %; остальные 10 % приходятся на мелкие поры (5,7–10 мкм). Результаты компьютерного анализа согласуются с экспериментальными данными по определению суммарного объема пор по влагоемкости (88 %). Влагопоглощение полимерного носителя составило 38,5 ± 0,20 %.

Рис. 1. Технология эксперимента пластики костного дефекта: А – группа сравнения; 2 – группа с применением «Коллапола»; В – пористый матрикс на основе П3ГБ
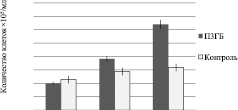
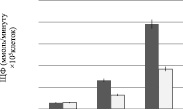
По результатам МТТ-теста (рис. 2), проведенного на 3, 7 и 10 сутки, количество клеток на на 3D матриксах составило 0,63⋅105 клеток/мл, что достоверно выше, чем на культуральном пластике 0,3⋅105 клеток/мл. Результаты определения активности щелочной фосфатазы согласуются с результатами МТТ-теста. ЩФ на 10 сутки культивирования ММСК на среде с факторами дифференцировки составила у клеток на 3D матриксах 3,908 ммоль/минуту⋅105 клеток по сравнению с контролем (рис. 3).


Рис. 2. 3D пористые матриксы на основе П3ГБ (слева – фотография, маркер 1 см; справа – РЭМ-изображение)
а b
Рис. 3. Исследование способности матриксов адгезировать дифференцированные клетки ММСК в сравнении с контролем (культуральный пластик): а – количество жизнеспособных остеобластов на 3D матриксах; b – активность щелочной фосфатазы остеобластов на 3D матриксах после 10 дней культивирования.
Результаты эксперимента in vivo
Результаты сравнительного анализа клинической картины у экспериментальных животных первой экспериментальной группы (после замещения дефекта ПГБ) и второй экспериментальной группы (замещение Коллаполом) и группы сравнения представлены в таблице.
В раннем послеоперационном периоде наблюдали вялое состояние животных, кролики мало двигались, не опирались на оперированную конечность. Восстановление аппетита и двигательной активности кроликов произошло к 3–5 суткам, на 7–9 сутки после операции у животных второй экспериментальной группы появлялся отек мягких тканей в области операции, в группе сравнения – локальная гиперемия кожи. В среднем на 15,5 ± 1,2 сутки отек и гиперемия купировались. Опора на конечность появлялась на 5,01 ± 1,5 сутки после операции. Операционные раны заживали per prima, случаев нагноения не отмечено, послеоперационные швы удалялись на 7 сутки. Летальных случаев не зафиксировано.
При анализе рентгенологических исследований оперированных конечностей кроликов выявлено следующее. При замещении костного дефекта пористым 3D матриксом на основе П3ГБ уже на 60-е сутки определялась полость округлой формы в средней трети бедренной кости размерами 1,5×2 мм, что значительно меньше, чем во второй экспериментальной группе. Полость дефекта имела четкие контуры, без ободка склероза. Надкостница не изменена, периостальная реакция отсутствовала. На 120-е сутки произошло полное восстановление костного дефекта бедренной кости (рис. 4).
Во второй экспериментальной группе на 60-е сутки на обзорной рентгенограмме нижних конечностей, после имплантации Коллапола, определялась полость округлой формы в средней трети бедренной кости размерами 2×3 мм. Полость с четкими контурами без ободка склероза. Однако, на 120-е сутки в данной группе произошло сокращение размеров костного дефекта бедренной кости в 2 раза в сравнении с R-картиной на 60-е сутки наблюдения, визуализировалось уменьшение полости до 1×1,5 мм. Контуры полости нечеткие за счет прорастания (заполнения) костной ткани в полость дефекта, периостальная реакция отсутствовала, тем не менее полного восстановления дефекта не произошло.
Течение послеоперационного периода у экспериментальных животных
|
Исследуемый признак |
Сутки после операции (М ± SD) |
||
|
Первая (П3ГБ) экспериментальная |
Вторая («Коллапол») экспериментальная |
Группа сравнения (пластика аутокостью) |
|
|
Восстановление опороспособности оперированной конечности |
5 ± 0,9* |
6 ± 0,9* |
6 ± 1,2 |
|
Заживление операционной кожной раны |
7,4 ± 0,9* |
7,2 ± 0,9* |
8,9 ± 1,7 |
|
Купирование отека и гиперемии мягких тканей |
8,75 ± 0,96* |
9,28 ± 0,9* |
11,7 ± 1,8 |
Примечание. * – данные статистически достоверны при p < 0,05.
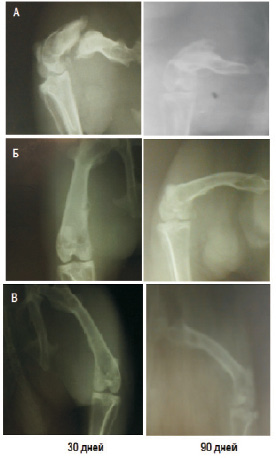
Рис. 4. Данные рентгенологических исследований динамики восстановления модельного дефекта костной ткани: А – группа сравнения; Б – вторая экспериментальная группа; В – первая экспериментальная группа (3D пористые имплантаты на основе П3ГБ)
В группе сравнения на обзорной рентгенограмме на 60-е сутки определялся патологический перелом бедренной кости в средней трети (в области ранее сформированного дефекта костной ткани) со смещением костных отломков по ширине и под углом, диастазом последних 3–4 мм. Определялись признаки выраженной периостальной реакции костных отломков, локальные очаги деструкции костной ткани, остеолизис. На 120-е сутки происходила его частичная консолидация в сравнении с R-картиной на 60-е сутки наблюдения. Визуализировалось формирование ложного сустава в месте перелома, признаки хронического периостального воспаления, локальные очаги деструкции костной ткани.
При гистологическом исследовании через 30 дней в зоне дефекта при имплантации пористого матрикса П3ГБ вокруг имплантата определяется неравномерной толщины зона из рыхлой волокнистой соединительной ткани, содержащая инфильтрацию из лимфоцитов и немногочисленных сегментоядерных лейкоцитов (рис. 5). В ряде полей зрения клеточная инфильтрация, включающая единичные макрофаги, распространяется на пористый матрикс. Через месяц после имплантации коммерческого препарата «Коллапол» поверхность моделированного дефекта костной ткани покрыта слоем некротических масс, фибрина в которых видны костные отломки. Вокруг имплантата наблюдалась развитая воспалительная инфильтрация с преобладанием полиморфноядерных лейкоцитов (рис. 6). Костный дефект в группе сравнения на этом сроке после оперативного вмешательства был заполнен рыхлой волокнистой соединительной тканью, богатой капиллярного типа сосудами, содержащей неравномерно выраженную инфильтрацию из лимфоцитов, немногочисленных нейтрофилов, макрофагов.
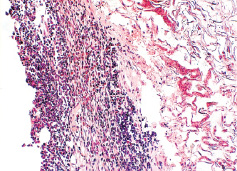
Рис. 5. Костный дефект через 30 дней после имплантации пористого матрикса П3ГБ. Вокруг имплантата определяется воспалительный вал из лимфоцитов и сегментоядерных лейкоцитов
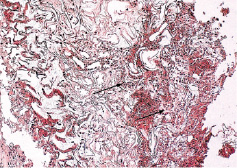
Рис. 6. Дефект костной ткани через месяц после имплантации коммерческого препарата «Коллапол». Развитая воспалительная реакция вокруг имплантата с преобладанием полиморфноядерных лейкоцитов (↑)
Спустя 60 дней в первой экспериментальной группе матрикс П3ГБ окружен рыхлой волокнистой соединительной тканью, содержащей многочисленные макрофаги, в том числе гигантские многоядерные остеокластоподобные клетки, обеспечивающие лакунарную резорбцию костных фрагментов (рис. 7). Со стороны рыхлой соединительной ткани в толщу пористого имплантата врастают мелкие тонкостенные кровеносные сосуды капиллярного типа. На периферии имплантатов появляются участки из плотной волокнистой соединительной ткани, включающие остеобласты, что является признаком начала процесса замещения мягкой соединительной мозоли на остеоидное вещество. На этом сроке хорошо заметна резорбция полимерного имплантата, сопровождающаяся его фрагментацией.
Во второй экспериментальной группе на 60 сутки послеоперационного периода полость дефекта была заполнена преимущественно зрелой соединительной тканью, в которой располагаются частицы материала «Коллапол», окруженные лимфоцитами, полиморфноядерными лейкоцитами, макрофагами. Сохраняются участки, представленные клеточным детритом с перифокальной воспалительной реакцией (рис. 8).
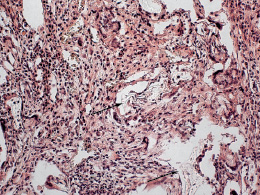
Рис. 7. Матрикс П3ГБ в опытной группе спустя 60 дней после операции. Многочисленные гигантские многоядерные клетки в волокнистой соединительной ткани, окружающей фрагменты пористого имплантата. Резорбция полимерного имплантата, сопровождающаяся его фрагментацией (↑)
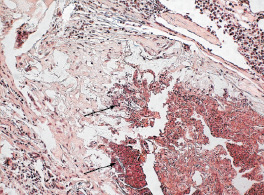
Рис. 8. Зона дефекта в группе сравнения на 60 день послеоперационного периода. Возле частиц материала «Коллапол» сохраняются участки, редставленные клеточным детритом с перифокальной воспалительной реакцией (↑)
В группе сравнения дефект заполнен слабо васкуляризированной грубоволокнистой рубцовой тканью с фрагментами незрелого хряща.
На 90 сутки эксперимента в зоне имплантации ПГБ регистрируется активное формирование новообразованной костной массы. Новообразованная кость имеет относительно зрелый характер с отчетливо выраженным пластинчатым строением, формированием остеонов (рис. 9). Центр костного регенерата представлен новообразованными остеоидными балками, на периферии костные структуры имеют достаточно упорядоченное расположение, их граница с окружающей дефект костью выражена нечетко. Костномозговой канал равномерно широкий, заполнен костным мозгом. На данном этапе репаративные процессы протекают без активного участия гистиоцитов и многоядерных клеток, без выраженной воспалительной реакции.
Во второй экспериментальной группе через три месяца после имплантации препарата «Коллапол» репаративный остеогенез отличается сохранением в центре дефекта относительно крупных участков из рыхлой неоформленной и плотной волокнистой соединительной ткани (рис. 10).
В группе сравнения зона повреждения заполнена костной мозолью из вновь сформированной кости с хаотично расположенными, имеющими разнообразную форму балками и полостями с костным мозгом (рис. 11). Костномозговой канал неравномерно сужен.
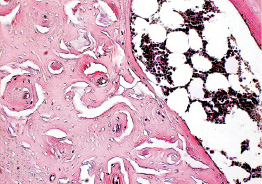
Рис. 9. Результаты эксперимента через 90 суток. В зоне имплантации ПГБ определяется новообразованная кость, имеющая достаточно зрелый вид. Костномозговой канал содержит костный мозг
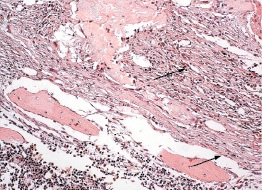
Рис. 10. Репаративный остеогенез через три месяца после имплантации препарата «Коллапол». В центре дефекта сохраняются относительно крупные участки из волокнистой соединительной ткани (↑)
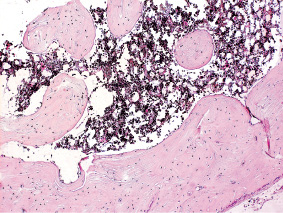
Рис. 11. Зона повреждения в контрольной группе через 90 суток. Определяется костная мозоль из вновь сформированной кости с хаотично расположенными балками и полостями с костным мозгом
Таким образом, по данным рентгенологических и морфологических исследований установлено, что при имплантации пористого объемного носителя на основе П3ГБ процесс регенерации костной ткани происходит быстрее, с менее выраженной экссудативной воспалительной реакцией, с формированием новообразованной кости, имеющей более зрелый характер.
Работа выполнена за счет средств государственного задания на проведение фундаментальных исследований РАН (проект № гос. регистрации 01201351505).
Рецензенты:
Черданцев Д.В., д.м.н., профессор, заведующий кафедрой и клиникой хирургических болезней № 2 им. проф. А.М. Дыхно с курсом эндоскопии и эндохирургии ПО, Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого, г. Красноярск;
Горбунов Н.С., д.м.н., профессор, заведующий кафедрой оперативной хирругии и топографической анатомии, Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого, г. Красноярск.
Библиографическая ссылка
Шумилова А.А., Шишацкая Е.И., Маркелова Н.М., Винник Ю.С., Зуев А.П., Кириченко А.К., Соловьева Н.С. ОСТЕОПЛАСТИЧЕСКИЕ СВОЙСТВА МАКРОПОРИСТЫХ ИМПЛАНТАТОВ НА ОСНОВЕ ПОЛИ-3-ГИДРОКСИБУТИРАТА В РЕГЕНЕРАЦИИ КОСТНОГО ДЕФЕКТА ТРУБЧАТОЙ КОСТИ КРОЛИКА // Фундаментальные исследования. 2015. № 7-4. С. 697-706;URL: https://fundamental-research.ru/ru/article/view?id=38804 (дата обращения: 01.05.2026).



