Введение различных минералов в состав композитных материалов часто во многом определяется их способностью выдерживать высокую температуру. Немалый интерес представляют такие вещества, как– слюды, глинистые материалы и им подобные. Перед появлением новых аморфных или кристаллических фаз в таких веществах идёт процесс дегидроксилации, обусловленный их нагревом и сопровождающийся изменением физических свойств минералов при выводе адсорбированной межслоевой воды [2, 7–11].
Несмотря на многочисленные работы, детального понимания процесса дегидроксилации до сих пор нет. Важными факторами, влияющими на обсуждаемый процесс, являются уменьшение размеров частиц и понижение степени кристаллизации. Данные эффекты снижают температуру, при которой начинается реакция. Многими авторами предпринимались попытки разобраться с механизмом дегидроксилации, изучая кинетические реакции.
Однако во всех случаях, в силу особенностей исследуемых образцов или выбранных экспериментальных условий, опыты могут решать лишь конкретные физические задачи, но при этом всё-таки не дают возможности сделать обобщающие выводы относительно механизма обсуждаемого явления.
Цель работы состоит в том, чтобы, используя квантово-механические представления, изучить процесс дегидроксилации различных веществ, например слюд. Понимание механизма дегидроксилации важно для корректной оценки, прежде всего, термической стойкости слюд, а также выявления механизмов межфазового взаимодействия рассматриваемых веществ. Полученные результаты нацелены на выявление путей улучшения технологии производства качественных композиционных материалов на основе слюд.
Необходимо получить самые общие сведения и закономерности процесса дегидроксилации слюд. Изучая литературные данные о механизме дегидроксилации различных минералов, включая слюды, можно выделить две модели. Первая модель рассматриваемого процесса предполагает перемещение гидроксильных ионов (гомогенный процесс). Второй моделью является процесс перемещения протонов (негомогенный или гетерогенный процесс). Гомогенный механизм имеет ряд недостатков, при этом гетерогенный механизм представляется более правдоподобным. Для доказательства реальности гетерогенного варианта процесса дегидроксилации требуется провести соответствующие квантово-механические расчёты с привлечением экспериментальных данных. С помощью таких методов, как термография, рентгенофазовый анализ, ИК-спектроскопия, и других методов можно оценить степень дегидроксилации [2, 7–11].
Только анализ поведения протонов в гидроксильных группах в условиях, при которых предполагаемая реакция с участием протона становится возможна, позволит понять исследуемый механизм дегидроксилации. При одновременном использовании вышеуказанных методов возможно достаточно полное описание процесса разложения слюд.
В настоящее время имеется несколько моделей или механизмов процесса потери гидроксильных групп OH–. В одной из рассматриваемых моделей предполагается, что в диффузии участвует один изолированный протон. В таком случае скорость потери гидроксильных групп будет определяться высотой и формой энергетического барьера, зависящего от природы слюды. Другими словами, каждая слюда имеет свою энергию активации процесса дегидроксилации. Таким образом, данный процесс будет протекать для разных слюд при разных температурах [8].
Ранее предложенная структура безводного мусковита (Эберхарт, 1963) требует, чтобы в процессе дегидроксилации атом кислорода сохранял своё местоположение [2]. Поскольку изолированный кислород не обладает возможностью диффундировать, как изолированный протон, то следствием этой модели является предположение о взаимодействии протона с кислородом в процессе его перехода.
Для того чтобы выяснить механизм дегидроксилации и понять роль в этом механизме протона, были проведены исследования, в частности методом ИК-спектроскопии [7–11]. Каждый протон при нормальной температуре локализуется вблизи атома кислорода, но может принимать участие в перемещении по свободным орбиталям соседних атомов кислорода. Так как энергия колебаний гидроксильных ионов тесно связана с ИК-спектрами, то полезно изучить влияние температуры на ИК-спектры различных слюд.
Изучение ИК-спектров слюд при высокой температуре показало, что имеется относительно небольшое смещение частоты максимума полосы поглощения гидроксильных групп в сторону более низких частот. Порядок указанных смещений находится в диапазоне значений от половины до трети ширины полос при изменении температуры от 400–500 °С.
Указанные процессы обратимы и в основном объясняются небольшими смещениями межатомных расстояний внутри решётки минералов. Для всех слюд отмечено, что интенсивность полос поглощения уменьшается при увеличении температуры [9]. В результате последующего охлаждения полосы снова восстанавливаются. Наблюдаемые изменения в спектрах не объясняются изменением ориентации ОН ионов, поскольку, как это следует из экспериментов, ориентация гидроксилов в слюдах не изменяется с температурой.
Для объяснения изменения интенсивности ИК-спектров недостаточно рассуждений о перемещении электронного облака кислорода. Такой механизм должен изменить дипольный момент осциллятора, а вслед за этим и интенсивность поглощения. Кроме того, характер изменения полос валентных и деформационных колебаний схожи; зависимость интенсивности при изменении температуры сильно зависит от типа слюды; к тому же отношение коэффициента поглощения к содержанию воды почти втрое больше для мусковита по сравнению с флогопитом, при этом относительные изменения Kон при вариациях температуры сопоставимы для всех слюд.
В ранних работах по слюдам уменьшение интенсивности полос ОН связывалось с изменением числа вибраторов из-за делокализации протонов, при этом локализованные и нелокализованные протоны находятся в динамическом равновесии:

В соответствии с этим подходом представляет интерес более детальный анализ системы ОН…О. Необходимо провести квантово-механические расчеты механизма дегидроксилации [1, 3–6]. Делокализацию протона, с позиции квантовой механики, можно рассматривать как процесс его перехода в возбуждённое состояние. В качестве физической модели процесса дегидроксилации можно рассмотреть два атома кислорода с симметрично расположенным между ними протоном. Система протона, связанная с атомом кислорода, представляет гармонический осциллятор, потенциальная энергия которого представлена на рис. 1. В рамках данной модели в невозбуждённом состоянии протон не имеет возможности переходить от одного атома кислорода к другому. С ростом температуры протон, переходя в возбуждённое состояние, будет находиться на более высоких энергетических уровнях (рис. 1).
При увеличении значений энергии протона до величин, сопоставимых с высотой потенциального барьера, будет увеличиваться его «прозрачность» и соответственно расти вероятность его делокализации. Можно показать, что в результате перехода протона в возбуждённое состояние в области значений энергий, соответствующих высоте барьера, наблюдаемая частота полос поглощения не изменяется.
В предлагаемой модели делокализация протона (протонирование) определяет перестройку водородной связи, что неизбежно отражается на ИК-спектрах. Выявлено, что именно эта связь характеризует наблюдаемые валентные колебания группы ОН. В экспериментах по мере увеличения энергии водородной связи наблюдается уменьшение частоты поглощения ОН группы, при этом полоса уширяется на фоне снижения её интенсивности.
Иначе ведёт себя полоса деформационных колебаний ОН, которая испытывает увеличение частоты и ширины, не изменяя при этом свою интенсивность.
Иногда полагают, что вариация частоты валентных колебаний ОН обусловлена изменением потенциальной энергии вибратора при деформации связи ОН. С другой стороны, известно, что значения частоты ОН коррелируют с частотой колебания трёхатомной системы ОН…О. Также обсуждается изменение частоты под воздействием второго потенциального источника, обеспечивающего условия возникновения водородной связи.
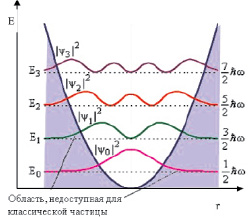
Рис. 1. Потенциальная энергия протона гидроксильной группы
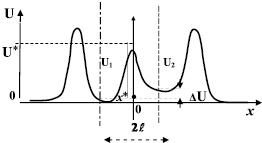
Рис. 2. Потенциальная энергия двух осцилляторов
Недостаточное толкование о вопросе изменений интенсивности полосы валентных колебаний вызывает необходимость проведения квантово-механического представления механизма дегидроксилации. Последующий расчет позволит определить степень локализации протона вблизи соответствующих атомов кислорода, найти положение энергетических уровней и степени их локализации.
За основу предлагаемой модели выберем систему из двух источников с параболической зависимостью потенциальной энергии U и смещения x от положения равновесия (рис. 2).
Выберем две потенциальные зависимости (U1 и U2), характеризующие воздействие двух рассматриваемых атомов на протон, при этом учтём смещение минимумов потенциальных энергий данных источников на величину ΔU = U2min – U1min.
Общая потенциальная энергия системы двух близко расположенных осцилляторов U(x) имеет промежуточный барьер ΔU с координатой
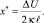 (1)
(1)
Выражение (1) соответствует пересечению потенциальных функций гармонических осцилляторов U1(x) и U2(x), имеющих вид
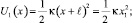 (2)
(2)
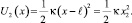 (3)
(3)
Высота промежуточного барьера, разделяющего потенциальные ямы, определяется выражением
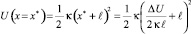 (4)
(4)
или 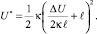 (5)
(5)
Локализация протона, связанного с одним из атомов кислорода, определяется его волновой функцией ψ(x), а её квадрат даёт значение плотности вероятности нахождения частицы в заданной области её движения. Вероятность обнаружения микрочастицы вблизи второго атома кислорода мала. Однако наличие второго потенциального барьера, несомненно, меняет данную вероятность. Также понятно, что при увеличении энергии протона (т.е. при его переходе в возбуждённое состояние) растёт прозрачность среднего барьера вследствие туннельного эффекта. Изменение вероятности нахождения протона вблизи второго потенциального источника соответствует процессу дегидроксилации рассматриваемой системы. Следует отметить, что туннельный эффект может существенно менять делокализацию микрочастицы только при её энергии не превышающей высоту барьера, и, следовательно, не является определяющим процессом. Более важным механизмом наблюдаемых изменений является смешивание волновых функций и смещение энергетических уровней при сближении двух атомов. Поведение микрочастицы соответствует волновому уравнению Шрёдингера, полностью определяющему её движение.
В квантовой механике движение частицы не может быть точно задано и определяется только вероятностью её локализации в пространстве при помощи волновой функции ψ(x).
Для первого изолированного атома с потенциальной энергией U1(x) запишем
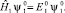 (6)
(6)
Здесь волновая функция ψ является решением стационарного уравнения Шрёдингера. Также запишем и для второго атома:
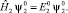 (7)
(7)
Функции 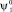 и
и 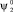 – волновые функции, которые соответствуют двум близко расположенным изолированным потенциальным источникам с невозмущёнными энергетическими уровнями.
– волновые функции, которые соответствуют двум близко расположенным изолированным потенциальным источникам с невозмущёнными энергетическими уровнями.
При сближении двух источников их волновые функции и энергетический спектр взаимно нарушаются. Проделав в дальнейшем соответствующие квантово-механические расчеты, можно найти положение энергетических уровней, степень их локализации, выявить основные черты и понять механизм дегидроксилации слюд.
Таким образом, в работе предлагается модель процесса дегидроксилации минералов, в частности слюд, при их нагреве. Предполагается возможность перехода атома водорода гидроксильной группы к соседнему атому кислорода.
В дальнейшем, проведя соответствующие квантово-механические расчеты, можно подтвердить предложенную модель дегидроксилации слюд.
Рецензенты:
Воронов В.К., д.х.н., профессор, Иркутский национальный исследовательский технический университет, г. Иркутск;
Чупин В.Р., д.т.н., профессор, директор института архитектуры и строительства, Иркутский национальный исследовательский технический университет, г. Иркутск.
Библиографическая ссылка
Шишелова Т.И., Липовченко Е.Л. МЕХАНИЗМ ДЕГИДРОКСИЛАЦИИ МИНЕРАЛОВ С ПОЗИЦИИ КВАНТОВОЙ МЕХАНИКИ // Фундаментальные исследования. 2015. № 6-2. С. 311-315;URL: https://fundamental-research.ru/ru/article/view?id=38562 (дата обращения: 31.05.2026).



