Биомасса является возобновляемым ресурсом и привлекает внимание в качестве альтернативы ископаемому топливу, а производство этанола из биомассы (биоэтанол) представляет собой практическую альтернативу бензину. Преобразование растительных клеточных стенок представляет собой получение биоэтанола второго поколения [8]. Лигноцеллюлоза – это самая распространенная биомасса на земле. Однако прочность биомассы стала главным фактором, влияющим на производство биотоплива [7]. Целлюлозосодержащее сырье представляет собой прочную матрицу, образованную целлюлозой, гемицеллюлозой и лигнином; взаимосвязь этих компонентов обусловливает устойчивость матрицы ко всем внешним воздействиям, поэтому для ее деструкции применяют различные способы предобработки. Следовательно, предобработка служит важным этапом устранения прочности сырья и повышения выхода сбраживаемых сахаров на этапе энзиматического разрушения [6]. Наиболее перспективным для России сырьем в производстве биоэтанола является непищевое целлюлозосодержащее сырьё (древесина, солома, отходы обработки зерна), поскольку крахмало- и сахаросодержащее сырьё дорого и в наших природно-климатических условиях может быть использовано только для выработки спирта пищевого и медицинского назначения. В ИПХЭТ СО РАН в качестве сырья используется возобновляемый источник сырья: биомасса энергетической злаковой культуры – Мискантус китайский (М). Сейчас это растение позиционируют в качестве перспективного целлюлозосодержащего сырья для производства целлюлозы и продуктов ее модификации [1, 4–5]. Целью данной работы являлось исследование ферментативного гидролиза в водной среде лигноцеллюлозного субстрата (ЛЦС) из мискантуса и последующее получение биоэтанола, а также изучение влияния последовательности технологических стадий осахаривания-сбраживания на процесс биосинтеза этанола.
Материалы и методы исследования
Субстратом для получения биоэтанола являлся ЛЦС мискантуса, полученный на опытном производстве ИПХЭТ СО РАН в одну стадию обработкой мискантуса разбавленным раствором азотной кислоты при температуре 90–96 °С. Определение основных характеристик субстрата (массовой доли (м.д.) целлюлозы по Кюршнеру, м.д. пентозанов, м.д. кислотонерастворимого лигнина, зольность) проводилось по стандартным методикам. Характеристики ЛЦС М представлены в табл. 1.
Таблица 1
Характеристики используемого субстрата
|
Характеристики м.д., % |
ЛЦС М |
|
Целлюлоза по Кюршнеру |
88,6 |
|
Пентозаны |
7,9 |
|
Кислотонерастворимый лигнин |
10,8 |
|
Зольность |
4,8 |
В работе использовались ферментные препараты «Целлолюкс-А» (производитель ПО «Сиббиофарм», Бердск) и «Брюзайм BGX» (производитель «Polfa Tarchomin Pharmaceutical Works S.A.», Польша, для компании «Diadic International Inc.», США). Препарат «Целлолюкс-А» позиционируется на рынке как целлюлаза для расщепления некрахмалистых полисахаридов, «Брюзайм BGX» – как гемицеллюлаза.
Технологические стадии осахаривания и сбраживания в данной работе проводились последовательно и одновременно. Для проведения процессов в колбу Эрленмейера емкостью 1000 мл помещали навеску субстрата и дистиллированную воду. Концентрация субстрата составила 90 г/л.
При последовательном процессе осахаривания-сбраживания (ППОС) ферментолиз проводился в водной среде при рН 4,6–4,7 и при непрерывном перемешивании на платформе «ПЭ – 6410 М» с частотой 150 мин-1. Температура гидролиза составляла (46 ± 2) °С, продолжительность – 72 ч. Мультиэнзимная композиция вносилась следующим образом: «Целлолюкс – А» в расчете 0,04 г фермента на 1 г субстрата и «Брюзайм BGX» в расчете 0,2 г фермента на 1 г субстрата. Полученный ферментативный гидролизат стерилизовался методом автоклавирования при 0,5 атм в течение 40 мин.
При одновременном процессе осахаривания–сбраживания (ОПОС) ферментолиз проводился в приведённых выше условиях, но его продолжительность составила 24 ч, после этого среда охлаждалась до 28 °С, вносились засевные дрожжи и в течение трех последующих суток проводилось спиртовое брожение, совмещенное с осахариванием.
Концентрация редуцирующих веществ (РВ) в пересчете на глюкозу определялась спектрофотометрически с помощью реактива на основе 3,5-динитросалициловой кислоты на «UNICO UV-2804». Выход редуцирующих веществ (РВ) рассчитан с учетом коэффициента 0,9, обусловленного присоединением молекулы воды к ангидроглюкозным остаткам соответствующих мономерных звеньев в результате ферментативного гидролиза.
Ферментативные гидролизаты ЛЦС М сбраживались с помощью дрожжей Saccharomyces сerevisiae Y-1693 (ФГУП «ГосНИИГенетика», г. Москва). Доза инокулята составляла 10 %. Дрожжи находились в экспоненциальной фазе развития имели следующие характеристики: общее количество – 141,5 млн КОЕ/мл, из них почкующихся – 27,6 %. Спиртовое брожение проводилось в анаэробных условиях при 28 °С в течение трех суток.
Объемная доля спирта в бражках определялась ареометром в дистилляте, полученном перегонкой спирта из бражки согласно ГОСТ Р 51135-2003 [2]. По крепости полученных бражек и концентрации РВ в исходной среде рассчитывался выход биоэтанола. Теоретическая концентрация этанола рассчитывалась по стехиометрическому уравнению брожения, выход биоэтанола – как отношение экспериментальной концентрации этанола к теоретической. Полученные образцы биоэтанола концентрировались методом простой перегонки, дополнительной очистки не проводилось. Анализ этанола выполнен методом газожидкостной хроматографии (ГЖХ) по ГОСТ Р 51786-2001 [3] на газовом хроматографе с пламенно-ионизационным детектором «Кристалл 2000М» фирмы «СКБ Хроматэк».
Результаты исследования и их обсуждения
На рисунке представлена зависимость концентрации РВ от продолжительности процессов осахаривания-сбраживания ЛЦС М, проводимых последовательно и одновременно.
Полученные результаты показали, что при ППОС накопление РВ происходит через 72 ч и составляет 65,4 г/л, а при ОПОС – через 32 ч и составляет 64,5 г/л. Это можно объяснить тем, что при добавлении дрожжей в ОПОС через 24 ч от начала процесса РВ начинают расходоваться на синтез этанола, то есть они отводятся из системы, и, таким образом, равновесие суммарной ферментативной реакции гидролиза целлюлозы постоянно смещается в сторону образования продуктов реакции. Этим достигается интенсификация процесса осахаривания.
Эффективность конверсии целлюлозы в РВ для ППОС составила 72,6 %, а для ОПОС – 71,6 %. Таким образом, химическая предобработка мискантуса в одну стадию методом азотнокислой варки позволяет получать качественный субстрат с высокой реакционной способностью к ферментолизу. Результаты спиртового брожения ферментативного гидролизата ЛЦС мискантуса при проведении процессов осахаривания-сбраживания последовательно и одновременно представлены в табл. 2.
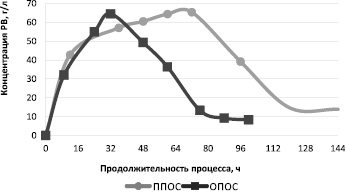
Зависимости концентрации РВ от продолжительности процессов при последовательном и одновременном осахаривании-сбраживании ЛЦС М
Таблица 2
Результаты ферментолиза и спиртового брожения при проведении технологических стадий последовательно и одновременно для ЛЦС М
|
Показатель |
ППОС |
ОПОС |
|
Концентрация РВ в ферментативном гидролизате, г/л |
65,4 |
64,5 |
|
Крепость бражки, об. % |
3,0 |
3,5 |
|
Остаточная концентрация РВ в бражке, г/л |
10,0 |
8,3 |
|
Выход биоэтанола, % от теоретического |
70,9 |
83,7 |
|
Выход биоэтанола из 1 т сырья, дал |
19,4 |
22,6 |
Таблица 3
Содержание примесей в опытных образцах биоэтанола из ЛЦС М
|
Показатель |
Опытные образцы биоэтанола при |
|
|
ППОС |
ОПОС |
|
|
Массовая концентрация альдегидов, в пересчёте на безводный спирт, мг/дм3, не более |
6100 |
4100 |
|
Массовая концентрация сивушного масла, в пересчёте на безводный спирт, мг/дм3, не более |
2500 |
2400 |
|
Массовая концентрация эфиров, в пересчёте на безводный спирт, мг/дм3, не более |
70 |
100 |
|
Содержание метанола в пересчёте на безводный спирт, об. %, не более |
0,002 |
0,002 |
При ППОС синтезируется биоэтанол с выходом 70,9 % от теоретического, выход биоэтанола из 1 т М составляет 19,4 дал. При ОПОС биоэтанол синтезируется с выходом 83,7 % от теоретического, а выход биоэтанола из 1 т М – 22,6 дал. Сравнение синтеза биэтанола, полученного при проведении процесса осахаривания-сбраживания последовательно и одновременно, показывает, что при одновременном процессе выход этанола увеличивается в 1,2 раза по сравнению с последовательным процессом.
Кроме того, при ОПОС исключается стадия фильтрования ферментативного гидролизата и в 1,5 раза сокращается продолжительность технологических стадий: для ППОС требуется 6 суток, для ОПОС – 4 суток. При ОПОС остаточная концентрация редуцирующих веществ в бражке ниже на 1,7 г/л, чем при ППОС, что также указывает на повышение эффективности процесса.
Результаты качества полученных образцов биоэтанола приведены в табл. 3.
В опытных образцах объёмная доля метанола крайне мала – 0,002 об. %. Также в опытных образцах мало эфиров, что косвенно может указывать на чистоту культуры дрожжей при брожении и благоприятные условия для биосинтеза этанола. Довольно высокая концентрация альдегидов в опытных образцах (от 4100 мг/дм3 до 6100 мг/дм3) связана с природой сырья, поскольку исключено накопление фракции альдегидов (фурфурола и оксиметилфурфурола) в процессе ферментативного гидролиза, так как процесс проводился при температуре (46 ± 2) °С и рН 4,6-4,7. Массовая концентрация сивушного масла значительно высокая (2400–2500 мг/дм3),что объяснимо, так как ректификация опытного образца не проводилась. Таким образом, ферментативный гидролиз ЛЦС М позволяет получить доброкачественный гидролизат с низким содержанием вредных примесей и обуславливает низкое содержание побочных и вторичных продуктов спиртового брожения в бражках.
Выводы
Выявлено, что химическая предобработка мискантуса раствором азотной кислоты в одну стадию позволяет получать субстрат с высокой реакционной способностью к ферментативному гидролизу: выход РВ при ППОС составил 65,4 г/л, при ОПОС – 64,5 г/л.
Получен биоэтанол на среде ферментативного водного гидролизата ЛЦС М с помощью штамма Saccharomyces сerevisiae Y-1693. При ППОС синтезируется биоэтанол с выходом 70,9 % от теоретического, выход биоэтанола из 1 т М составляет 19,4 дал. При ОПОС биоэтанол синтезируется с выходом 83,7 % от теоретического, а выход биоэтанола из 1 т М – 22,6 дал.
Установлено, что при проведении процессов осахаривания-сбраживания выход биоэтанола увеличивается в 1,2 раза по сравнению с последовательным процессом. Проведение технологических стадий одновременно позволяет сократить продолжительность процесса в 1,5 раза и исключить фильтрацию промежуточного продукта – ферментативного гидролизата. Это позволит уменьшить затраты при получении биоэтанола и упростить технологический процесс, что важно для его успешного масштабирования.
Показано, что спирты, полученные из ЛЦС М, характеризуются низким содержанием эфирной фракции и метанола.
Рецензенты:
Новожилов Е.В., д.т.н., профессор, заведующий кафедрой биотехнологии и биотехнических систем, Северный (Арктический) федеральный университет, г. Архангельск;
Комарова Л.Ф., д.т.н., профессор, заведующая кафедрой химической техники и инженерной экологии, ФГБОУ ВПО «Алтайский государственный технический университет им. И.И. Ползунова», г. Барнаул.
Работа поступила в редакцию 01.04.2015.
Библиографическая ссылка
Байбакова О.В. БИОКОНВЕРСИЯ ЛИГНОЦЕЛЛЮЛОЗНОГО СУБСТРАТА МИСКАНТУСА В ЭТАНОЛ // Фундаментальные исследования. 2015. № 2-13. С. 2783-2786;URL: https://fundamental-research.ru/ru/article/view?id=37561 (дата обращения: 26.04.2026).



