Сахарный диабет (СД) является одним из наиболее распространенных в мире заболеваний эндокринной системы. К настоящему времени зарегистрировано более 230 млн человек, страдающих СД. Согласно прогнозам экспертов Всемирной организации здравоохранения, к 2030 г. в мире число больных СД увеличится до 366 млн человек. Учитывая высокий уровень инвалидизации и смертности от СД (3-е место среди непосредственных причин смерти), проводится огромная работа по совершенствованию традиционных методов лечения и разработке новых лекарственных средств (ЛС) для лечения пациентов, страдающих этим грозным заболеванием [1, 6, 10, 11].
Известно, что ЛС, обладающие антиоксидантным и антигипоксическим действием, способны снижать инсулинорезистентность, значительно ослаблять различные нарушения в организме, в том числе связанные с СД [5, 7, 12].
Бензофурокаин (этилового эфира 5-окси-6-диметиламинометил-2-метил-4-хлорбензо-фуран-3-карбоновой кислоты тартрат) – отечественный препарат, обладает поливалентной фармакодинамикой, включающей такие фармакотерапевтические свойства, как антиоксидантное, антигипоксическое, противовоспалительное, сосудорасширяющее; способен активировать нуклеиновый и энергетический обмен, стимулировать регенеративные процессы в кожных ранах (механического и ожогового генеза), десне (при хроническом генерализованном пародонтите), повышать выживаемость животных при остром панкреатите [2, 8, 9, 13].
Целью работы явилось выявление у бензофурокаина прямого гипогликемического действия.
Материалы и методы исследования
Эксперименты проведены на 55 нелинейных белых мышах-самцах массой 20–26 г.
Для выявления у бензофурокаина гипогликемических свойств использовали модель глюкозо-толерантного теста (ГТТ), описанную А.В. Бузлама и соавт. [4].
Предварительно контрольных и подопытных животных подвергали 12-часовой пищевой депривации, которая сохранялась и в течение 2-часового эксперимента, при этом свободный доступ к воде сохранялся.
Бензофурокаин инъецировали в виде 1 % водного раствора однократно внутрибрюшинно в дозах 5 и 10 мг/кг. В качестве референтного препарата использовали глибенкламид в дозе 0,36 мг/кг (соответствует максимальной суточной дозе для человека, составляющей 25 мг), который вводили в виде 0,01 % суспензии однократно внутрижелудочно при помощи зонда, представляющего собой иглу с напаянной оливой. Оба препарата использовали за 60 мин до воспроизведения ГТТ: 40 % водный раствор глюкозы вводили однократно подкожно в дозе 3 г/кг. Измерение концентрации глюкозы в крови (мМ/л), забор которой осуществляли из хвостовой вены, проводили глюкозооксидазным методом: у подопытных животных 5-кратно до введения глибенкламида и бензофурокаина (исходно), после введения этих препаратов до инъецирования глюкозы (точка отсчета, принимаемая за 0 мин), через 30, 60 и 120 мин после глюкозы. В контроле измерения концентрации глюкозы проводили 4-кратно – натощак, до введения глюкозы (исходно – 0 мин) и спустя 30, 60 и 120 мин после глюкозы.
Вычисляли коэффициент (К) А.А. Покровского [4] – отношение разности максимального и исходного уровней глюкозы в крови к исходному, выраженное в %, по формуле
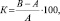
где А – исходный уровень глюкозы, определяемой натощак; В – максимальный уровень глюкозы.
Результаты опытов обрабатывали статистически с вычислением средней арифметической, стандартного отклонения и достоверности различий (t) по критерию Стьюдента [3].
Результаты исследования и их обсуждение
У животных контрольной группы концентрация глюкозы в крови натощак составляла 4,37 ± 0,32 мМ/л. При ГТТ наибольший уровень гликемии наблюдался через 30 мин после введения глюкозы и был равен 11,98 ± 0,71 мМ/л, что статистически значимо, в 2,7 раза (или на 173,9 %), выше исходного уровня. Спустя 60 мин концентрация глюкозы в крови снижалась до 9,49 ± 0,63 мМ/л, что достоверно в 1,3 раза (или на 20,8 %) ниже по отношению к предыдущему измерению концентрации глюкозы и в 2,2 раза (или на 117,2 %) выше исходного уровня. Через 120 мин концентрация глюкозы в крови составляла 5,97 ± 0,47 мМ/л и по сравнению с таковой исходного уровня была достоверно в 1,4 раза (или на 36,6 %) повышенной. Коэффициент А.А. Покровского оказался равным 174,1, что указывает на нарушение толерантности к глюкозе (таблица).
При использовании глибенкламида (0,36 мг/кг) спустя 60 мин после его введения отмечалось статистически значимое в 1,3 раза (или на 24,6 %) снижение гликемии натощак (до 4,45 ± 0,48 мМ/л) по сравнению с исходными значениями (5,90 ± 0,49 мМ/л). В условиях ГТТ спустя 30 мин после введения глюкозы уровень гликемии достоверно в 1,5 раза (или на 46,3 %) был выше исходного (8,63 ± 0,62 мМ/л против 5,90 ± 0,49 мМ/л), что в 1,4 раза (или на 26,3 %) ниже по сравнению с абсолютным значением соответствующего показателя в контроле (8, ± 0,62 мМ/л против 11,98 ± 0,71 мМ/л) или на 147,6 % по сравнению с относительным (по отношению к исходному) значением. Через 60 и 120 мин на фоне действия глибенкламида при сравнении с контрольными данными по абсолютным значениям (6,25 ± 0,42 и 3,87 ± 0,19 мМ/л против 9,49 ± 0,63 и 5,97 ± 0,47 мМ/л) гликемия явилась достоверно в 1,5 и 1,5 раза (или на 34,1 и 35,2 %) меньшей. Коэффициент А.А. Покровского оказался равным 46,3, что свидетельствует об устранении глибенкламидом толерантности к глюкозе.
Бензофурокаин в дозах 5 и 10 мг/кг через 60 мин после инъецирования незначительно снижал (на 18,8 и 15,1 % соответственно) гликемию натощак. При ГТТ через 30 мин после введения глюкозы уровень гликемии статистически достоверно в 1,4 и 1,5 раза (или на 43,5 и 52,9 %) соответственно выше исходного (8,64 ± 0,69 и 7,92 ± 0,39 мМ/л против 6,02 ± 0,47 и 5,18 ± 0,31 мМ/л), что явилось в 1,4 и 1,5 раза (или на 27,9 и 33,9 %) более низким по сравнению с абсолютным значением соответствующего показателя в контроле (8,64 ± 0,69 и 7,92 ± 0,39 мМ/л против 11,98 ± 0,71 мМ/л) или на 146,0 и 140,0 % по сравнению с относительным (по отношению к исходному) значением. Спустя 60 мин на фоне действия бензофурокаина в избранных дозах при сравнении с контролем по абсолютным значениям (7,50 ± 0,70 и 6,50 ± 0,34 мМ/л против 9,49 ± 0,63 мМ/л) гликемия явилась достоверно, в 1,3 и 1,5 раза (или на 21,0 и 31,5 %), меньшей, а через 120 мин – практически не отличалась от контрольной. Коэффициенты А.А. Покровского при использовании бензофурокаина в дозах 5 и 10 мг/кг соответственно равны 43,5 и 52,9, что свидетельствует о снижении этим препаратом толерантности к глюкозе.
Таким образом, бензофурокаин, как и глибенкламид, способен снижать концентрацию глюкозы в крови, однако степень их гипогликемического действия является различной и в большей мере выражена для глибенкламида.
Сравнительная гипогликемическая активность бензофурокаина (5 и 10 мг/кг внутрибрюшинно) и глибенкламида (0,36 мг/кг внутрижелудочно) при ГТТ в опытах на мышах
|
Показатель |
Количество животных |
Концентрация глюкозы в крови, мМ/л, через n мин |
||||
|
исходно |
0 |
30 |
60 |
120 |
||
|
Контроль |
10 |
– |
4,37 ± 0,32 (3,64–5,10) |
11,98 ± 0,71 (10,36–13,60) *р < 0,001 |
9,49 ± 0,63 (8,07–10,91) *р < 0,001 |
5,97 ± 0,47 (4,92–7,02) *р < 0,01 |
|
Разница с исх., % |
– |
– |
+173,9 |
+117,2 |
+36,6 |
|
|
Коэффициент А.А. Покровского |
– |
– |
174,1 |
– |
– |
|
|
Глибенкламид, 0,36 мг/кг |
15 |
5,90 ± 0,49 (4,84–6,96) |
4,45 ± 0,48 (3,43–5,47) *р < 0,05 |
8,63 ± 0,62 (7,29–9,97) *р < 0,002 +р < 0,002 |
6,25 ± 0,42 (5,34–7,16) *р > 0,05 +р < 0,001 |
3,87 ± 0,19 (3,46–4,28) *р < 0,001 +р < 0,001 |
|
Разница с исх., % |
– |
–24,6 |
+46,3 |
+5,9 |
–34,4 |
|
|
Разница с контр., % |
– |
– |
–26,3 |
–34,1 |
–35,2 |
|
|
Коэффициент А.А. Покровского |
46,3 |
|||||
|
Бензофурокаин, 5 мг/кг |
15 |
6,02 ± 0,47 (5,01–7,03) |
4,89 ± 0,35 (4,15–5,63) *р > 0,05 |
8,64 ± 0,69 (7,15–10,13) *р < 0,01 +р < 0,01 |
7,50 ± 0,70 (6,16–8,84) *р > 0,05 +р < 0,05 |
6,77 ± 0,53 (5,63–7,91) *р > 0,05 +р > 0,05 |
|
Разница с исх., % |
– |
–18,8 |
+43,5 |
+24,6 |
+12,5 |
|
|
Разница с контр., % |
– |
– |
–27,9 |
–21,0 |
+13,4 |
|
|
Коэффициент А.А. Покровского |
43,5 |
|||||
|
Бензофурокаин, 10 мг/кг |
15 |
5,18 ± 0,31 (4,52–5,84) |
4,40 ± 0,25 (3,85–4,95) *р > 0,05 |
7,92 ± 0,39 (7,09–8,75) *р < 0,001 +р < 0,001 |
6,50 ± 0,34 (5,77–7,23) *р < 0,01 +р < 0,001 |
5,62 ± 0,32 (4,94¸ 6,30) *р > 0,05 + р > 0,05 |
|
Разница с исх., % |
– |
–15,1 |
+52,9 |
+25,5 |
+ 8,5 |
|
|
Разница с контр., % |
– |
– |
–33,9 |
–31,5 |
-5,9 |
|
|
Коэффициент А.А. Покровского |
52,9 |
|||||
Примечания: 1. Коэффициент А.А. Покровского в норме ≈ 50 % (максимальный – 75 %), выше 80 %, как правило, свидетельствует о нарушении углеводного обмена [4]. 2. В скобках – доверительные границы при р = 0,05.
2. * + Сравнение показателей подопытных групп животных с исходными значениями по группе и контролем соответственно.
Исходя из того, что у интактных животных бензофурокаин не оказывает существенного влияния на уровень гликемии натощак, проявляя статистически значимую активность при ГТТ, выявленное действие скорее следует расценивать как нормогликемическое, нежели гипогликемическое.
Рецензенты:
Тюренков И.Н., д.м.н., профессор, заведующий кафедрой фармакологии и биофармации, ФУВ ГБОУ ВПО ВолгГМУ Минздрава России, г. Волгоград;
Спасов А.А., д.м.н., профессор, зав. кафедрой фармакологии, ГБОУ ВПО ВолгГМУ Минздрава России, г. Волгоград.
Библиографическая ссылка
Бедросова К.А., Галенко-Ярошевский П.А., Попков В.Л., Уваров А.В. СРАВНИТЕЛЬНАЯ ГИПОГЛИКЕМИЧЕСКАЯ АКТИВНОСТЬ БЕНЗОФУРОКАИНА И ГЛИБЕНКЛАМИДА НА МОДЕЛИ ГЛЮКОЗО-ТОЛЕРАНТНОГО ТЕСТА // Фундаментальные исследования. 2015. № 1-4. С. 695-698;URL: https://fundamental-research.ru/ru/article/view?id=37403 (дата обращения: 17.05.2026).



