Известно, что во время длительного сокращения мышцы, регистрируемая механическая сила градуально снижается. Этот феномен, рассматриваемый как «утомление», один из наиболее интригующих явлений, ассоциируемых с сократительной активностью мышцы. Процесс утомления скелетных мышц исследовали в разных экспериментальных условиях и в большинстве случаев определяли, как неспособность поддерживать требуемую или рассчитанную силу «an inability to maintain the required or expected force» [19]), или как точка нарушения «the failure point» [31]). Несмотря на многочисленные исследования, этиология мышечного утомления остается неизвестной [22], а тем более в условиях механической разгрузки мышечного аппарата.
В качестве показателя мышечного утомления широко используют изменения поверхностной электромиограммы (ЭМГ) [21-28]. Однако связь между ЭМГ и утомлением не только нелинейная, но часто изменения в ЭМГ предшествуют утомлению мышцы [27] и интерпретация ЭМГ сигнала затруднена сложностью его происхождения. Параметры ЭМГ во время произвольной активности мышцы являются результатом суммации и «выпадением» отдельных потенциалов действия (ПД) двигательных единиц из числа всех активных двигательных единиц [16]. Известно, что характеристика ЭМГ зависит от паттерн частоты импульсации двигательной единицы и конфигурации ПД [28]. В той связи объективным, легко измеряемым, физиологическим показателем оценки утомления является активность мышцы при электрической стимуляции постоянной частотой. В последнем случае параметры механического ответа не зависят от центрального драйва [14, 23].
Известно, что во время выполнения мышечной работы до утомления отмечается накопление ионов H+ и продуктов метаболитов [38, 39], сдвиг ионной концентрации Na+ и K+ [23]. Такие изменения могут нарушать связь возбуждение-сокращение, включающее свойства мышечной мембраны и генерацию ПД мышцы, ведущих в ЭМГ проявлений утомления мышцы, но отличающееся от механических проявлений [13, 27, 32]. Возможно, это не единственные причины и утомление может иметь место в каждом из перечисленных моментов. Все это указывает не только на связь между неупотреблением и изменением во внутриклеточных механизмах, контролирующих кинетику мышечного сокращения, но и предполагает, что изменение ионной проницаемости мышечной мембраны может существенно влиять на сократительную кинетику мышцы.
Цель настоящего исследования — определить паттерн утомления при ритмическом тетаническом сокращении ТМГ у человека после 7-суток гравитационной разгрузки. Механические и электрические параметры мышцы регистрировали во время электрической стимуляции ее моторного нерва, что позволяло отделить периферический аппарат от центрального управления. Сопоставление изменений в сократительных и электрических ответах этой группы мышц привлекает должное внимание со стороны многих исследователей и, в частности занимающихся проблемой космической физиологии.
МЕТОДИКА
Испытуемые и иммерсионная процедура
Эксперимент был выполнен с участием 6 здоровых мужчин-добровольцев в возрасте между 18 и 40 лет (средний 22.7 ± 3.5), при росте от 168 до 180 см (средний 176.3 ± 0.3) и весом от 64 до 80 кг (средний 66.5 ± 2.3), которые прошли специальный медицинский отбор, базировавшийся на анализе истории болезни, биохимическом анализе крови, анализе электрокардиограммы в покое и при выполнении велоэргометрического нагрузочного теста. Все испытуемые клинически были оценены как здоровые и находились в хорошем физическом состоянии, не употребляли медикаментозных средств и были некурящими и отличались высокой устойчивостью к ортостатической нагрузке и антиортостатическому (наклон головы -6º) положению тела.
Экспериментальные процедуры были выполнены в соответствии с Хельсинской Декларацией и испытуемые после полной информации о процедурах и задачах настоящего исследования дали письменное согласие на участие в нем. Программа исследований была одобрена комиссией по биомедицинской этике при ГНЦ РФ - ИМБП РАН.
Для моделирования механической разгрузки мышечного аппарата использовали модель «сухой» водной иммерсии [10]. Испытуемого помещали в специальную ванну в горизонтальном положении на свободноплавающую высокоэластическую тканевую пленку, отделяющей поверхность тела испытуемого от жидкости - воды. Продолжительность пребывания в таких условиях составляла 7 суток. Температура воды в ванне была постоянной на уровне 33.4 ° C и автоматически поддерживалась на этом уровне в течение всего эксперимента. Испытуемый постоянно оставался в горизонтальном положении, включая выделительные функции и прием пищи. Во время экспозиции испытуемый постоянно находился под медицинским наблюдением на протяжении 24 часов. Обслуживающий медицинский персонал постоянно присутствовал при транспортировании испытуемого, при выполнении личной гигиены, включая туалет и прием пищи, медицинском обслуживании в пределах ограничений протокола.
Функциональные свойства периферического нервно-мышечного аппарата (НМА) оценивали дважды — до и после механической разгрузки, и протокол исследований был идентичным.
Экспериментальная процедура
Работоспособность периферического НМА, на примере ТМГ, у человека в условиях in situ оценивали по крутизне снижения тетанического изометрического сокращения, продуцируемого ТМГ при ее ритмическом тетаническом сокращении. Сокращение мышцы вызывали супрамаксимальными электрическими импульсами, используя монополярный электрод, помещенный накожно в подколенной ямке на область n. tibialis. Утомление исследовали при выполнении 2 мин стандартной серии, состоящей из изометрических ритмических 1 с сокращений, разделенных паузой отдыха той же длительности [5]. Частота стимуляции 50 имп/с, физиологическая частота, с одной стороны, близкая к частоте активации мышечных клеток во время начального развития сильного произвольного сокращения [15], а с другой — позволяет развивать максимальную силу сокращения мышцы [2-4].
Стимуляция
N. tibialis электрически стимулировали прямоугольными супрамаксимальными (+40 %) импульсами длительностью каждого 1 мс, используя монополярный электрод (диаметром 1 см). Активный электрод (катод) устанавливали в подколенной ямке (область наименьшего сопротивления) на моторный нерв, пассивный (размером 6 х 4 см) — на нижней трети передней поверхности бедра. Электрические импульсы подавали от нейромышечного стимулятора (тип ЭСУ-1, СССР) через изолирующую приставку. Использовали одиночные и тетанические ритмические импульсы.
Регистрация механических и электрических ответов
Для регистрации механических ответов отдельной скелетной мышцы использовали метод тендометрии, основанный на физическом законе разложения сил по принципу параллелограмма [2]. Экспериментальная процедура и установка для регистрации электрических ответов и механического ответа отдельной мышцы у человека в условиях in situ в деталях описана ранее [2, 4; см. рис. 1] Коротко, испытуемый удобно располагался в специальном кресле в стандартной позиции - угол в тазобедренном, голеностопном и коленном суставах составлял порядка 90 ° и был постоянным на протяжении всего исследования. Конечность жестко фиксировали, создавая изометрический режим сокращения мышцы. Динамометр, представляющий стальное кольцо, плотно прижимали к Ахиллову сухожилию мышцы. Степень прижатия составляла 5 кГ и визуально контролировалась по шкале часового индикатора, вмонтированного в скобу динамометра, и оставалась постоянной в течение всего периода исследования. Механическая деформация динамометра при сокращении мышцы преобразовывалась в электрические сигналы, и после усиления усилителем (тип АНЧ-7м, СССР) регистрировали на светолучевом осциллографе
(тип К-115, СССР). Динамометр до и после исследования калибровали, нагружая его массой 5 кГ.
Регистрацию электрической активности мышцы, электрический сигнал или поверхностный ПД (ППД), осуществляли поверхностными биполярными AG-AgCl чашечными (8 мм) электродами, расположенными на уровне ниже 6 см головок m. gastrocnemius по средней линии брюшка m. soleus, с межэлектродным расстоянием 25 мм. Положение отводящих электродов подбирали таким образом, чтобы форма электрических ответов мышцы — М-ответов, была наиболее простой. Большой электрод заземления (размером 7.5 х 6.5 см) устанавливали в проксимальной части голени между отводящими и регистрирующими электродами. ППД усиливали усилителем (тип УБП-1-02, СССР), а затем синхронно осуществляли запись на светолучевом осциллографе и, для визуального контроля, на экране запоминающего осциллоскопа (тип С8-9А, СССР).
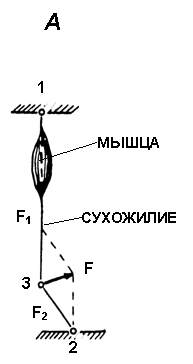
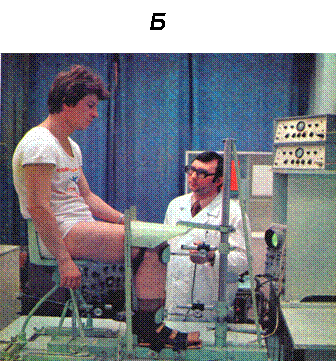
Рис. 1.
А. Схема регистрации силы сокращения скелетной мышцы у человека с помощью тендометрического датчика в условиях in situ.
Б. Тендометрическая установка и позиция человека при регистрации механических и электрических ответов отдельной скелетной мышцы голеностопного сустава.
1 и 2 - точки фиксации звеньев конечности, 3 - точка фиксации динамометра
Регистрацию механических и электрических ответов мышцы во время ритмической тетанической стимуляции осуществляли на протяжении 1 с после начала тетанизации нерва, а затем короткими (около 0.2 с) отрезками в конце каждого сокращения.
Электрические и механические ответы ТМГ регистрировали на специальной ленте светолучевого осциллографа и дополнительно на экране запоминающего осциллографа.
Измерение
По тендограмме изометрического одиночного сокращения мышцы, в ответ на одиночный электрический импульс n. tibialis, измеряли силу (пик амплитуды) одиночного сокращения (Рос), время одиночного сокращения (ВОС) и время полурасслабления (1/2 ПР) мышцы.
Рассчитывали также максимальную скорость (dPoc/dt) развития изометрического одиночного сокращения.
Работоспособность (выносливость) периферического НМА оценивали по показателю индекса утомления (ИУ) -- отношение (в процентах) средней силы 5 последних сокращений в ряду сокращений мышцы к средней силе 5 первых сокращений [5]. Электрическую активность мышцы (m. soleus) оценивали как по амплитуде отдельных электрических ответов -- М-ответов («от пика до пика» [1, 35], так и по амплитуде, длительности и площади негативной фазы М-ответа [7]. Для определения относительной степени изменения сократительных (С) и электрических (Э) ответов мышцы в результате утомления вычисляли Э/С-отношение, где Э -- отношение амплитуды пост-иммерсионного М-ответа к соответствующему до иммерсионного М-ответа, а С -- отношение пост-иммерсионного к соответствующему до иммерсионному механическому ответу ТМГ. Э/С-отношение определяли по показателям Э и С ответов в конце 1, 3, 5, 31, 61, 91 и 121 с от начала тетанизации нерва.
Статистика
При обработке полученных результатов исследования рассчитывали среднюю и стандартную ошибку средней (М ± m). Различие между фоновыми (контрольными) показателями и показателями, зарегистрированными после АНОГ, оценивали с помощью параметрического t-критерия Стьюдента и непараметрического критерия Вилкоксона. Уровень достоверности р < 0.05 признавался как существенный.
РЕЗУЛЬТАТЫ
Утомление и тетаническая сила
Скорость снижения тетанического изометрического напряжения (Ро), развиваемого ТМГ во время электрически вызванного (50 имп/с) ритмического теста на утомление, иллюстрирует рис. 2, А. В этом примере тетаническая сила сокращения мышцы на протяжении 2 мин ритмического теста градуально уменьшается и составляет в среднем 57 % ее исходной величины (р < 0.05). Существенных различий на протяжении всей кривой до и после механической разгрузки мышцы не обнаруживается — ИУ составил 36.2 ± 5.4 и 38.6± 2.8 %, соответственно (р > 0.05).
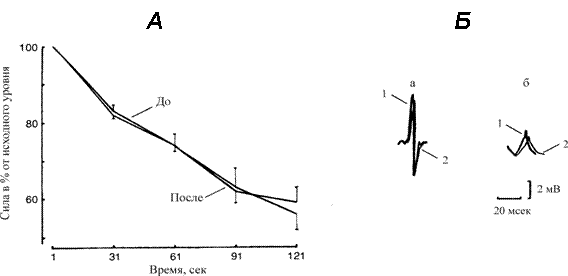
Рис. 2.
А. Изменение силы сокращения трехглавой мышцы голени во время 60 ритмических 1‑с электрически вызванных (50 имп/с) сокращений с 1‑с интервалами отдыха между сокращениями в до и после 7 суточной механической разгрузки. Величины выражены как % от исходной тетанической силы сокращения.
Б. Поверхностный потенциал действия, зарегистрированный в начале (а) и на
60 ритмическом сокращении (б) в контрольных условиях (1) и после разгрузки (2).
Вместе с тем, анализ кривых изменения сократительной активности мышцы обнаружил в основном бифазный характер ответа. При этом каждая последующая фаза характеризуется своей динамикой изменения силы сокращения мышцы. Более быстрое снижение силы сокращения от исходной величины отмечается на 30-31 с (17-18 %) с последующим относительным замедлением к концу 60-61 с (8-9 %) и вновь некоторым возрастанием скорости снижения силы сокращения отмечается к 90-91 с (11-12 %) и с замедлением на последнем участке кривой (3-7 %). Это наблюдение кажется парадоксальным, поскольку хорошо известно, что во время сильных изометрических сокращений механическое напряжение мышцы препятствует внутримышечной циркуляции кровотока и развивается ишемический процесс [20]. Результат предполагает, что эти две фазы утомления обусловлены разными процессами — по возможности чувствительностью к внутримышечному циркулирующему кровотоку.
Интересно, что после механической разгрузки не обнаруживаются различий в кривой снижения мышечного напряжения при выполнении теста на утомление. Наше наблюдение, что развиваемая во время сокращения мышцы ишемия видоизменяет первоначальную фазу соотношения между временем сокращения и уровнем снижения силы, и значительно ослабевает во второй части кривой, допускает, что разные механизмы вовлекаются в двух фазах.
Утомление и электрические процессы
Уменьшение продуцируемой механической силы сокращения может быть результатом снижения электрической активности мышцы. В этой связи мы проанализировали ЭМГ активность мышцы (см. раздел «МЕТОДИКА») и усредненные данные представлены в табл. 1 и графически на рис. 2, Б. Наши результаты показывают, что изменение электрических процессов, наблюдаемых во время выполнения ритмических тестовых сокращений на утомление, различается в контроле и после ее механической разгрузки. После 7-суточной разгрузки мышечного аппарата отмечается уменьшение амплитуды негативной фазы ПД и увеличение длительности М-ответа. По существу эти изменения начинаются с первого М-ответа и возрастают в конце 1, 5 и особенно на 121 с тестового сокращения (табл. 1; рис. 2-Б).
Таблица 1. Электрические свойства мышцы до и после 7-суточной механической разгрузки
|
|
Поверхностный потенциал действия
|
|||||||||
|
Первый |
Время от момента начала электрической стимуляции, с
|
|||||||||
|
1 |
3 |
5 |
121 |
|||||||
|
до |
после |
до |
после |
до |
после |
до |
после |
до |
после |
|
|
А, мв
|
5.2 ± 1.2 |
5.0 ± 0.2 |
8.6 ± 4.2 |
7.6* ± 1.6 |
10.2 ± 5.6 |
8.1** ± 0.8 |
8.8 ± 3.6 |
8.1 ± 0.5 |
3.4 ± 0.4 |
1.6* ± 0.4 |
|
Д, мс
|
6.5 ± 1.5 |
9.7* ± 1.4 |
5.5* ± 0.5 |
6.0* ± 1.0 |
6.0 ± 1.0 |
10.0** ± 3.1 |
6.7* ± 0.3 |
9.7* ± 3.2 |
12.0 ± 2.0 |
17.0** ± 2.0 |
|
П, мв×мс
|
20.0 ± 4.1 |
21.2* ± 4.4 |
30.0 ± 4.7 |
19.4* ± 4.4 |
27.8 ± 11.7 |
38.3** ± 8.1 |
28.8 ± 10.6 |
37.8** ± 9.9 |
20.8 ± 5.8 |
13.6** ± 5.4 |
Примечание: А -- амплитуда поверхностного потенциала действия (ПД);
Д -- длительность негативной фазы ПД;
П -- площадь негативной фазы ПД;
* -- и ** -- уровни достоверности (р < 0.05-0.01, соответственно).
Более детальный анализ динамики изменения электрических процессов мышцы в обоих тестах обнаруживает существенное уменьшение длительности ППД (р < 0.05) в течение первых 3 с при сопутствующем увеличении амплитуды и площади ППД (табл. 1; рис. 3). С этого момента длительность негативной фазы ППД продолжает увеличиваться на всем протяжении ритмического теста на утомление, тогда как временной ход изменения амплитуды и площади ППД разнится — первоначальное их увеличение, наблюдаемое в течение первых 150 и 250 ответов, соответственно, сменяется не только уменьшением до исходного уровня, но и инверсией регистрируемых параметров. Вместе с тем обращает внимание характер расположения кривых. Крутизна (градиент) увеличения или уменьшения регистрируемых электрических ответов мышцы была больше после иммерсии по сравнению с контрольным уровнем.
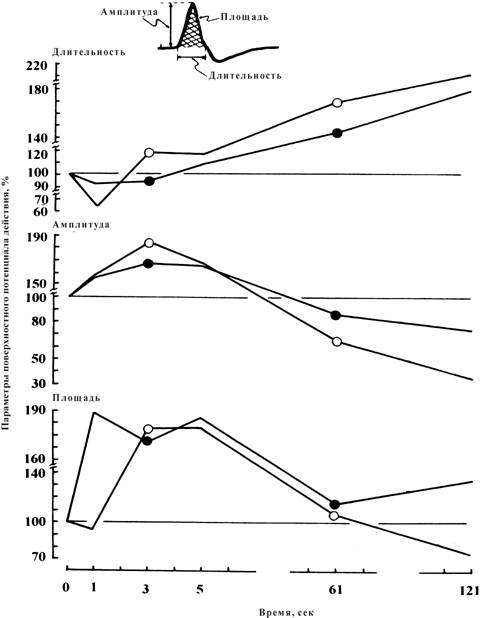
Рис. 3. Динамика изменений параметров поверхностного потенциала действия (ППД) во время 60 ритмических 1-с электрически вызванных сокращений (50 имп/с) с 1-с интервалами отдыха между сокращениями до и после 7 суточной механической разгрузки. Изменения параметров ППД (показано на вставке): длительности (верх), амплитуды (середина) и площади (внизу) выражены как процентное отношение к их контрольной величине.
![]() контроль;
контроль; ![]() после разгрузки.
после разгрузки.
Таким образом, после снятия функциональных требований (запросов) при выполнении дозированной локальной работы до утомления значительно снижается как сила электрически вызванного (тестового) сокращения, так и электрические ответы мышцы. Однако, если после гравитационной разгрузки при выполнении ритмического электрически вызванного теста на утомление не отмечается различий в динамике снижения силы сокращения ТМГ, то существенные различия обнаруживаются в динамике изменений электрических ответов. Относительную степень уменьшения каждого из этих двух показателей можно определить по изменению отношения электрического М-ответа к механическому, сократительному, ответу ТМГ (Э/С‑отношение). Анализ динамики изменений Э/С‑отношения обнаружил значительное различие (рис. 4). Судя по изменению показателя Э/С‑отношения, во время выполнения одинаковой по интенсивности мышечной работы могут возникать неодинаковые изменения в состоянии «сократительных» и «электрогенных» звеньев периферического НМА. Так, после механической разгрузки на протяжении первых 5 с тестового раздражения наблюдается относительно большее уменьшение силы сокращения, чем электрических М-ответов. С увеличением длительности выполняемой работы отмечается относительно большее уменьшение электрических ответов мышцы.
![]()
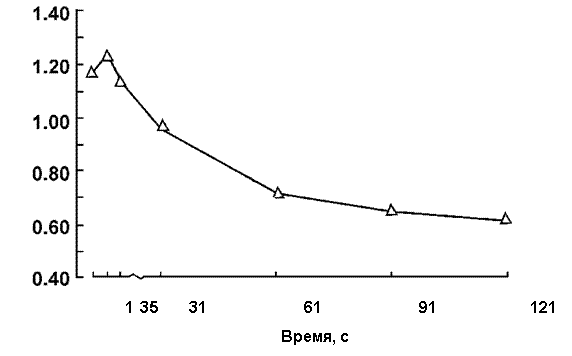
Рис. 4. Изменение отношения электрических ответов мышцы к механическому (Э/М‑отношение) во время 60 ритмических 1‑с электрически вызванных (50 имп/с) сокращений с 1‑с интервалом отдыха между сокращениями после 7 суточной механической разгрузки.
Утомление и сопряжение возбуждение-сокращение
Экспериментальные данные, сообщенные в разделе «Утомление и электрические процессы», указывают, что во время ритмических сокращений снижается электрически вызванная тетаническая сила и изменяются электрические процессы, являющиеся триггерами сокращения мышцы. Это допускает, что некоторые этапы процесса связи возбуждение-сокращение мышцы могут вызываться ионными процессами вне мембраны во время выполнения теста на утомление.
Сопряжение возбуждение-сокращение может быть экспериментально исследовано в условиях in situ у человека при одновременной регистрации Рoc и соответствующего электрического ответа — ППД мышцы в ответ на одиночный супрамаксимальный электрический импульс короткой длительности (табл. 2). Сравнение параметров ППД до и после 7-суточной иммерсии обнаруживает существенное различие (табл. 2). Исследования механических ответов мышцы указывают, что при неизменной Рoc и ВОС (р > 0.05) мышцы, существенно уменьшается dPос/dt и 1/2 ПР (р < 0.05). Электромеханическая диссоциация предполагает, что механические изменения не тесно связаны с периферическими электрическими изменениями и некоторые ступени ионных процессов связи возбуждение-сокращение мышцы могут быть изменены вне мембраны.
Таблица 2. Параметры одиночного изометрического сокращения и потенциала действия мышцы до и после 7-суточной механической разгрузки
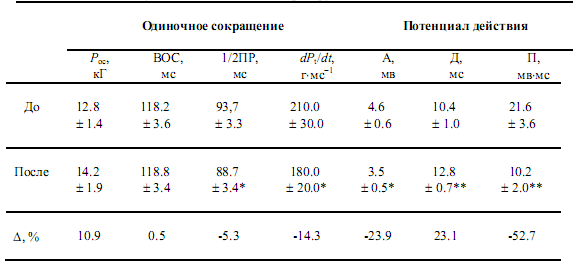
Примечание: Рос — сила одиночного сокращения; ВОС — время одиночного сокращения;
1/2 ПР -- время полурасслабления; dPt/dt — максимальная скорость развития напряжения; А —амплитуда поверхностного потенциала действия (ПД);
Д — длительность негативной фазы ПД; П — площадь негативной фазы ПД;
* — и ** — уровни достоверности (p < 0.05-0.01, соответственно).
ОБСУЖДЕНИЕ
Механическое ослабление (утомление) во время сокращения мышцы является одним из наиболее интригующих физиологических феноменов мышечной работоспособности. Настоящая работа является вкладом в дискуссию этой проблемы. Рассматривается специфическое влияние ритмического сокращения мышцы посредством электрической стимуляции ее моторного нерва в условиях in situ после снятия функциональных требований. Возможность влияния центральной (моторной) команды во время выполнения теста на утомление была исключена нашей экспериментальной процедурой (см. раздел «МЕТОДИКА»).
Полученные данные показывают, во-первых, что скорость снижения силы сокращения мышцы во время ритмической стимуляции на утомление не различается в контроле и после неупотребления, во-вторых, во время стимуляции ППД, зарегистрированные с помощью поверхностных электродов, показывают заметное снижение амплитуды и увеличение длительности, предполагая наличие нарушений в процессе периферической генерации ПД мышечными волокнами и, в-третьих, сопоставление электрических и механических ответов мышцы (Э/С‑отношение) показывает, что удельная роль утомления «электрогенного» и «сократительного» звеньев НМА изменяется в процессе развития периферического утомления.
Наши результаты (см. рис. 2, A) не обнаруживают различий в снижении работоспособности периферического НМА до и после механической разгрузки, что хорошо согласуется с ранее полученными данными [36, 37] и поддерживают точку зрения Merton [29], что периферические механизмы играют важную роль в снижении силы мышечного сокращения. Периферическое утомление вероятно результат ослабления в возбудимости скелетных мышечных волокон. Ослабление генерации ПД может происходить вдоль терминалей веточек моторного нерва (21), в синаптическом соединении [21] и вдоль мембраны мышечного волокна [8, 11, 14, 25].
Интегральным показателем состояния «электрогенного» звена НМА может быть величина (амплитуда и площадь) регистрируемого ППД. Следует отметить, что снижение амплитуды тестовых М-ответов может быть следствием усиления десинхронизации вызванных ПД мышечных волокон утомленной мышцы, что само по себе не указывает о блоке в нервно-мышечной синаптической передачи и/или нарушений в процессе генерации ПД мышечными волокнами. Уменьшение в площади М-ответов в ритмическом ряду указывает на истинное снижение электрической активности мышцы.
Сравнение между электрическим и механическим нарушением, наблюдаемое во время выполнения ритмических тестовых изометрических сокращений мышцы на утомление, крайне интересно, поскольку идентичное уменьшение силы тетанического сокращения до и после функциональной разгрузки (см. рис. 2, A) сопровождается комплексом электрических изменений (см. рис. 2, Б; рис. 3). Эти результаты допускают, что электрические изменения недостаточно тесно контролируют механические нарушения и, что процессы локализации вне мышечной мембраны играют, по-видимому, преобладающую роль в наблюдаемом ослаблении сокращения.
Регистрация изменений ППД во время утомления показывает, что на периферическом уровне могут быть вовлечены различные электрические механизмы. Сравнение между контролем и после функциональной разгрузки указывает, что нарушения электрических процессов были различными в обоих тестах. Согласно нашим экспериментальным данным (табл. 1; рис. 3) в течение первых секунд сокращения длительность ППД уменьшается в обоих тестах при соответствующем увеличении амплитуды и площади негативной фазы. Это доказывает, что пресинаптический и/или потенциал концевой пластинки был облегчен и, что дисперсия ПД между волокнами была снижена [17, 18]. Последующее увеличение длительности и площади ППД, наблюдаемое в пределах существенного снижения амплитуды ППД, могло быть, главным образом, благодаря замедлению скорости генерации ПД вдоль мембраны мышечного волокна [8, 9, 14, 30], так что конфигурация ППД мышцы приобретает расширенную форму (см. рис. 2, Б;).
Во второй половине ритмического сокращения уменьшение амплитуды ППД предполагает, что пресинаптическая и/или концевая пластинка теперь была повреждена присутствием утомления. Это предположение согласуется с полученными данными, что площадь ППД, которая предварительно обнаруживала тенденцию к увеличению, теперь начинает уменьшаться, хотя длительность ППД продолжает увеличиваться на всем протяжении теста. Это также согласуется с ранее полученными данными, что время проведения тока через концевую пластинку было уменьшенным после разгрузки [8, 33], несмотря на идентичное ослабление в скорости развития силы сокращения. Разное поведение между нервной и мышечной мембранами не является сюрпризом, поскольку их архитектура совершенно разнится и восстановление ионной концентрации может быть замедленной в связи наличия Т (тубулярной) поперечной системы по сравнению с нервной мембраной. Наличие Т (поперечной) тубулярной системы поддерживает предположение о важности роли в мышце электрического утомления [12, 25].
Исследование связи возбуждение-сокращение мышцы достигается при сравнении параметров одиночного ППД и соответственно Рос, свидетельствует о электромеханической диссоциации возбуждение-сокращение. Это является важным аргументом, указывающим, во-первых, что механическое ослабление не только не тесно связано с периферическими электрическими изменениями, а, во-вторых, что электрические и механические изменения в разгруженной мышце отражают периферическую природу. Наблюдаемое в нашем исследовании замедление ППД после разгрузки, ассоциируемое с уменьшением амплитуды и площади, по-видимому, можно объяснить замедлением скорости проведения вдоль мембраны мышечной клетки в разгруженной мышце (по крайней мере, по медленным волокнам [8]) и/или ослаблением концевой пластинки. Замедление времени развития ППД не связано с уменьшением dPос/dt и/или с уменьшением Рос, предполагает, что механические изменения не тесно контролируются ионными процессами периферической мембраны и, таким образом, поддерживают предположение, что внутриклеточные процессы мышцы играют доминирующую роль. Изменение в конфигурации ППД ассоциируется с уменьшением внеклеточной концентрации Na+, увеличением концентрации K+ и концентрацией ионов H+ мышечных волокон [14, 23, 26]. Последняя позволяет предположить, что энергетический метаболизм мышцы играет важную роль в регуляции возбудимости мембраны мышцы. Дополнительным фактором усиления экскреции электролитов может быть сама функциональная разгрузка, нарушающая электролитный гомеостаз (37) и, таким образом, снижающая возбудимость мышечной мембраны [8, 19, 27, 23]. Наша поверхностная ЭМГ (параметры ее представлены в тексте) сильно поддерживает это предположение.
Как показывают наши данные, снижение силы сокращения мышцы в тесте на утомление не отличалось в контроле и после разгрузки, указывая, с одной стороны, что развиваемое утомление нельзя объяснить изменениями в самом сократительном звене НМА в результате гравитационной разгрузки и, во-вторых, что одним из компонентов (если не единственной причиной), развивающегося периферического утомления может быть нарушение в «электрогенном» звене НМА. Сопоставление изменений сократительного ответа с соответствующим изменением электрического ответа (Э/С-отношение) позволяет определить удельную роль «электрогенного» и сократительного звеньев в развитии периферического утомления. Анализ Э/С-отношения до и после разгрузки обнаружил, что возникает неодинаковая динамика изменений в состоянии сократительного и электрического звеньев периферического НМА (см. рис. 4). Эти результаты не противоречат вышеописанной дискуссии, поскольку трактовка Э/С‑отношения предполагает линейную связь между величиной электрического и механического ответов мышцы. Однако, последняя имеет нелинейную связь [27], и особенно при утомлении может нарушаться. При вызванном сокращении, триггером которого является электрическая стимуляция моторного нерва, уменьшение силы мышечного волокна может компенсироваться модуляцией частоты разряда двигательных единиц, не оказывая существенного влияния на силу тетанического сокращения мышечного волокна [40]. Кроме того, нормальный ПД мышечного волокна в несколько раз превышает пороговую величину, необходимую для активации сократительного аппарата [34], в результате даже уменьшенные ПД способны запускать нормальное сокращение мышечных волокон.
ЗАКЛЮЧЕНИЕ
Утомление, развивающееся при выполнении упражнений короткой длительности (как в настоящем исследовании) и, проявляющееся в снижение тетанической силы сокращения мышцы, является следствием изменений периферического НМА. Исследование электрически вызванного сокращения вносит существенный вклад в понимание основных механизмов периферического утомления НМА, поскольку позволяет исключить влияние модуляции частоты импульсации моторных, двигательных, единиц на регистрируемые параметры механических ответов мышцы.
Результаты настоящего исследования показывают, что механическое ослабление изометрического напряжения во время ритмических мышечных сокращений определяется периферическими факторами и механизмы ассоциируются с мембраной и внутриклеточными процессами. Сравнение снижения электрических ответов и механического ответа во время ритмических электрически вызванных сокращений в обоих тестовых сокращениях указывает, что замедление генерации ПД вдоль нервной и мышечной мембран, также как и возможно увеличение синаптической задержки, не объясняет ослабления развиваемого напряжения. Сравнение электрических и механических ответов, зарегистрированных в контрольных условиях и после гравитационной разгрузки, поддерживает предположение, что электрические изменения не тесно контролируют механическое ослабление. Таким образом, нервно-мышечные изменения, наблюдаемые во время выполнения короткой длительности упражнений, внутриклеточные процессы могут играть доминирующую роль в отношении наблюдаемого снижения силы сокращения во время выполнения дозированного теста на утомление после функциональной разгрузки.
Благодарность
Автор выражает искреннюю благодарность всем врачам клинотдела ГНЦ РФ - ИМБП РАН (зав. отделом Ю.И. Воронков) и лично Е.И. Доброквашиной за участие в отборе испытуемых.
Автор выражает также особую благодарность и признательность всем испытуемым, принявшим участие в эксперименте, без которых невозможно было бы получить фактический материал.
СПИСОК ЛИТЕРАТУРЫ:
- БадалянЛ.О., СкворцовИ.А. Клиническая электромиография. М. Медицина. - 1986. С. 386.
- КорякЮ.А. Методы исследования нервно-мышечного аппарата у спортсменов. М. ИМБП. - 1992. С. 63.
- КорякЮ.А. Сравнение сократительных свойств мышц нижних конечностей у человека. // Физиол. ж. - 1994. - Т. 40. С. 30-38.
- КорякЮ.А. Функциональные свойства нервно‑мышечного аппарата человека при повышенной и пониженной нагрузке. // Докт. дисс. ГНЦ РФ - ИМБП РАН. М. 2006.
- КорякЮ.А., ПоляковВ.В., ПоцепаевА.И., МартьяновВ.А. Исследование динамической работоспособности периферического нервно-мышечного аппарата спортсменов. // Физиол. основы управления движениями. (КоробковА.В., ред.). М. - 1975. С. 73-74.
- НосковВ.Б., КозыревскаяГ.И., МоруковБ.В., АртамасоваЕ.М., РустамьянЛ.А. Положение тела при гипокинезии и водно-солевой обмен. // Косм. биол. и авиакосм. мед. - 1985. - Т. 19. С. 31-33.
- СкворцовИ.А. Электронейромиография. Методика. Динамика показаний в онтогенезе. // Клинико-электронейромышечное изучение нервно-мышечных заболеваний и синдромов. (БадалянЛ.О., СкворцовИ.А., ред.). М. - 1981. C. 37-71.
- ХристоваЛ.Г., ГидиковА.А., АслановаИ.Ф., КиренскаяА.В., КозловаВ.Г., КозловскаяИ.Б. Влияние иммерсионной гипокинезии на некоторые параметры мышечных потенциалов человека. // Косм. биол. и авиакосм. мед. - 1986. - Т. 20.
С. 27-31. - ХристоваЛ.Г., ГидиковА.А., АслановаИ.Ф., БеляеваМ.Г., КиренскаяА.В., КозловаВ.Г., КозловскаяИ.Б. Влияние иммерсионной гипокинезии на потенциалы двигательных единиц мускулатуры человека. // Косм. биол. и авиакосм. мед. - 1988. - Т. 22. С. 39-43.
- ШульженкоЕ.В., Виль-ВильямсИ.Ф. Возможность проведения длительной водной иммерсии методом «сухого» погружения. // Косм. биол. и авиакосм. мед. - 1976. - Т. 10, С. 82-84.
- BezanlillaF., CaputoC., Gonzalez-SerratosH., VenosaR.S. Sodium dependence of the inward spread of activation in isolated twitch muscle fibers of the frog. // J. Physiol. - 1972. - V. 223. P. 507-523.
- BianchiC.P., NarayonS. Muscle fatigue and the role of transverse tubules. // Science. - 1982. - V. 215. P. 295-296.
- Bigland-RitchieB.R. EMG/force relations and fatigue of human voluntary contraction. // Exer. Sport Sci. Rev. - 1981. - V. 9. P. 75-117.
- Bigland-RitchieB.R., JonesD.A., WoodsJ.J. Excitation frequency and muscle fatigue: electrical responses during human voluntary and stimulated contraction. // Exp. Neurol. - 1979. - V. 64. P. 414-427.
- Bigland-RitchieB.R., JohanssonR., LippoldO.C.J., SmithS., WoodsJ.J. Changes in motoneurone firing rates during sustained maximal voluntary contractions. // J. Physiol. - 1983. - V. 340. P. 335-346.
- DeLucaC.J. Physiology and mathematics of myoelectric signals. // IEEE Trans. Biomed. -1979. - P. 313-325.
- DesmedtJ.E. Methodes d¢etute de la fonction neuromusculaire chez l¢homme: myoframme isometrique, electromyogramme d¢excitation et topographie de l¢innervation terminale. // Acta Neurol. Psychiatr. Belg. - 1958. - V. 58. P. 977-1017.
- DesmedtJ.E., EmerykB., RenoirteP., HainautK. Disorder of contraction processes in sex-linked (Duchenne) muscular dystrophy, with correlative electromyographic study of myopathic involvement in small hand muscles. // Amer. J. Med. - 1968.- V. 45. P. 853-872.
- EdwardsR.H.T. Human muscle function and fatigue. // Human Fatigue: Physiological Mechanisms. (Porter R., Whelan J., eds.). London. Pitman Medical. - 1981. P. 1-18.
- EdwardsR.H.T., HillD.K., MacDonnellM. Myothermal and intermuscular pressure measurement during isometric contractions of the human quadriceps muscle. // J. Physiol. -1972. - V. 224. P. 58P-59P.
- EdwardsR.H.T., LippoldO.C.J. The relationship between tension and intergrated electrical activity in fatigue muscle. // J. Physiol. - 1956. - V. 132. P. 677-681.
- FittsR.H., CourtrightJ.B., KimD.H., WitzmannF.A. Muscle fatigue with prolonged exercise: contractile and biochemical alterations. // Amer. J. Physiol. -1982. - V. 242. P. C65-C73.
- JonesD.A., Bigland-RitchieB.R., EdwardsR.H.T. Excitation frequency and muscle fatigue: mechanical responses during voluntary and stimulated contractions. // Exp Neurol. - 1979. - V. 64. P. 401-413.
- KoryakYu. Contractile properties of the human triceps surae muscle during simulated weightlessness. // Eur. J. Appl. Physiol. - 1995. - V. 70. P. 344-350.
- KrnjevicK., MilediR. Failure of neuromuscular propagation in rats. // J. Physiol. - 1958. - V. 140. P. 440-461.
- LannergenJ., WesterbledH. Action potential fatigue in single skeletal muscle fibres of Xenopus. // Acta Physiol. Scand. - 1982. - V. 129. P. 311-318.
- LindstromL., KadeforsR., PetersenI. An electromyographic index for localized muscle fatigue. // J. Appl. Physiol. - 1977. - V. 43. P. 750-754.
- LindstromJ., MagnussonR.T. Interpretation of myoelectric power spectra: a model and its applications. // Proc. IEEE. - 1977. - V. 65. P. 653-662.
- MertonP.A. Voluntary strength and fatigue. // J. Physiol. - 1954. - V. 123. P. 553-564.
- Milner-BrownH.S., MillerR.G. Muscle membrane excitation and impulse propagation velocity are reduced during muscle fatigue. // Muscle & Nerve. - 1986. - V. 9. P. 367-374.
- MoritaniT., NagataA., DeVriesH., MuroM. Critical power as a measure of physical work capacity and anaerobic threshold. // Ergonomics. - 1981. - V. 24. P. 339-350.
- MoritaniT., MuroM., NagataA. Intramuscular and fatigue surface electromyogram changes during fatigue. // J. Appl. Physiol. - 1986. - V. 60. P. 1179-1185.
- RuzzierF., GregorioF., ScukaM. On the changes of the time course of the end-plate current during repetitive stimulation. // Pflüg. Arch. - 1982. - V. 393. P. 121-132.
- SandowA. Excitation-contraction coupling in skeletal muscle. // Pharmacol. Rev. - 1965. - V. 17. P. 265-320.
- SicaR.E.P., McComasA.J. An electrophysiological investigation of limb-girdle and facioscapulohumeral dystrophy. // J. Neurol. Neurosurg. Psychiat. - 1971. - V. 34. P. 469-474.
- St.-PierreD., GardinerP.F. Effect of "disuse" on mammalian fast-twitch muscle: joint fixation compared with neurally applied to tetrodotoxin. // Exp. Neurol. - 1985. - V. 90. P. 635-651.
- WhiteM.J., DaviesC.T.M. The effects of immobilization, after lower leg fracture, on the contractile properties of human triceps surae. // Clin. Sci. - 1984. - V. 66. P. 277-282.
- WilkieD.R. Muscular fatigue: effects of hydrogen ions and inorganic phosphate. // Federation Proc. - 1986. - V. 45. P. 2921-2923.
- WitzmannF.A., KimD.H., FittsR.H. Effect of hindlimb immobilization on the fatigability of skeletal muscle. // J. Appl. Physiol. - 1983. - V. 53. P. 1242-1248.
- WoodsF.F., FarbusF., Bigland-RitchieB.R. Evidence for a fatigue-induced reflex inhibition of motoneuronen firing rates. // J. Neurophysiol. - 1987. - V. 58. P. 125-137.
Библиографическая ссылка
Коряк Ю.А. НЕЙРОМЫШЕЧНЫЕ ИЗМЕНЕНИЯ ПОД ВЛИЯНИЕМ СЕМИСУТОЧНОЙ МЕХАНИЧЕСКОЙ РАЗГРУЗКИ МЫШЕЧНОГО АППАРАТА У ЧЕЛОВЕКА // Фундаментальные исследования. 2008. № 9. С. 8-21;URL: https://fundamental-research.ru/ru/article/view?id=3696 (дата обращения: 16.05.2026).



