Кадмий – один из самых токсичных тяжелых металлов, поступающий в окружающую среду с отходами металлургии цинка, с выхлопными газами автомобилей, при производстве красок и электротехнической продукции, с фосфорными удобрениями и фунгицидами. Табак интенсивно аккумулирует кадмий – одна сигарета содержит 1,2–2,5 мкг кадмия. Опасность загрязнения кадмием усиливается вследствие большой подвижности и доступности металла для растений, которые могут накапливать кадмий даже при незначительном загрязнении [1, 15]. По фитотоксичности и способности накапливаться в растениях в ряду тяжелых металлов он занимает первое место (Cd > Cu > Zn > Pb) [6]. Воздействие кадмия на растения обусловлено его способностью замещать цинк в активных центрах металлсодержащих ферментов, что приводит к нарушению биохимических процессов. Фитотоксичность кадмия проявляется в торможении фотосинтеза, нарушении водного обмена, изменении проницаемости клеточных мембран [11].
Известно, что гуминовые вещества снижают токсичность тяжелых металлов, связывая ионы металлов в прочные комплексы и выполняя тем самым роль естественных детоксикантов [5, 10, 13]. По снижению интенсивности аккумуляции в гумусе почв металлы располагаются в следующий ряд – Cu > Cd > Pb = Co > Ni > Zn > Mn. Установлено, что действие гуминовых веществ приводит к образованию хелатных соединений и снижению токсичности этих тяжелых металлов [6, 14].
Гуминовые вещества – специфическая группа высокомолекулярных соединений, которые образуются из органических остатков при затрудненном доступе кислорода. Их содержание в морских водах 0,1–3 мг/л, в речных – 20 мг/л, в болотах – до 200 мг/л, в почвах – 1–12 % [9]. Гуминовые вещества составляют основную часть каустобиолитов – горючих сланцев, ископаемых углей, торфа. Важнейшей, наиболее реакционноспособной частью гуминовых веществ являются гумусовые кислоты (ГК) – гуминовые и фульвокислоты. Макромолекулы ГК состоят из упорядоченного конденсированного ядра и неупорядоченной периферийной части, включающей полисахаридно-полипептидные фрагменты. При ядре и боковых цепях макромолекул ГК находятся способные к диссоциации кислотные и основные группы, придающие этим соединениям свойства полиэлектролитов. ГК являются аккумуляторами АК, углеводов, пигментов, биологически активных веществ, лигнина, макро- и микроэлементов [7, 8]. В естественном состоянии гуминовые вещества малоактивны и практически полностью находятся в нерастворимой форме. Физиологически активными являются соли ГК со щелочными металлами – гуматы, которые производят из углей, торфа, сапропелей.
Таким образом, в условиях роста загрязнения окружающей среды тяжелыми металлами особую актуальность приобретает изучение фитопротекторных свойств гуматов. В связи с этим целью исследований являлось изучение влияния гумата, полученного из торфа [2], на устойчивость растений пшеницы к высоким концентрациям кадмия.
Материалы и методы исследования
Объектами исследования были растения яровой пшеницы (Triticum aestivum L.) сорта Приокская. Семена проращивали в чашках Петри на фильтровальной бумаге с растворами сульфата кадмия в концентрациях 25, 50, 100, 250, 500 и 1000 мкМ при температуре 20–22 С. Растения выращивали в условиях водной культуры на питательной смеси Хогланда в камере искусственного климата. Гуминовый препарат использовали в концентрации 0,01 и 0,005 % для проращивания семян и для выращивания растений соответственно. Концентрации выбраны по результатам ранее проведенных экспериментов [3]. Реакцию растений на действие ионов металлов и гумата оценивали по всхожести семян, морфологическим показателям проростков на седьмой день эксперимента, а также по накоплению биомассы и морфологическим показателям развития растений в фазы кущения, выхода в трубку и колошения. Контролем служили растения, выращенные без сульфата кадмия в среде. Степень устойчивости определяли по соотношению сухих масс надземных органов растений на опытном и контрольном вариантах [12]. За показатель тканевой суккулентности принимали соотношение сырой и сухой массы растений. Рассчитывали коэффициент протекторного действия гумата:
1) по накоплению массы растениями – определяли соотношение массы растений, выращенных при использовании гуминового препарата и без гумата (коэффициент протекторного действия гумата по массе) [4];
2) по накоплению токсичного иона – определяли соотношение содержания кадмия в растениях, выращенных без гумата и при использовании гумата (коэффициент протекторного действия гумата по накоплению кадмия).
Содержание ионов кадмия в растениях определяли на атомно-абсорбционном спектрометре «Shimadzu» (Япония), модель 6800. Анализ проводили в фазу колошения (для контрольных растений) на растениях, выращенных при 25 и 50 мкМ сульфата кадмия в среде. При более высоких концентрациях растения практически останавливались в росте, не накапливали массу и выполнить анализ достоверно не представлялось возможным.
Статистическую обработку данных проводили при помощи программы Excel с использованием дисперсионного и корреляционного методов анализа.
Результаты исследования и их обсуждение
Кадмий существенно снизил длину побегов и корней проростков пшеницы во всех вариантах опыта. Причем степень торможения роста проростков усиливалась с увеличением концентрации сульфата кадмия – коэффициент корреляции составил –0,82 и –0,81 для побегов и корней соответственно. Фитопротекторное действие гумата в большей степени было направлено на длину корней, чем побегов. Так, при 25 мкМ сульфата кадмия в среде гумат снизил токсическое действие кадмия в 1,1 и 1,3 раза, при 1000 мкМ – в 1,6 и 2,2 раза для побегов и корней соответственно. Соотношение побеги/корни увеличилось с ростом концентрации кадмия, что свидетельствует о более сильном подавлении роста корней. Для этого показателя установлен высокий коэффициент корреляции – 0,97 без гумата и 0,88 в присутствии гумата.
Достоверное снижение массы растений наблюдалось на всех вариантах опыта. Особенно сильное торможение роста начиналось с концентрации сульфата кадмия 50 мкМ – растения практически останавливались в росте. Так, масса одного растения в фазу кущения (для контрольных растений) составила 0,05 ± 0,01 г, в фазу колошения – 0,09 ± 0,01 г. Степень металлоустойчивости растений значительно снизилась с увеличением концентрации кадмия в среде (табл. 1). В процессе развития растений их устойчивость повысилась только при 25 мкМ, при более высоких концентрациях наблюдалось снижение этого показателя. При 1000 мкМ растения были убраны в фазу кущения, в связи с их гибелью, при 500 мкМ – в фазу выхода в трубку. Гумат достоверно повысил металлоустойчивость растений только при 25 мкМ.
Кадмий существенно снизил как накопление биомассы, так и линейный рост растений на всех вариантах опыта (рисунок). В фазу кущения протекторная роль гумата проявилась при 25, 50 и 100 мкМ. При более высоких концентрациях токсическое действие кадмия на высоту растений усиливалось в присутствии гумата, тогда как защитное действие гумата на корневую систему растений сохранялось.
Таблица 1
Степень металлоустойчивости растений пшеницы (%)
|
Концентрация CdSO4, мкМ |
Без гумата |
С гуматом |
||||
|
Кущение |
Выход в трубку |
Колошение |
Кущение |
Выход в трубку |
Колошение |
|
|
1. 25 |
12,0 |
17,33 |
26,15 |
21,33 |
20,33 |
44,83 |
|
2. 50 |
6,67 |
2,33 |
2,59 |
12,00 |
6,67 |
7,76 |
|
3. 100 |
5,33 |
2,00 |
2,30 |
6,67 |
2,00 |
2,30 |
|
4. 250 |
5,33 |
1,67 |
2,01 |
5,33 |
1,67 |
1,72 |
|
5. 500 |
2,67 |
1,00 |
– |
1,33 |
0,67 |
– |
|
6. 1000 |
2,67 |
– |
– |
1,33 |
– |
– |
Примечание. *Фазы развития указаны для контрольных растений.
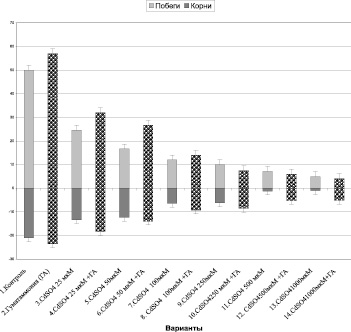
Влияние кадмия на линейный рост растений пшеницы (кущение). Бары на диаграмме показывают значения НСР05
Эффективность гумата характеризует коэффициент протекторного действия (табл. 2). Если коэффициент равен 1 – влияние гумата отсутствует, если значение коэффициента меньше 1 – гумат усиливет токсическое действие металла, если больше 1 – наблюдается выраженный защитный эффект гумата. Стимулирующее действие гумата наблюдалось и без добавления сульфата меди в среду. Коэффициент протекторного действия гумата был высоким при 25 и 50 мкМ, однако при 50 мкМ эффект гумата не доказан статистически. При 500 и 1000 мкМ проявилась тенденция усиления токсического действия кадмия в присутствии гумата.
Для характеристики оводненности тканей использовали показатель тканевой суккулентности. Суккулентность снижалась с увеличением концентрации сульфата кадмия. Так, в фазу кущения этот показатель снизился с 5,24 на контроле до 1,5 при 1000 мкМ, в фазу колошения – с 6,01 на контроле до 2,67 при 500 мкМ CdSO4. Гумат положительно влиял на водный обмен растений в условиях стрессового воздействия высокими концентрациями кадмия. Так, в фазу колошения показатель суккулентности при 25 мкМ составил 9,97 без гумата и 12,5 в присутствии гумата, при 50 мкМ – 2,56 и 4,56, при 100 мкМ – 3,12 и 4,38, при 250 мкМ – 3,29 и 3,50 соответственно.
Таблица 2
Коэффициент протекторного действия гумата (по массе)
|
Концентрация CdSO4, мкМ |
Кущение |
Выход в трубку |
Колошение |
|
1. 0 |
1,35 |
1,44 |
1,38 |
|
2. 25 |
1,78 |
1,17 |
1,71 |
|
3. 50 |
1,80 |
2,86 |
3,00 |
|
4. 100 |
1,25 |
1,00 |
1,00 |
|
5. 250 |
1,00 |
1,00 |
0,86 |
|
6. 500 |
0,50 |
0,67 |
– |
|
7. 1000 |
0,50 |
– |
– |
Все изученные концентрации сульфата кадмия вызвали торможение процесса кущения растений. Защитный эффект гумата проявился только в среде без кадмия и при 25 мкМ CdSO4 – гумат усилил побегообразование растений в 1,2 и 1,8 раза соответственно.
Пшеница накапливала кадмий преимущественно в корневой системе, что характерно для растений ‒ исключателей токсичных ионов и подтверждает регулирующую функцию корневой системы, не допускающую избыточного накопления токсичных ионов в побегах (табл. 3). Но при повышении концентрации сульфата кадмия процессы регуляции нарушаются. О регулирующей функции корневой системы можно судить по соотношению содержания токсичных ионов в корнях и побегах. Наиболее высокая регулирующая способность корневой системы наблюдалась при 25 мкМ. При 50 мкМ возросла регулирующая роль корней в присутствии гумата.
Таблица 3
Содержание кадмия в растениях, мг/кг сухой массы (колошение)
|
Концентрация CuSO4, мкМ/л |
Без гумата |
С гуматом |
||||
|
Побеги |
Корни |
Корни/побеги |
Побеги |
Корни |
Корни/побеги |
|
|
1. 0 |
9,5 ± 0,3 |
3,6 ± 0,1 |
0,38 |
9,8 ± 0,2 |
4,0 ± 0,5 |
0,41 |
|
2. 25 |
33,0 ± 2,0 |
630,0 ± 2,0 |
19,09 |
21,0 ± 1,0 |
260,0 ± 15,0 |
12,38 |
|
3. 50 |
83,0 ± 3,0 |
910,0 ± 20,0 |
10,96 |
96,0 ± 1,0 |
2260,0 ± 80,0 |
23,54 |
Таблица 4
Коэффициент протекторного действия гумата (по содержанию кадмия)
|
Концентрация CdSO4, мкМ/л |
Побеги |
Корни |
|
1. 0 |
0,97 |
0,90 |
|
2. 25 |
1,57 |
2,42 |
|
3. 50 |
0,86 |
0,40 |
Протекторное действие гумата на накопление ионов кадмия (табл. 4) наблюдается только при 25 мкМ CdSO4 – гумат снизил содержание кадмия в побегах в 1,5 раза, в корнях – более, чем в 2 раза. При 50 мкМ гумат усилил накопление кадмия растениями пшеницы, особенно в корнях – в 2,5 раза. Очевидно, что защитная функция гумата, заключающаяся в снижении накопления токсичного иона в растениях, ограничивается высокими концентрациями кадмия в среде.
Заключение
Таким образом, при изучении воздействия высокими концентрациями кадмия на растения пшеницы подтверждена его высокая фитотоксичность – только при 25 мкМ CdSO4 растения смогли пройти все фазы развития, снижая массу на 26 % к фазе колошения. Степень металлоустойчивости этих растений повысилась в процессе их развития с 12,0 до 26,2 % в фазы кущения и колошения соответственно. Высокая регулирующая функция корневой системы растений наблюдалась также при 25 мкМ – соотношение содержания кадмия в корнях и побегах составило 19, тогда как при 50 мкМ – 11.
Протекторная роль гумата наблюдалась только при концентрации сульфата кадмия 25 мкМ – степень металлоустойчивости растений повысилась в фазу кущения на 9 %, в фазу колошения – на 19 % по сравнению с растениями, выращенными без гумата. Защитная роль гумата обусловлена снижением накопления токсичного иона в растениях – при 25 мкМ в присутствии гумата содержание кадмия снизилось в 1,57 и в 2,42 раза в побегах и корнях соответственно. При 50 мкМ наблюдался противоположный процесс – усиление накопления токсичного иона в корневой системе растений в присутствии гумата.
Рецензенты:
Пономарев В.А., д.б.н., профессор, кафедра селекции, ботаники и экологии, Ивановская ГСХА им. академика Д.К. Беляева, г. Иваново;
Борисова Е.А., д.б.н., профессор, зав.кафедрой общей биологии и физиологии, Ивановский государственный университет, г. Иваново.
Работа поступила в редакцию 28.12.2014.
Библиографическая ссылка
Кирдей Т.А. РОЛЬ ГУМАТА В СНИЖЕНИИ ФИТОТОКСИЧНОСТИ КАДМИЯ // Фундаментальные исследования. 2014. № 12-9. С. 1921-1925;URL: https://fundamental-research.ru/ru/article/view?id=36463 (дата обращения: 27.04.2026).



