Настоящая работа является продолжением наших исследований, посвященных тестированию ингибиторов окисления различного химического строения кинетическими методами [4, 5]. Для торможения процессов окисления применяют антиоксиданты (АО), которые находят все более широкое применение для предотвращения окислительных превращений липидов in vitro, а также in vivo в комплексной терапии широкого круга заболеваний [1, 2]. В связи с этим актуальной является проблема предварительного тестирования антиоксидантных свойств лекарственных препаратов, а также расширение ассортимента эффективных синтетических антиоксидантов, достижение высоких эффектов ингибирования при меньших концентрациях антиоксиданта.
Цель исследования – тестирование антиоксидантной активности капотена при различных способах инициирования в безводных и водно-липидных средах в сравнении со стандартными антиоксидантами, дибунолом и a-токоферолом.
Материалы и методы исследования
Антиоксидантную активность (АОА) изучали волюмометрическим методом поглощения кислорода в модифицированной установке типа Варбурга при окислении метиллинолеата (МЛ) в присутствии 1∙10−3 М цетилтриметиламмоний бромида (ЦТМАБ) в качестве поверхностно-активного вещества (ПАВ), с добавками 2∙10−3 М хлорида меди (II) в пробе при t = (60 ± 0,2) °С, Wi = 1,9∙10–5 М∙с–1. Соотношение липидов и воды составляло 1:3, а общий объем пробы 4 мл. Кинетическая модель тестирования антиоксидантов, подбор концентраций катализатора и ПАВ описываются в работе [6]. Кинетику поглощения кислорода изучали в среде инертного растворителя хлорбензола, процесс инициировали за счет термического разложения 6∙10–3 М азо-бис-изо-бутиронитрила (АИБН) в пробе при t = (60 ± 0,2) °С, Wi = 4,8∙10-8 М∙с–1. В качестве критериев оценки антиоксидантных свойств соединений использовали – периоды индукции (t), начальные и максимальные скорости окисления (Wнач., Wmax.). Кинетику накопления гидропероксидов изучали при аутоокислении метилолеата (МО) методом обратного йодометрического титрования в среде хлорбензола при t = (60 ± 0,2) °С.
Результаты исследования и их обсуждение
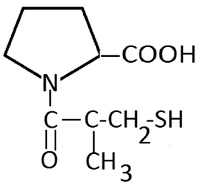
Капотен является производным пролина с отдаленной боковой тиольной группой. Препарат применяют при лечении легкой и умеренной гипертонии, а также при тяжелых формах сердечно-сосудистых заболеваний [3]. Химическая структура капотена позволяет прогнозировать его ингибирующую активность за счет разрушения гидропероксидов тиольной группой. Представляло интерес исследование антиоксидантной активности капотена в процессе окисления метиллинолеата в условиях инициирования в среде хлорбензола и катализа в водно-липидной среде в сравнении с дибунолом и a-токоферолом. Формулы изучаемых соединений представлены в табл. 1.
Таблица 1
Химические формулы изучаемых антиоксидантов
|
Название АО |
Формула |
|
Капотен 1-[(2S)-3-меркапто-2-метилпропионил]-L-пролин |
|
|
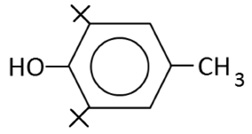
Дибунол (2,6-ди-трет-бутил-4-метил-фенол) |
|
|
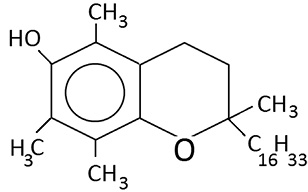
a-токоферол (6-гидрокси-2,5,7,8-тетраметил-2-фитилхроман) |
|
На рис. 1 представлены кинетические кривые (КК) окисления МЛ в растворе хлорбензола в присутствии широкого диапазона концентраций (1∙10−6–1∙10−1) М капотена. Показано, что капотен в безводной среде проявляет сложный механизм действия, обусловленный его вероятным участием в реакциях зарождения, продолжения и обрыва цепей. При одних концентрациях капотена происходит уменьшение максимальной скорости, при других наблюдается промотирование процесса окисления. Из табл. 2 видно, что начальные и максимальные скорости процесса меняются экстремально: снижаются с увеличением концентрации до 1∙10-4 М (соответствует соотношению инициатора и капотена 60:1) и увеличиваются при дальнейшем её повышении. Зависимость периода индукции от концентрации капотена в среде хлорбензола имеет максимум при концентрации (4–5)∙10-4 М (рис. 2). Характер воздействия капотена на процесс инициированного окисления МЛ может быть объяснен его участием в радикальном процессе. Радикал инициатора АИБН (Ri•) конкурентно взаимодействует с метиллинолеатом (RH) или с тиольной группой капотена (R1SH) по реакциям:
Ri• + RH → RiH + R•;
R1SH + Ri• → RiH + R1S•.
Далее радикалы метиллинолеата (R·) и капотена (R1S·) взаимодействуют с кислородом по реакциям:
R• + O2 → RO2•;
RO2• + RH → ROOH + R•;
R1SH + O2 → R1S• + HO2•;
R1S• + RH → R1SH + R•.
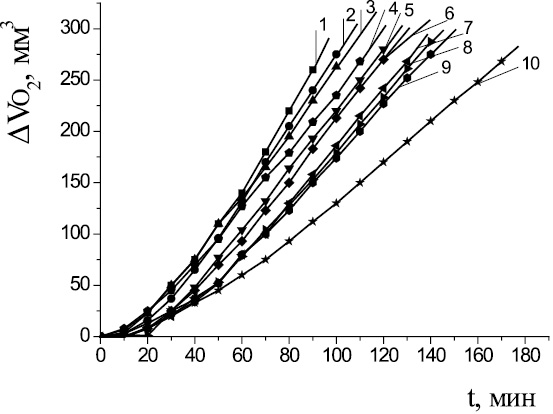
Рис. 1. Кинетика окисления метиллинолеата в безводной среде в присутствии 6∙10–3 М АИБН и капотена М: 2 – контроль; 1 – 1∙10–2, 3 – 8∙10–3; 4 – 1∙10–1; 5 – 5∙10–4; 6 – 5∙10–6, 7 – 1∙10–6; 8 – 1∙10–3; 9 – 8∙10–4; 10 – 5∙10–5, t = 60 °С
Наблюдаемое увеличение начальной скорости процесса при высоких концентрациях капотена происходит за счет участия капотена в реакциях инициирования, при этом соотношение инициатора и капотена составляет 1:(1,7–17).
Снижение начальной скорости окисления при небольших добавках капотена может быть связано с участием соединения в реакциях обрыва цепей:
R1SH + RO2• → ROOH + R1 S•.
Таблица 2
Кинетические параметры окисления метиллинолеата в растворе хлорбензола в присутствии 6∙10–3 М АИБН и в водно-липидной среде в присутствии 2∙10−3 М CuCl2 в зависимости от концентрации капотена, [InH] – ингибитор, t = 60 °С
|
Безводная среда, 6∙10–3 М АИБН |
||||
|
[InH], М |
t, мин |
Wнач∙10–8, М∙с–1 |
Wmax∙10–7, М∙с–1 |
[АИБН] [InH] |
|
Контроль МЛ |
20 |
6,0 |
2,2 |
– |
|
1∙10−6 |
42 |
5,0 |
1,9 |
6000:1 |
|
5∙10−6 |
36 |
4,7 |
1,8 |
1200:1 |
|
5∙10−5 |
90 |
4,5 |
1,7 |
120:1 |
|
1∙10−4 |
44 |
4,5 |
1,7 |
60:1 |
|
5∙10−4 |
36 |
4,9 |
2,0 |
12:1 |
|
1∙10−3 |
20 |
6,0 |
2,2 |
6:1 |
|
1∙10−2 |
30 |
7,2 |
2,4 |
1:1,7 |
|
1∙10−1 |
22 |
8,0 |
2,8 |
1:17 |
|
Водно-липидная среда, 2∙10−3 М CuCl2, 1∙10−3 М ЦТМАБ |
||||
|
[InH], М |
t, мин |
Wнач∙10–5, М∙с–1 |
Wmax∙10–4, М∙с–1 |
[CuCl2] [InH] |
|
Контроль МЛ |
5 |
14,4 |
2,6 |
– |
|
1∙10−6 |
8 |
7,6 |
1,6 |
2000:1 |
|
1∙10−5 |
15 |
6,9 |
1,0 |
200:1 |
|
1∙10−4 |
26 |
6,2 |
1,6 |
20:1 |
|
1∙10−3 |
45 |
3,6 |
1,7 |
2:1 |
|
1∙10−2 |
95 |
2,1 |
1,7 |
1:5 |
|
1∙10−1 |
395 |
0,6 |
1,7 |
1:50 |
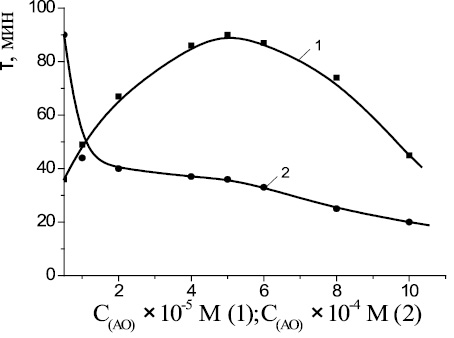
Рис. 2. Зависимости периода индукции от концентрации капотена в безводной среде; 6∙10–3 М АИБН, субстрат окисления – метиллинолеат, t = 60 °С
На рис. 3 приведены КК каталитического окисления МЛ в водно-липидной среде в присутствии (1∙10−6–1∙10−1) М капотена. Показано, что все добавки соединения тормозят процесс окисления, степень и характер влияния зависит от концентрации. Низкие концентрации капотена (1∙10−6–1∙10−3) М пропорционально уменьшают начальную и максимальную скорости процесса. При концентрациях 1∙10−3 М и выше происходит торможение начальных стадий процесса, увеличение периода индукции и достижение максимальной скорости процесса после выхода из периода индукции (табл. 2). На рис. 4 показана линейная зависимость периода индукции от роста концентрации капотена. Характер влияния капотена на кинетику каталитического окисления МЛ может быть объяснен следующим образом. Капотен может участвовать в реакциях обрыва цепей, обеспечивая ингибирование процесса окисления. Снижение скорости окисления под влиянием капотена может быть обусловлено его конкурентным участием с катализатором в молекулярном распаде гидропероксидов:
RO2• + R1SH → ROOH + R1S•;
ROOH + R1SH → M;
ROOH + Cu2+ → RO2• + H+ + Cu1+.
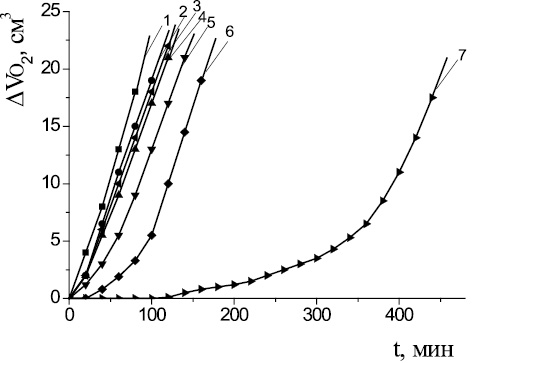
Рис. 3. Кинетика окисления метиллинолеата в водно-липидной среде в присутствии капотена: 1 – контроль; 2 – 1∙10–6 М; 3 – 1∙10–5 М; 4 – 1∙10–4 М; 5 – 1∙10–3 М; 6 – 1∙10–2 М; 7 – 1∙10–1 М; 2∙10−3 М CuCl2, 1∙10−3 М ЦТМАБ, t = 60 °С
Значимое торможение с последующим достижением максимальной скорости процесса начинается при соотношениях катализатора и капотена 1:1 и усиливается при соотношениях 1:5 и 1:50. Очевидно, что в этих условиях происходит нейтрализация катализатора за счет его восстановления в Cu1+. При большом избытке капотена восстановление Cu2+ в Cu1+ происходит быстрее, наблюдается эффективное торможение процесса окисления:
R1SH + Cu2+ → R1S• + H+ + Cu1+.
Для подтверждения гипотезы о возможном разрушении гидропероксидов под действием капотена был проведен эксперимент по прямому тестированию кинетики накопления гидропероксидов (ROOH) после введения капотена в частично окисленный субстрат (время эксперимента 8 часов). В течение первого часа (рис. 5) наблюдалось снижение концентрации гидропероксидов, в контрольном опыте ROOH продолжали накапливаться. Установлено, что все исследуемые добавки капотена способствовали разрушению гидропероксидов на 50–75 %.
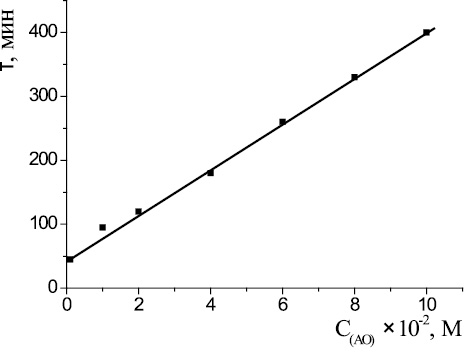
Рис. 4. Зависимость периода индукции от концентрации капотена в водно-липидной среде: 2∙10–3 М CuCl2, 1∙10−3 М ЦТМАБ, субстрат окисления – метиллинолеат, t = 60 °С
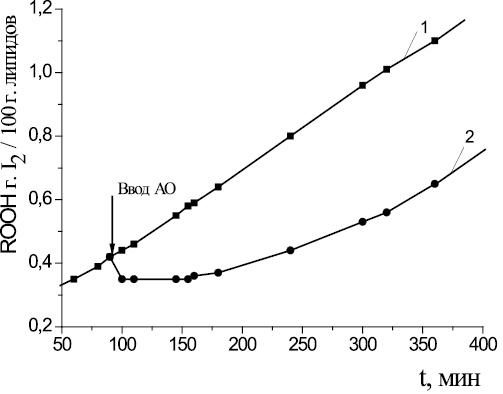
Рис. 5. Кинетика накопления гидропероксидов при аутоокислении МО в присутствии АО: 1 – контроль; 2 – капотен. Стрелкой показан ввод АО. С(АО) = 2∙10–4M, t = 60 °C
Проведено исследование закономерностей окисления метиллинолеата в присутствии добавок стационарных ингибиторов окисления дибунола и a-токоферола. Установлен идентичный характер кинетических кривых окисления липидного субстрата в растворе хлорбензола в присутствии 6∙10−3 М инициатора и водно-липидной системе с добавками 2∙10−3 М хлорида меди (II) при равных концентрациях дибунола: наблюдался период полного торможения, период аутоускорения и достижение максимальной скорости окисления. Периоды индукции увеличивались пропорционально увеличению концентрации дибунола (табл. 3).
Таблица 3
Кинетические параметры окисления метиллинолеата в растворе хлорбензола в присутствии 6∙10–3 М АИБН и в водно-липидной среде в присутствии 2∙10−3 М CuCl2 в зависимости от концентрации a-токоферола, дибунола, [InH] – ингибитор, t = 60 °С
|
Безводная среда, 6∙10–3 М АИБН |
|||
|
[InH], М |
t, мин |
Wнач∙10–8, М∙с–1 |
Wmax∙10–7, М∙с–1 |
|
Контроль МЛ |
15 |
4,3 |
2,6 |
|
a-токоферол |
|
|
|
|
1∙10–8 |
17 |
4,3 |
2,3 |
|
1∙10–6 |
35 |
2,5 |
1,9 |
|
1∙10–4 |
67 |
1,1 |
1,8 |
|
1∙10–3 |
350 |
0,6 |
1,7 |
|
Дибунол |
|
|
|
|
1∙10–6 |
35 |
4,3 |
2,5 |
|
1∙10–5 |
45 |
3,4 |
2,4 |
|
1∙10–4 |
170 |
2,1 |
2,1 |
|
1∙10–3 |
650 |
1,6 |
1,8 |
|
Водно-липидная среда, 2∙10−3 М CuCl2, 1∙10−3 М ЦТМАБ |
|||
|
[InH], М |
t, мин |
Wнач∙10–5, М∙с–1 |
Wmax∙10–4, М∙с–1 |
|
Контроль МЛ |
5 |
14,4 |
2,6 |
|
a-токоферол |
|
|
|
|
1∙10−8 |
10 |
14,0 |
2,1 |
|
1∙10−6 |
20 |
9,7 |
1,9 |
|
1∙10–4 |
35 |
5,2 |
1,4 |
|
1∙10–3 |
15 |
14,6 |
3,2 |
|
Дибунол |
|
|
|
|
1∙10−6 |
30 |
13,8 |
2,5 |
|
1∙10−5 |
40 |
12,7 |
2,3 |
|
1∙10−4 |
160 |
4,1 |
1,8 |
|
1∙10−3 |
590 |
1,9 |
1,5 |
КК окисления метиллинолеата в безводной среде с добавками (1∙10–8–1∙10–5) М a-токоферола имели аутоускоренный характер без периода полного торможения. Период полного торможения появлялся только при концентрациях (1∙10–4–5∙10–4) М и увеличивался пропорционально концентрации ингибитора, a-токоферол в водно-липидной среде проявлял слабые антиоксидантные свойства, в концентрациях свыше 1∙10–3 М промотировал процесс окисление липидных субстратов. В присутствии (1∙10–5–1∙10–4) М a-токоферола наблюдалось замедление начальных стадий окисления и уменьшение максимальной скорости (табл. 3). В процессе окисления a-токоферол образует достаточно активные токофероксильные радикалы (In•), способные участвовать в побочных реакциях продолжения цепей с молекулами суб страта (RH) [1]:
In• + RH → R• + InH.
В результате этой реакции восстанавливается активная фенольная форма антиоксиданта, взаимодействующая в дальнейшем с пероксильными радикалами:
RO2• + InH → ROOH + In•.
Выводы
1. Установлено, что синтетический ингибитор окисления дибунол в двух кинетических моделях в безводной и водно-липидной средах превосходит по своему действию природный антиоксидант a-токоферол.
2. Выявлена высокая антиоксидантная активность капотена в водно-липидных катализируемых субстратах, превышающая ингибирующие свойства a-токоферола и уступающая активности дибунола.
3. Установлено, что капотен в процессе окисления разрушает гидропероксиды молекулярным путем. Вероятно, что способность разрушения гидропероксидов капотеном связана с наличием тиольной группы.
Рецензенты:Ерёмин Д.И., д.б.н., профессор кафедры почвоведения и агрохимии, ФГБОУ ВПО «Государственный аграрный университет Северного Зауралья», г. Тюмень;
Грехова И.В., д.б.н., профессор кафедры общей химии, ФГБОУ ВПО «Государственный аграрный университет Северного Зауралья», г. Тюмень.
Работа поступила в редакцию 12.11.2014.
Библиографическая ссылка
Перевозкина М.Г. КИНЕТИЧЕСКИЕ МЕТОДЫ ДЛЯ ТЕСТИРОВАНИЯ АНТИОКСИДАНТНЫХ СВОЙСТВ КАПОТЕНА // Фундаментальные исследования. 2014. № 11-11. С. 2416-2422;URL: https://fundamental-research.ru/ru/article/view?id=35957 (дата обращения: 28.05.2026).