При любой патологии в организме создаются условия для интенсификации свободнорадикального окисления липидов и белков (СРО), в результате чего значительно возрастает количество молекулярных, первичных, вторичных и конечных продуктов, которые являются мощными прооксидантами, инициирующими процессы СРО. Развивается так называемый феномен «снежной» лавины, а именно: количества молекулярных первичных, вторичных и конечных продуктов значимо возрастает. Следующий этап этого процесса – проявление функционального дисбаланса в неферментативном и ферментативном звеньях эндогенной системы антиоксидантной защиты (АОЗ), которая не справляется с задачами регламентации и лимитирования уровней активных форм кислорода, свободных радикалов и молекулярных продуктов СРО, в результате чего создаются условия для формирования «свободнорадикальной патологии», или окислительного стресса. Стресс именно окислительный, а не оксидантный или оксидативный, как его называли раньше и порой называют и сейчас в публикуемых изданиях. Термин окислительный стресс более адаптирован для обозначения самого процесса, лежащего в основе его формирования, а именно свободно-радикального окисления. Оксиданты, прооксиданты и антиоксиданты являются «боевыми» единицами процесса свободнорадикального окисления и окислительного стресса. При этом отмечена прямая связь между уровнем активных форм кислорода, свободных радикалов, молекулярных продуктов СРО и интенсивностью проявления окислительного стресса, а именно их избыток как проявление окислительного стресса приводит к нарушению функционального и структурного состояния клеточных биомембран, что является одним из ключевых направлений в развитии патологии. Необходимо выделить два блока формирования окислительного стресса:
1. Интенсификация процессов СРО липидов и белков.
2. Функциональный дисбаланс в ферментативном и неферментативном звеньях эндогенной системы АОЗ.
Современные теории полигенной системы защиты организма рассматривают не только иммунную систему как основной фактор защиты, но и систему метаболизма, которая формирует метаболический барьер для защиты организма, или, выражаясь образно, метаболический иммунитет. Исходя из этих позиций взаимодействие процессов СРО и эндогенной системы АОЗ можно считать одним из механизмов развития метаболического иммунитета, тогда и окислительный стресс как проявление нарушения согласованного взаимодействия процессов СРО липидов и белков и эндогенной системы АОЗ можно рассматривать как поломку одного из механизмов в едином комплексе метаболического иммунитета, что окажет негативное влияние на жизнедеятельность организма и его взаимоотношение с меняющимися факторами внешней среды, что приведет к дезадаптации организма и развитию патологии. Таким образом, окислительный стресс следует рассматривать как одно из звеньев сложнейшего механизма патогенеза инсульта и рассеянного склероза [1, 2, 5]. Настоящее исследование посвящено верификации окислительного стресса, одного из звеньев сложнейшего патогенеза медико-социально и экономически значимых заболеваний нервной системы – инсульта и рассеянного склероза. Инсульт входит в рубрику цереброваскулярных заболеваний, являясь лидирующей причиной смертности, негативно влияющей на демографические показатели населения Российской Федерации. Рассеянный склероз – актуальнейшая проблема современной клинической неврологии. Болеют молодые талантливые юноши и девушки. Тяжелое течение этого заболевания приводит к высокой степени инвалидизации, выводя из активной творческой колеи жизни перспективную работоспособную часть населения. Научная ценность и практическая значимость работ, направленных на изучение сложнейших механизмов патогенеза инсульта и рассеянного склероза, состоит в том, что они позволяют разрабатывать перспективные патогенетически обусловленные подходы к лечению этих социально значимых заболеваний нервной системы [6].
Целью настоящего исследования является верификация двух блоков формирования окислительного стресса при инсульте и рассеянном склерозе.
Материалы и методы исследования
Группу исследования составили 120 пациентов, из них 60 больных с инсультом: ишемический инсульт (ИИ) – 30 и геморрагический (ГИ) – 30. Вторая группа пациентов – 60 больных рассеянным склерозом, которые были подразделены на 2 подгруппы: первично прогрессирующая форма клинического течения рассеянного склероза (ППРС) – 30, вторично прогрессирующая форма клинического течения рассеянного склероза (ВПРС) – 30. В контрольную группу вошли 30 исследуемых человек сопоставимого возраста с клиническими группами, но без проявлений заболеваний нервной системы – доноры.
В качестве субстратов для определения динамики параметров интенсивности свободнорадикального окисления липидов и белков, а именно параметров первичных, вторичных и конечных продуктов свободнорадикального окисления липидов и белков и активности эндогенной системы антиоксидантной защиты по маркерам неферментативного звена: витамин Е и восстановленный глутатион и ферментативного звена: глутатионпероксидаза и глутатионредуктаза, верифицирующей окислительный стресс при инсульте и рассеянном склерозе, у всех 120 пациентов использовалась цельная стабилизированная кровь, сыворотка, плазма крови и взвесь эритроцитов, полученные общепринятыми в биологической методологии способами. Таким же образом было проведено исследование субстратов и у 30 доноров. При этом применялись следующие методики исследования: спектрофотометрия, спектрокалориметрия, фотоэлектрокалориметрия и биохемилюминесценция. Для оценки достоверности различия показателей в сравниваемых группах по каждому показателю математически были рассчитаны выборочные средние, а также 95 % доверительные интервалы для генеральных средних.
Результаты исследования
и их обсуждение
Нами получены результаты параметров вторичных и конечных продуктов свободнорадикального окисления липидов и белков при ишемическом и геморрагическом инсульте, а также при рассеянном склерозе первично и вторично прогрессирующей клинической формы течения заболевания, которые представлены на рис. 1 и 2. Вторичный продукт свободнорадикального окисления липидов, а именно малоновый деальдегид, образуется в результате окислительной модификации углеводородных хвостов молекул липидов и жирных кислот, фактически в результате распада диеновых конъюгатов и кетодиенов. Повышение параметров малонового диальдегида свидетельствуют об избыточной активации процессов свободнорадикального окисления. Малоновый диальдегид очень токсичен и химически активен. Увеличение параметров малонового диальдегида сопровождается заметным снижением активности глюкозо-6-фосфатазы в эндоплазматическом ретикулуме, а также различных АТФаз и ацетилхолинэстеразы в эритроцитах. Таким образом малоновый диальдегид оказывает повреждающее действие, связанное с нарушением структурно-функционального состояния биомембран. Способствует увеличению их проницаемости для Ca2+, что может влиять на возникновение его избытка в клетке с реализацией повреж-
дающего действия.
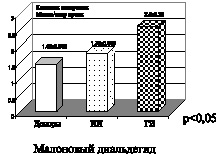
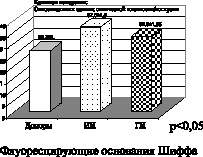
Рис. 1. Ишемический (ИИ) и геморрагический инсульт (ГИ)
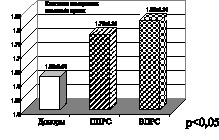
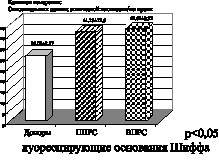
Рис. 2. Рассеянный склероз. Первично прогрессирующая (ППРС) и вторично прогрессирующая (ВПРС) клинические формы течения рассеянного склероза
На представленных рисунках при ишемическом, в большей степени геморрагическом инсульте, а также при склерозе первично и вторично прогрессирующих клинических формах рассеянного склероза четко отмечено увеличение параметров малонового диальдегида, что подтверждает интенсификацию процессов свободнорадикального окисления липидов при вышеперечисленных клинических формах заболеваний. Вторичный продукт СРО – малоновый диальдегид, взаимодействуя с N-концевыми остатками аминокислот и аминогруппами фосфолипидами, образуют конъюгированные флуоресцирующие соединения типа основания Шиффа. Эти соединения являются более стабильными, конечными продуктами СРО липидов и белков. Их утилизация в организме происходит с очень низкой скоростью, в результате чего они накапливаются в тканях организма как балласт. Увеличение параметров оснований Шиффа при геморрагическом и больше при ишемическом инсульте, а также при первично прогрессирующей и вторично прогрессирующей клинических формах течения рассеянного склероза свидетельствует о тенденции к хронизации и избыточной активации процессов свободнорадикального окисления липидов и белков.
Полученные данные исследования позволяют сделать вывод о том, что при ишемическом и геморрагическом инсульте, а также при первично прогрессирующей и вторично прогрессирующей формах рассеянного склероза имеет место формирование первого блока окислительного стресса, а именно интенсификация процессов свободнорадикального окисления липидов и белков.
Активация процессов СРО липидов и белков при анализируемых нами формах логически требует увеличения активности маркеров неферментативного и ферментативного звеньев эндогенной системы антиоксидантной защиты [3, 4]. Проанализируем полученные нами в процессе исследования данные показателей активности маркеров АОЗ, а именно маркеров неферментативного звена эндогенной системы антиоксидантной защиты: витамина Е, восстановленного глутатиона при ишемическом и геморрагическом инсульте и витамина Е и общих тиолов при первично прогрессирующей и вторично прогрессирующей формах рассеянного склероза, которые представлены на рис. 3, 4.

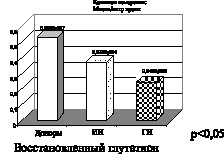
Рис. 3. Ишемический (ИИ) и геморрагический инсульт (ГИ)
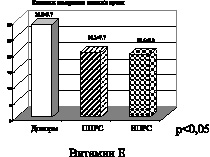
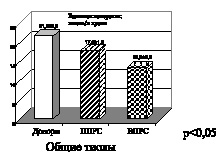
Рис. 4. Рассеянный склероз. Первично прогрессирующая (ППРС) и вторично прогрессирующая (ВПРС) клинические формы течения рассеянного склероза
На рис. 3 представлены показатели активности витамина Е и восстановленного глутатиона. Витамин Е является одним из основных эндогенных антиоксидантов, а именно эффективно «тушит» синглетный кислород и «перехватывает» свободные радикалы непосредственно реагируя с ними на стадии обрыва цепей. Антиоксидантную активность витамина Е связывают также с его взаимодействием с перекисными соединениями органической природы. Представленные на рисунке данные указывают на снижение активности витамина Е при геморрагическом и в большей степени ишемическом инсульте.
Восстановленный глутатион – эндогенный антиоксидант, который участвует в реакциях с гидроперекисями, сам при этом окисляется. Используется в работе антиперекисного комплекса в качестве субстрата, а именно глутатионпероксидаза взаимодействует с восстановленным глутатионом в реакциях с гидроперекисями, и при этом глутатион окисляется. Окисленный же глутатион является субстратом для работы глутатионредуктазы, которая в результате взаимодействия с гидроперекисями переводит его в восстановленное состояние – восстановленный глутатион, который вновь используется субстратом для реакций, в которых участвует глутатионпероксидаза. Глутатион участвует в транспорте аминокислот, а также в поддержании субгидрильных групп белков в восстановленном состоянии. Снижение его показателей активности, представленное на рис. 3, свидетельствует о дисбалансе в ферментативном и неферментативном звеньях
эндогенной системы антиоксидантной защиты при ишемическом и геморрагическом инсульте.
На рис. 4 при первично и вторично прогрессирующих клинических формах течения рассеянного склероза также отмечено снижение активности витамина Е. Снижение показателей активности витамина Е свидетельствует о функциональном дисбалансе в неферментативном звене эндогенной системы антиоксидантной защиты. Антиоксидантными свойствами обладают и соединения, содержащие сульфгидридные группы, относящиеся к неферментативному звену системы АОЗ. Это общие тиолы –SH-группировки, которые взаимодействуют с активными формами кислорода и перекисными радикалами, восстанавливая последние до нетоксичных продуктов. Снижение показателей активности общих тиолов, представленное на рис. 4, еще раз подтверждает наличие функционального дисбаланса в эндогенной системе антиоксидантной защиты. На рис. 5, 6 представлены графики показателей активности глутатионпероксидазы и глутатионредуктазы маркеров ферментативного звена эндогенной системы антиоксидантной защиты.


Рис. 5. Ишемический (ИИ) и геморрагический инсульт (ГИ)
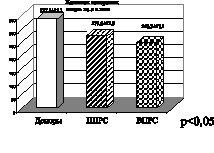
Активность глутатионредуктаза Активность глутатионпероксидаза
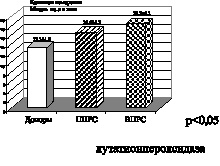
Рис. 6. Рассеянный склероз. Первично прогрессирующая (ППРС) и вторично прогрессирующая (ВПРС) клинические формы течения рассеянного склероза
Глутатионпероксидаза – фермент, катализирующий превращение перекиси водорода и органических гидроперекисей до гидросоединений, которые в дальнейшем могут метаболизироваться клеточными системами. Эффективность глутатионпероксидазного механизма восстановления гидроперекисей в значительной степени зависит от уровня основного донора для осуществления этой реакции – восстановленного глутатиона. Поддержание достаточного уровня восстановленной формы глутатиона, окисляющегося при функционировании глутатионзависимых антиперекисных систем, осуществляется ферментом глутатионредуктазой. Глутатионредуктазу относят к ферментативному звену АОЗ. Субстратом для работы глутатионредуктазы является окисленный глутатион, который она переводит в восстановленный. Активность фермента возрастает при увеличении концентрации восстановленных форм
перидиннуклеотидов и окисленного глутатиона. Таким образом, глутатионредуктаза и глутатионпероксидаза формируют замкнутый антиперекисной комплекс. На рис. 5, 6 представлены показатели активности глутатионпероксидазы и глутатионредуктазы, при этом необходимо отметить, что при ишемическом инсульте отмечено снижение показателя активности глутатионпероксидазы, при геморрагическом инсульте в меньшей степени, а при рассеянном склерозе первично и вторично прогрессирующих клинических форм течения имеет место снижение активности глутатионредуктазы. Это подтверждает наличие функционального дисбаланса в ферментативном звене эндогенной системы антиоксидантной защиты. Таким образом, на основании полученных нами данных подтверждается формирование второго блока окислительного стресса, а именно функциональный дисбаланс в неферментативном и ферментативном звеньях эндогенной системы антиоксидантной защиты при геморрагическом, ишемическом инсульте, а также при первично и вторично прогрессирующих клинических формах течения рассеянного склероза.
Заключение
Анализируя все полученные данные по параметрам интенсивности свободнорадикального окисления липидов и белков, а также показателям активности ферментативного и неферментативного звеньев эндогенной системы антиоксидантной защиты, можно сделать вывод о верификации окислительного стресса в патогенезе ишемического, геморрагического инсульта и первично, вторично прогрессирующих форм клинического течения рассеянного склероза, что является основанием для назначения антиоксидантов в комплексном лечении инсульта и рассеянного склероза. Успешное лечение этих тяжелых заболеваний улучшит качество жизни пациентов.
Рецензенты:Алабовский В.В., д.м.н., профессор, заведующий кафедрой биохимии, ВГМА им. Н.Н. Бурденко, г. Воронеж;
Лаврентьев А.А., д.м.н., профессор кафедры реанимации и анестезиологии ИДПО, ВГМА им. Н.Н. Бурденко, г. Воронеж.
Работа поступила в редакцию 23.10.2014.
Библиографическая ссылка
Луцкий М.А., Земсков А.М., Смелянец М.А., Лушникова Ю.П. ФОРМИРОВАНИЕ ОКИСЛИТЕЛЬНОГО СТРЕССА, ОДНОГО ИЗ ЗВЕНЬЕВ СЛОЖНОГО ПАТОГЕНЕЗА СОЦИАЛЬНО ЗНАЧИМЫХ ЗАБОЛЕВАНИЙ НЕРВНОЙ СИСТЕМЫ – ИНСУЛЬТА И РАССЕЯННОГО СКЛЕРОЗА // Фундаментальные исследования. 2014. № 10-5. С. 924-929;URL: https://fundamental-research.ru/ru/article/view?id=35766 (дата обращения: 02.05.2026).



