Но-шпалгин – комбинированное лекарственное средство, обладающее спазмолитическим и анальгезирующим действием [4]. Широкое использование парацетамола, дротаверина гидрохлорида и кодеина фосфата, являющихся компонентами данного препарата, неизбежно приводит к попаданию их в окружающую среду. В последнее время в почве и в водных источниках все чаще обнаруживаются лекарственные средства и их метаболиты. Попадающие в окружающую среду стабильные и биоактивные фармполлютанты оказывают хроническое воздействие на организм человека и способствуют нарушению экологического баланса [6, 9]. В ранее проведенных исследованиях показано, что биохимическое превращение парацетамола, дротаверина гидрохлорида и кодеина фосфата с использованием доминирующих в почвенных микробиоценозах актинобактерий рода Rhodococcus сопровождается образованием устойчивых метаболитов [2, 3, 5]. Следует отметить, что научные статьи, посвященные одновременной идентификации парацетамола, кодеина и дротаверина в культуральной жидкости бактериальных культур, отсутствуют. Поиск условий идентификации данных веществ предполагает разработку методики качественного анализа препарата Но-шпалгин в процессе его биологической деструкции.
Цель настоящего исследования – разработка методики идентификации компонентов комплексного лекарственного средства Но-шпалгин, а также продуктов их биологической деструкции в постферментационных культуральных средах родококков с использованием тонкослойной хроматографии.
Материалы и методы исследования
В работе использовали фармацевтические субстанции парацетамола (C8H9NO2, CAS: 103-90-2) («Аньцю Луань Фармасьютикал Ко., Лтд.», Китай), кодеина фосфата (C18H21NO3, CAS: 76-57-3) («Алкалибер С.А.», Испания), дротаверина гидрохлорида (C24Н31NO4, CAS: 985-12-6) (Ирбитский химико-фармацевтический завод, Россия) и комплексный препарат в виде готовой лекарственной формы (таблетки) Но-шпалгин (ЗАО «Хиноин», Будапешт, Венгрия), содержащий парацетамола 500 мг, дротаверина гидрохлорида 40 мг, кодеина фосфата (в форме гемигидрата) 8 мг.
Эксперименты по биодеструкции лекарственных средств проводили в колбах Эрленмейера, содержащих 100 мл минерально-солевой среды RS [5], в условиях периодического культивирования (160 об/мин, 28 °С, pH 6,8) на орбитальной качалке Cetromat IS («Sartorius», Германия). Концентрации парацетамола, дротаверина гидрохлорида и кодеина фосфата составляли 200, 20 и 40 мг/л соответственно. В качестве биодеструктора дротаверина гидрохлорида и кодеина фосфата использовали штамм R. rhodochrous ИЭГМ 647, парацетамола – штамм R. erythropolis ИЭГМ 767 из Региональной профилированной коллекции алканотрофных микроорганизмов (акроним коллекции ИЭГМ, номер во Всемирной федерации коллекции культур 768, [8]) [2, 3, 5]. Для биодеструкции Но-шпалгина использовали ассоциацию обоих штаммов. Посевным материалом служили клетки R. rhodochrous ИЭГМ 647, предварительно выращенные в присутствии низких концентраций дротаверина (2 мг/л) и кодеина (4 мг/л). Клетки штамма R. erythropolis ИЭГМ 767 выращивали в присутствии структурного аналога парацетамола – фенола (1000 мг/л). Продолжительность процесса биодеструкции парацетамола составила 20 сут, кодеина фосфата – 90 сут, дротаверина гидрохлорида – 25 сут, Но-шпалгина – 90 сут. В качестве контролей абиотической деструкции использовали стерильный раствор соединений в среде RS.
Пробы культуральных жидкостей для аналитических исследований (2 мл) в процессе биодеструкции лекарственных средств отбирали на 10 сут в случае парацетамола, на 15 сут – дротаверина гидрохлорида, 75 сут – кодеина фосфата и 30 сут – Но-шпалгина. Подготовку проб для анализа осуществляли посредством их центрифугирования при 10000 об/мин (MiniSpin Eppendorf, Германия) в течение 5 мин. Для хроматографического анализа дротаверина гидрохлорида использовали надосадочную жидкость (10 мкл), парацетамола и Но-шпалгина – осадок и надосадочную жидкость. В случае кодеина фосфата использовали хлороформенный экстракт надосадочной жидкости (pH 8,0).
При изучении хроматографической подвижности парацетамола и продуктов его биодеструкции исследовали 8 систем растворителей: 1П – хлороформ-ацетон (9:1); 2П – хлороформ – ацетон (8:2); 3П – гексан – этилацетат (85:15); 4П – диоксан – хлороформ – ацетон – раствор аммиака 25 % (47,5:45:5:2,5); 5П – этилацетат – спирт этиловый 95 % раствор аммиака 25 % (17:2:1); 6П – хлороформ – спирт этиловый 95 % (7:3); 7П – толуол – ацетон – спирт этиловый 95 % раствор аммиака 25 % (45:45:7,5:2,5); 8П – хлороформ – спирт этиловый 95 % (8:2). В отношении кодеина фосфата и продуктов его биодеструкции апробировали 6 систем растворителей: 1К – толуол-ацетон-спирт этиловый 95 % раствор аммиака 25 % (45:45:7,5:2,5); 2К – толуол-спирт этиловый 95 % триэтиламин (9:1:1); 3К – этилацетат – спирт – этиловый 95 % раствор аммиака 25 % (17:2:1); 4К – хлороформ – н-бутанол – раствор аммиака 25 % (70:40:15); 5К – хлороформ-спирт этиловый 95 % (9:1); 6К – хлороформ-спирт этиловый 95 % раствор аммиака 25 % (9,5:0,5:1); 7К – хлороформ-метанол-раствор аммиака 25 % (9:0,9:0,1). Для разделения дротаверина гидрохлорида и продуктов его биодеструкции использовали 6 составов подвижных фаз: 1Д – хлороформ – спирт этиловый 95 % (80:20); 2Д – бензол – метанол – раствор аммиака 25 % (20:4:0,1); 3Д – бензол-спирт этиловый 95 % раствор аммиака 25 % (80:10:0,1); 4Д – хлороформ – спирт этиловый 95 % ацетон (80:20:10); 5Д – хлороформ – спирт этиловый 95 % ацетон (80:10:5); 6Д – толуол – ацетон – спирт этиловый 95 % раствор аммиака 25 % (45:45:7,5:2,5).
Хроматографирование проводили на пластинах «Сорбфил» ПТСХ-АФ-А-УФ (ЗАО «Сорбполимер», Россия). Детекцию веществ осуществляли УФ облучением при длинах волн 254 и 365 нм, а также обработкой парами йода и реактивами Фреде, Эрдмана, Зонненшейна, Марки, Драгендорфа [1]. В качестве свидетелей лекарственных средств использовали растворы парацетамола 0,2 %, дротаверина гидрохлорида 0,002 % и кодеина фосфата 0,004 % в среде RS. Свидетелями продуктов разложения парацетамола являлись спиртовые растворы п-аминофенола, гидрохинона, бензохинона и пирокатехина (Merck, Германия), а продуктов биодеструкции дротаверина гидрохлорида – спиртовые растворы 3,4-диэтоксибензальдегида и 3,4-диэтоксибензойной кислоты (Merck, Германия).
Результаты исследования и их обсуждение
По нашим данным, наиболее эффективное разделение парацетамола и продуктов его биодеструкции наблюдалось в системах 1П, 7П и 8П (табл. 1).
Наиболее чувствительным детектором парацетамола и его метаболитов являлся УФ свет при длине волны 365 нм (предел обнаружения парацетамола УФ светом в системе 8П – 2,5 мкг/мкл, при обработке парами йода – 5 мкг/мкл).
Таблица 1
Значения величин Rf×100 парацетамола и продуктов его биодеструкции в культуральной среде R. erythropolis ИЭГМ 767
|
Исследуемые вещества |
Система растворителей |
|||||||
|
1П |
2П |
3П |
4П |
5П |
6П |
7П |
8П |
|
|
Парацетамол |
18 |
33 |
41 |
63 |
78 |
74 |
51 |
55 |
|
п-Аминофенол |
16 |
34 |
38 |
71 |
81 |
82 |
53 |
51 |
|
Гидрохинон |
59 |
63 |
49 |
83 |
94 |
77 |
69 |
60 |
|
Бензохинон |
46 |
66 |
57 |
– |
82 |
82 |
64 |
58 |
|
Пирокатехин |
43 |
– |
68 |
83 |
84 |
82 |
61 |
73 |
|
Неидентифицированный продукт биодеструкции |
29 |
12 |
– |
– |
– |
– |
11 |
81 |
Примечание. «–» зона вещества не обнаружена.
Эффективное разделение кодеина фосфата и продуктов его биодеструкции наблюдалось в системах 1К, 3К, 7К (табл. 2). Предел обнаружения кодеина фосфата в данных системах: при облучении УФ светом с длиной волны 365 нм – 1 мкг/мл, при обработке парами йода – 2 мкг/мл, при обработке реактивом Драгендорфа – 0,5 мкг/мл. Несмотря на высокую чувствительность в отношении кодеина, реактив Драгендорфа не позволяет идентифицировать большинство продуктов биодеструкции данного вещества. Поэтому рациональным является использование комбинированного детектирования: облучение УФ светом при длине волны 365 нм с последующей обработкой пластин реактивом Драгендорфа. Поскольку система 7К по сравнению с системами 1К и 3К позволяет обнаружить наибольшее количество продуктов биодеструкции кодеина, два из которых, согласно данным Lister D.L., Kanungo G. и др. [7], представляют собой 14-гидроксикодеинон (Rf×100 = 53) и дигидрокодеин (Rf×100 = 23), ее можно считать оптимальной для дальнейшего изучения параметров удерживания кодеина и продуктов его биодеструкции.
Таблица 2
Значения величин Rf×100 кодеина фосфата и продуктов его биодеструкции в культуральной среде R. rhodochrous ИЭГМ 647
|
Исследуемые вещества |
Система растворителей |
||||||
|
1К |
2К |
3К |
4К |
5К |
6К |
7К |
|
|
Кодеина фосфат |
34 |
44 |
23 |
63 |
28 |
44 |
36 |
|
Продукты биодеструкции |
25 |
– |
19; 41 |
– |
– |
– |
15;23;29;53 |
Примечание. «–» зона вещества не обнаружена.
Наиболее селективными системами, позволяющими разделить продукты биодеструкции дротаверина гидрохлорида, являлись 1Д, 3Д и 6Д (табл. 3).
Таблица 3
Значения величин Rf×100 дротаверина гидрохлорида и продуктов его биодеструкции в культуральной среде R. rhodochrous ИЭГМ 647
|
Исследуемые вещества |
Система растворителей |
|||||
|
1Д |
2Д |
3Д |
4Д |
5Д |
6Д |
|
|
Дротаверина гидрохлорид |
71 |
32 |
25 |
65 |
53 |
75 |
|
3,4-Диэтоксибензальдегид |
80 |
– |
78 |
– |
– |
– |
|
3,4-Диэтоксибензойная кислота |
90 |
– |
– |
– |
– |
88 |
|
Неидентифицированный продукт биодеструкции |
– |
– |
– |
– |
– |
80 |
Примечание. «–» зона вещества не обнаружена.
Предел обнаружения дротаверина гидрохлорида в данных системах составил 2 мкг/мл при детектировании УФ светом (длина волны 365 нм), парами йода и реактивом Драгендорфа. Однако предпочтительно использовать УФ свет, так как данный способ, в отличие от других, наряду с дротаверином позволяет обнаружить продукты его биодеструкции.
Для определения парацетамола, дротаверина гидрохлорида и кодеина фосфата как компонентов препарата Но-шпалгин, а также продуктов их биологической деструкции в культуральных средах родококков использовали 3 системы растворителей (табл. 4), выбранные в качестве оптимальных: 1Н – хлороформ – спирт этиловый 95 % (80:20); 2Н – этилацетат-спирт этиловый 95 % раствор аммиака 25 % (17:2:1); 3Н – толуол – ацетон – спирт этиловый 95 % раствор аммиака 25 % (45:45:7,5:2,5).
Таблица 4
Значения Rf×100 компонентов Но-шпалгина и продуктов их биодеструкции в культуральных средах R. rhodochrous ИЭГМ 647 и R. erythropolis ИЭГМ 767
|
Объекты исследования |
Подвижная фаза |
||
|
1Н |
2Н |
3Н |
|
|
Значения Rf×100 компонентов препарата Но-шпалгин и продуктов их биодеструкции |
|||
|
Парацетамол |
55 |
78 |
51 |
|
Продукты биодеструкции |
13, 58, 60, 73, 81 |
81, 82, 84, 94 |
11, 53, 64, 61, 69 |
|
Дротаверина гидрохлорид |
51 |
13 |
75 |
|
Продукты биодеструкции |
22 |
5, 88 |
5, 15, 90 |
|
Кодеина фосфат |
32 |
23 |
34 |
|
Продукты биодеструкции |
– |
19, 41 |
25, 43, 48, 71 |
|
Неидентифицированные продукты биодеструкции препарата Но-шпалгин |
– |
– |
80, 86 |
Примечание. «–» зона вещества не обнаружена.
По нашим данным, оптимальной системой для разделения компонентов препарата Но-шпалгин и продуктов их биодеструкции является система 3Н (табл. 5, рисунок). Детектор – УФ свет при длине волны 365 нм. Анализ продуктов биодеструкции парацетамола в данной системе растворителей позволил обнаружить, помимо парацетамола (Rf×100 = 51), п-аминофенол (Rf×100 = 53), бензохинон (Rf×100 = 64), гидрохинон (Rf×100 = 69) и два неидентифицированных вещества (Rf×100 = 61 и Rf×100 = 11). Среди продуктов биодеструкции дротаверина гидрохлорида, помимо дротаверина (Rf×100 = 75), обнаружены соединения: 3,4-диэтоксибензальдегид (Rf×100 = 90), 3,4-диэтоксибензойная кислота (Rf×100 = 5) и неидентифицированное вещество (Rf×100 = 15). В качестве продуктов биодеструкции кодеина фосфата в культуральной жидкости родококков, помимо кодеина (Rf×100 = 34), присутствовало четыре неидентифицированных вещества с Rf×100: 25; 43; 48; 71. Кроме того, в культуральной среде обнаружены два неидентифицированных соединения с Rf×100: 80 и 86.
Хроматографическую подвижность парацетамола, кодеина фосфата, дротаверина гидрохлорида и продуктов их биодеструкции как таковых, а также при совместном присутствии в составе комплексного препарата Но-шпалгин изучали в трехкратной повторности в выбранных оптимальных системах растворителей (табл. 5). Результаты параллельных определений считали сходимыми (repeatability) при условии:
│X1 - Xn│ < L(P, m)∙S. [1].
Данные табл. 6 свидетельствуют о повторяемости (сходимости) измерений коэффициентов подвижности парацетамола, кодеина фосфата, дротаверина гидрохлорида, препарата Но-шпалгин и продуктов их биодеструкции в оптимальных системах растворителей.
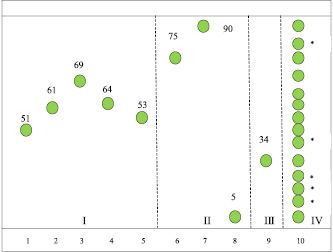
Хроматографическое поведение компонентов препарата Но-шпалгин и продуктов их биодеструкции в культуральных средах родококков в системе 3Н: I – свидетели парацетамола и продуктов его биодеструкции: 1 – парацетамол; 2 – пирокатехин; 3 – гидрохинон; 4 – бензохинон; 5 – п-аминофенол; II – свидетели дротаверина гидрохлорида и продуктов его биодеструкции: 6 – дротаверина гидрохлорид; 7 – 3;4-диэтоксибензальдегид; 8 – 3;4-диэтоксибензойная кислота; III – свидетель кодеина фосфата (9); IV – культуральная жидкость, содержащая Но-шпалгин и продукты его биодеструкции (10); * – неидентифицированные продукты биодеструкции (Rf×100: 11; 15; 25; 48; 80)
Таблица 5
Оценка повторяемости результатов параллельных определений коэффициентов подвижности компонентов препарата «Но-шпалгин» и продуктов их биодеструкции
|
Исследуемые вещества |
Метрологические характеристики (m = 3, Р = 95 %, L = 3,31) |
|||||
|
X1 |
X2 |
X3 |
|
S |
L×S |
|
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Парацетамол и продукты биодеструкции, система 8П |
||||||
|
Парацетамол |
55 |
55 |
54 |
54,67 |
0,46 |
1,52 |
|
п-Аминофенол |
51 |
50 |
52 |
51,00 |
1,0 |
3,31 |
|
Гидрохинон |
60 |
59 |
59 |
59,33 |
0,96 |
3,18 |
|
Бензохинон |
58 |
57 |
58 |
57,67 |
0,49 |
1,62 |
|
Пирокатехин |
73 |
74 |
71 |
72,67 |
1,26 |
4,17 |
|
Неидентифицированный продукт биодеструкции |
81 |
81 |
80 |
80,67 |
0,69 |
2,28 |
|
Кодеина фосфат и продукты биодеструкции, система 7К |
||||||
|
Кодеина фосфат |
36 |
36 |
36 |
36,0 |
0 |
0 |
|
14-Гидроксикодеинон |
53 |
53 |
54 |
53,33 |
0,93 |
3,07 |
|
Продукт биодеструкции № 1 |
28 |
28 |
26 |
27,33 |
1,15 |
3,80 |
|
Дигидрокодеин |
23 |
23 |
23 |
23,0 |
0 |
0 |
|
Продукт биодеструкции № 2 |
15 |
15 |
14 |
14,67 |
0,58 |
1,92 |
|
Дротаверина гидрохлорид и продукты биодеструкции, система 1Д |
||||||
|
Дротаверина гидрохлорид |
71 |
71 |
70 |
70,67 |
0,61 |
2,02 |
|
3,4-Диэтоксибензальдегид |
91 |
90 |
89 |
90 |
1,0 |
3,31 |
|
3,4-Диэтоксибензойная кислота |
80 |
80 |
79 |
79,67 |
0,68 |
2,25 |
|
Дротаверина гидрохлорид |
71 |
71 |
70 |
70,67 |
0,61 |
2,02 |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Препарат Но-шпалгин, система 3Н |
||||||
|
Парацетамол |
61 |
61 |
60 |
60,67 |
0,52 |
1,72 |
|
Кодеина фосфат |
34 |
34 |
32 |
33,33 |
1,29 |
4,27 |
|
Дротаверина гидрохлорид |
74 |
74 |
75 |
74,33 |
0,58 |
1,92 |
Примечания: Хn – экспериментально полученное значение Rf×100;  – среднее значение; S – стандартное отклонение; L – фактор, вычисленный по Пирсону L(P; m) при Р = 95 % [1].
– среднее значение; S – стандартное отклонение; L – фактор, вычисленный по Пирсону L(P; m) при Р = 95 % [1].
Заключение
Установлены оптимальные условия идентификации парацетамола, дротаверина гидрохлорида, кодеина фосфата и продуктов их биодеструкции в культуральных жидкостях родококков методом тонкослойной хроматографии. Получена повторяемость (сходимость) измерений коэффициентов подвижности исследуемых веществ. Показана возможность использования разработанной методики для идентификации компонентов комплексного лекарственного средства Но-шпалгин в культуральной жидкости родококков. Относительная простота и экспрессность методики обеспечивают ее использование в лабораторных условиях при изучении механизмов разложения лекарственных средств, а также при разработке способов высокоэффективного удаления их из сточных вод.
Рецензенты:
Хомов Ю.А., д.фарм.н., профессор кафедры фармацевтической химии ФЗО и ФДПО, ГБОУ ВПО «ПГФА» Минздрава России, г. Пермь;
Михайловский А.Г., д.фарм.н., профессор кафедры общей и органической химии, ГБОУ ВПО «ПГФА» Минздрава России, г. Пермь.
Работа поступила в редакцию 15.07.2014.
Библиографическая ссылка
Вихарева Е.В., Плотников А.Н., Мухутдинова А.Н., Мишенина И.И., Поспелова А.А., Тумилович Е.Ю. ИДЕНТИФИКАЦИЯ КОМПОНЕНТОВ КОМПЛЕКСНОГО ЛЕКАРСТВЕННОГО СРЕДСТВА НО-ШПАЛГИН И ПРОДУКТОВ ИХ БИОДЕСТРУКЦИИ В КУЛЬТУРАЛЬНЫХ ЖИДКОСТЯХ РОДОКОККОВ // Фундаментальные исследования. 2014. № 9-5. С. 1032-1037;URL: https://fundamental-research.ru/ru/article/view?id=35011 (дата обращения: 16.05.2026).




