Как известно, эндотоксикоз при перитоните ведет к выраженным изменениям показателей гомеостаза и способствует значительному ограничению возможности естественных детоксицирующих механизмов. Следствием этого является срыв компенсаторно-адаптационных возможностей [6], что в конечном итоге приводит к развитию полиорганной недостаточности [2], которая включает в себя синдром дыхательных расстройств, синдром печеночной и почечной недостаточности, инфекционно-токсический шок, расстройства сердечно-сосудистой системы и желудочно-кишечного тракта [5, 8].
При эндотоксикозе, сама концепция которого подразумевает полиорганность развивающейся патологии, миокард становится мишенью вторичного повреждения, вызванного эндогенными токсическими соединениями с комплексом морфофункциональных изменений [7].
В патогенезе поражения различных органов и систем при эндотоксикозе важнейшую роль играют мембранодеструктивные явления, которые приводят к структурным и функциональным изменениям в клетках и тканях [3]. В настоящее время доказано, что мембранодеструктивные процессы обусловлены интенсификацией процессов перекисного окисления липидов (ПОЛ), увеличением образования свободных радикалов и низкомолекулярных продуктов липопероксидации, а также гипоксией [1, 4].
С целью уменьшения выраженности мембранодеструктивных явлений при различных патологических процессах успешно применяют патогенетические схемы терапии, основанные на использовании препаратов антиоксидантного и антигипоксантного типа действия.
Цель исследования. Изучить кардиопротекторный липидрегулирующий эффект препаратов из различных фармакологических групп, обладающих антиоксидантным действием (аплегин, витамин Е, эмоксипин).
Материалы и методы исследования
В основу работы положены экспериментальные исследования на 48 взрослых беспородных половозрелых собаках обоего пола массой от 5,7 до 14 кг, разделенных для решения поставленных задач на четыре группы. Первая группа – контрольная (n = 12). При остром экспериментальном перитоните исследовали морфофункциональное состояние, качественный и количественный состав липидов, интенсивность ПОЛ, фосфолипазную активность тканевых структур миокарда, выраженность эндогенной интоксикации (ЭИ). Вторая группа – опытная (n = 12). Исследовали влияние аплегина на вышеуказанные компоненты гомеостаза при остром экспериментальном перитоните. Третья группа (n = 12). Диапазон изменений вышеуказанных компонентов гомеостаза изучали на фоне применения витамина Е. Четвертая группа (n = 12). В данной группе исследовались эффекты, возникающие при использовании эмоксипина.
Моделирование перитонита. Под общим обезболиванием (тиопентал-натрий 0,04 г/кг массы) животным в брюшную полость шприцем вводили 20 % каловую взвесь из расчета 0,5 мл/кг массы тела животного (Власов А.П., 1991). Через сутки после этой манипуляции животным выполняли срединную лапаротомию, оценивали возникшие патологические изменения в брюшной полости и санировали ее. В контрольные сроки (1, 3, 5 сутки) животным производили релапаротомию, биопсию ткани миокарда, осуществляли забор крови. Все экспериментальные исследования у животных выполнялись под общим обезболиванием.
В послеоперационном периоде экспериментальным животным проводили дезинтоксикационную (внутривенное введение 5 % раствора глюкозы и 0,89 % раствора хлорида натрия из расчета 50 мл/кг массы животного) и противовоспалительную (внутримышечные инъекции 2 раза в сутки раствора канамицина из расчета 15 мг/кг массы животного) терапию.
В опытных группах (вторая, третья и четвертая) животным в комплексную терапию включали лекарственные средства, обладающие антиоксидантным эффектом. Во второй группе животным ежедневно выполнялись внутривенные введения 10 % раствора аплегина из расчета 10 мг/кг массы тела, в третьей – внутримышечно вводился 10 % раствор альфа-токоферола ацетата из расчета 5 мг/кг; в четвертой – ежедневно внутривенно вводился 1 % раствор эмоксипина из расчета 10 мг/кг.
Липиды из биоптатов миокарда экстрагировали хлороформметаноловой смесью (Хиггинс Дж.А., 1990). Липиды фракционировали методом тонкослойной хроматографии на силикагелевых пластинах. Полярные фосфолипиды разделяли на пластинах фирмы Merk на стеклянной основе, нейтральные липиды фракционировали на силикагелевых пластинах для обращенно-фазной тонкослойной хроматографии (Хиггинс Дж.А., 1990; Vaskovsky V.E. et al., 1975). Молекулярный анализ липидов проводили на денситометре Model GS-670 (BIO-RAD, США) с соответствующим программным обеспечением (Phosphor Analyst/PS Sowtware).
Содержание малонового диальдегида (МДА) оценивали в реакции с 2-тиобарбитуровой кислотой. Для определения антиокислительной активности липидов предварительно проводили индукцию липопереокисления раствором сульфата железа в концентрации 5 мкмоль в течение часа. Активность супероксиддисмутазы (СОД) определяли по способности фермента тормозить аэробное восстановление нитросинего тетразолия до формазана (Гуревич В.С. и др., 1990; Досон Р. и др., 1991). Активность фосфолипазы А2 (Фл А2) оценивали в среде, содержащей 10 ммоль трис-HCL-буфер (pH 8,0), 150 ммоль тритон Х-100, 10 ммоль CaCl2 и субстрат (1,2 ммоль). В качестве субстрата использовали фосфатидилхолины яичного желтка. Регистрацию каталитической деятельности фермента проводили титрометрическим методом по мере образования свободных жирных кислот. Расчет проводили по калибровочной кривой, построенной по пальмитиновой кислоте, и выражали в мкмоль/с/г белка (Трофимов В.А., 1999). Электрокардиограмму (ЭКГ) регистрировали в стандартных отведениях на электрокардиографе ЭК ЭТ-01-«Р-Д». Концентрацию общего белка определяли по способу Бредфорд. Оценивали уровень молекул средней массы (МСМ) (Пикуза О.И., Шакирова Л.З., 1994). Определяли общую и эффективную концентрацию альбумина (Грызунов Ю.А., Добрецов Г.Е., 1994). Проводили световую микроскопию при окраске препаратов гематоксилин-эозином.
Полученные цифровые экспериментальные данные обработаны методом вариационной статистики с использованием t критерия Стьюдента. Вычисления и построение диаграмм, отражающих динамику изученных показателей, совершали с поддержкой программы Microsoft Excel XP. Применен текстовый процессор Microsoft Word XP.
Результаты исследования и их обсуждение
При моделировании острого перитонита в организме экспериментальных животных развивался синдром ЭИ. Отмечено повышение уровня как гидрофильных, так и гидрофобных токсических продуктов. Так, уровень молекул средней массы повышался более чем в 2 раза, индекс токсичности (ИТ) плазмы по альбумину возрастал в 2–4 раза, резерв связывания альбумина во все исследуемые сроки наблюдения был ниже исходного значения более, чем на 50 % (р < 0,05).
Развитие при перитоните синдрома ЭИ тесно коррелировало с интенсификацией процессов ПОЛ, активность которых более ярко представлена на организменном уровне.
После моделирования перитонита в плазме крови по отношению к исходу отмечалось увеличение уровня диеновых конъюгатов на 57,3 % (р < 0,05), триеновых конъюгатов – на 39,2 % (р < 0,05), МДА – на 69,5 % (р < 0,05), индуцированного МДА – на 114,3 % (р < 0,05), снижение активности СОД на 71,1 % (р < 0,05). Возрастала активность Фл А2 более чем в 10 раз (р < 0,05). Подтверждался факт зависимости степени выраженности ЭИ от накопления первичных и вторичных молекулярных продуктов липопереокисления и активации Фл А2.
На органном уровне (в ткани сердца) выраженность процессов ПОЛ отмечена в меньшей степени. При этом активность Фл А2 повышалась на 25,8 % (р < 0,05), а СОД снижалась на 42,5 % (р < 0,05).
Опыты показали, что в тканевых структурах миокарда при эндотоксикозе развиваются выраженные расстройства липидного обмена. Так, уровень эфиров холестерола уменьшался на 23,4 % (р < 0,05), а суммарных фосфолипидов – на 17,9 % (р < 0,05), в спектре которых выявлялись следующие изменения: уменьшение уровня сфингомиелина, фосфатидилсерина и фосфатидилинозита на 15,9; 26,8 и 17,6 % (р < 0,05) соответственно, что указывает на изменение состояния липидного бислоя мембран кардиомиоцитов, в частности его жидкостных свойств. На этом фоне происходило увеличение уровня моноацилглицерола на 9,5 % (р < 0,05), диацилглицерола – на 4,1 % (р < 0,05), свободных жирных кислот на 10,7 % (р < 0,05), лизофосфолипидов – на 282,1 % (р < 0,05), что указывает на развитие мембранодестабилизирующих процессов.
Выявленные изменения обуславливали и расстройства морфофункционального состояния миокарда, которые были представлены выраженными сосудистыми и дистрофическими изменениями. При изучении показателей ЭКГ оказалось, что число сердечных сокращений увеличивалось на 8,3 % (р < 0,05), амплитуда зубца Т уменьшалась на 27,5 % (р < 0,05). Также обнаруживалось достоверное уменьшение от нормы интервалов RR, PQ, QRS; зубцов S, Q.
Следовательно, при перитоните развивается выраженная ЭИ, наступает интенсификация процессов липопереокисления и активизация Фл А2, нарушается состав липидного бислоя кардиомиоцитов, что в конечном итоге ведет к функциональным расстройствам со стороны сердца. Наибольшая степень выраженности указанных нарушений регистрировалась в первые 3 суток эксперимента.
Традиционная терапия не обладает способностью быстро корригировать развившиеся нарушения гомеостаза. Даже на конечном этапе послеоперационного наблюдения (5 сутки) исследуемые показатели ЭИ достоверно отличались от исходных значений.
Во второй серии включение аплегина в схему комплексной терапии острого перитонита приводило к снижению интоксикации. Об этом свидетельствовали меньшие колебания исследуемых показателей ЭИ. При сравнительном анализе с результатами контрольной группы установлено, что через сутки после операции аплегин приводил к снижению содержания МСМ, ИТ и повышению уровня резерва связывания альбумина соответственно на 10,13, 28,76 и 26,67 % (р < 0,05). Причем к 5 суткам лечения показатели приближались к исходному значению, а их разрыв с контрольными результатами еще больше увеличивался.
Аплегин способствовал снижению процессов ПОЛ и уменьшал активность Фл А2, оказывал липидрегулирующий эффект. Однако его фармакологическое действие обнаруживалось лишь к 3–5 суткам.
На первом этапе наблюдения в плазме крови содержание диеновых конъюгатов уменьшалось незначительно, спустя 3 суток – их уровень продолжал снижаться и к конечному сроку наблюдения приближался к исходным значениям, но был отличен от таковых данных контроля. После первого введения аплегина активность Фл А2 в плазме крови оставалась повышенной. Не изменялся ее уровень и к третьим суткам наблюдения. Однако через 5 суток после санации брюшной полости активность Фл А2 в плазме крови снижалась на 23,9 % (р < 0,05).
Установлено, что аплегин оказывает влияние и на органном уровне – в ткани сердца. Нами отмечено, что при использовании препарата морфофункциональные изменения со стороны сердечной мышцы снижались, однако к конечному сроку наблюдения (пятые сутки) сохранялся слабо выраженный воспалительный процесс в миокарде, а исследуемые показатели функционального состояния сердечной мышцы не отличались от таковых контрольной группы.
При биохимической оценке выявлено, что через 3–5 суток применения препарата в тканевых структурах сердечной мышцы выраженность процессов ПОЛ уменьшалась, наблюдалось снижение активности Фл А2. При этом увеличивался антиоксидантный потенциал ткани сердца: активность СОД увеличивалась на 15,5 % (р < 0,05) (рис. 1).
Уменьшение активности ПОЛ и Фл А2 способствовало восстановлению липидного спектра структур миокарда. Наиболее существенным модификациям подверглись такие фракции липидов, как свободные жирные кислоты, лизофосфолипиды, фосфатидилхолин. Через трое суток на фоне применения аплегина уровень свободных жирных кислот падал на 27,6 % (р < 0,05), через пять суток – на 36,9 % (р < 0,05). Модификации подверглись и нейтральные липиды. Так, к пятым суткам уменьшался уровень моноацилглицеролов, диацилглицеролов на 35,4 и 16,8 % (р < 0,05) соответственно (рис. 2).
Таким образом, на фоне использования аплегина, за счет снижения интенсивности ПОЛ и депрессии Фл А2 происходит более быстрое, по сравнению с контролем, восстановление морфофункционального состояния миокарда. Однако наиболее полно эффект препарата реализуется лишь к конечному сроку применения.
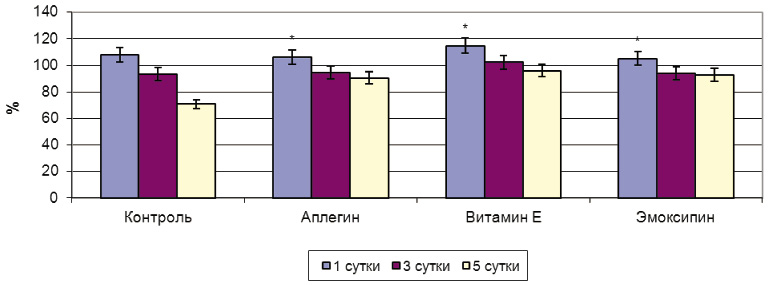
Рис. 1. Влияние антиоксидантов на активность фосфолипазы А2 ткани сердца при остром перитоните. Звездочкой отмечены данные, значение которых достоверно по отношению к норме
Включение в комплекс лечебных мероприятий при остром перитоните альфа-токоферола ацетата также способствовало снижению выраженности ЭИ, интенсивности ПОЛ и подавлению активности фосфолипазы А2. Влияние препарата прослеживается и на органном уровне. В тканевых структурах сердца на фоне его использования модифицируется как качественный, так и количественный состав липидов, что способствует восстановлению морфофункционального состояния миокарда.
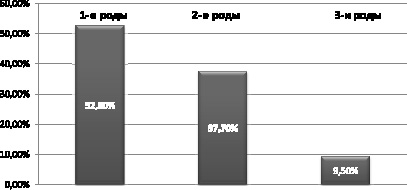
Рис. 2. Влияние антиоксидантов на уровень свободных жирных кислот миокарда при остром перитоните.
На фоне применения эмоксипина при лечении острого перитонита имело место уменьшение ЭИ, снижение интенсивности ПОЛ и подавление активности Фл А2. Важно отметить, что препарат нормализует липидный гомеостаз. В то же время выявляется разница воздействия препарата в различных средах. В плазме крови ряд эффектов начинает прослеживаться в первые сутки применения, а полноценное действие проявляется с 3 суток применения. На органном уровне существенное воздействие эмоксипина регистрируется с первых суток, а в последующем их эффективность не столь выражена.
Из изложенного вытекает, что использование препаратов, обладающих способностью корригировать интенсивность основных процессов, регулирующих морфофункциональное состояние биомембраны, является патогенетически обоснованным. Изучение фармакодинамики ряда из них (аплегин, витамин Е, эмоксипин) подтвердило данный факт. Использование их при ЭИ позволило уменьшить выраженность липидных перестроек в сердечной мышце, что, видимо, во многом и обусловило восстановление функциональных ее характеристик. Интересно отметить и тот факт, что указанные лекарственные средства кардиопротекторный липидрегулирующий эффект осуществляли не только за счет регулирования интенсивности процессов ПОЛ, но и за счет депрессии активности Фл А2.
Безусловно, в кардиопротекторном эффекте препаратов, обладающих антиоксидантным типом действия, определенную роль следует отнести и их способности снижать выраженность эндогенной интоксикации как одному из ведущих факторов, вызывающих каскад патофизиологических реакций, в том числе и со стороны сердца.
Выводы
1. При эндотоксикозе перитонеального генеза в тканевых структурах сердца возникают выраженные липидные перестройки, характеризующиеся модификацией качественного и количественного состава липидов, которые сопровождаются морфологическими и функциональными нарушениями в ткани сердца, интенсификацией процессов ПОЛ, повышением активности Фл А2 и снижением антиоксидантной защиты.
2. Применение при ЭИ препаратов, обладающих антиоксидантным действием (аплегин, витамин Е, эмоксипин), приводит к уменьшению морфофункциональных изменений в сердце. Кардиопротекторный эффект наиболее выражен у эмоксипина, менее – у аплегина и витамина Е.
3. Реализация кардиопротекторного эффекта используемых антиоксидантов четко прослеживается на их способности восстанавливать функциональные нарушения сердечной мышцы, что подтверждается увеличением амплитуды зубца Т, восстановлением уровня интервала SТ и уменьшением тахикардии.
4. Эффективность тестированных лекарственных средств в восстановлении функциональных изменений в сердце коррелирует с их способностью корригировать качественные и количественные изменения липидного спектра. На фоне использования препаратов отмечается снижение уровня свободных жирных кислот, лизофосфолипидов, повышение содержания суммарных фосфолипидов, фосфатидилхолина.
5. Кардиопротекторный липидрегулирующий эффект исследованных препаратов реализуется не только за счет уменьшения интенсивности процессов ПОЛ и повышения ферментного антиоксидантного потенциала тканевых структур миокарда, но и за счет депрессии активности Фл А2. Причем существенное влияние на фосфолипазную активность исследованных препаратов происходит после первого их введения.
Рецензенты:Смолькина А.В., д.м.н., профессор кафедры госпитальной хирургии медицинского факультета им. Т.З. Биктимирова, ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск;
Рубцов О.Ю., д.м.н., профессор кафедры факультетской хирургии, ФГБОУ ВПО «Мордовский государственный университет им. Н.П. Огарёва», г. Саранск.
Работа поступила в редакцию 14.03.2014.
Библиографическая ссылка
Лещанкина Н.Ю., Полозова Э.И., Радайкина О.Г., Васильев В.В., Турыгина С.А., Паршкова Т.Ю. СРАВНИТЕЛЬНЫЙ АНАЛИЗ ВЛИЯНИЯ АНТИОКСИДАНТОВ НА ЛИПИДНЫЙ ОБМЕН МИОКАРДА ПРИ ХИРУРГИЧЕСКОМ ЭНДОТОКСИКОЗЕ // Фундаментальные исследования. 2014. № 4-2. С. 291-295;URL: https://fundamental-research.ru/ru/article/view?id=33830 (дата обращения: 05.05.2026).



