Диагностика и лечение миомы матки – важная проблема современной гинекологии [1, 2, 3]. В зависимости от характера пролиферативных процессов в миоматозном узле выделяют морфологические формы миомы матки: простая и пролиферирующая. Разные гистологические типы миом обладают различным пролиферативным потенциалом, и, вследствие этого, требуют дифференцированного подхода к диагностике, лечению и профилактике возможных рецидивов. В современной медицинской практике актуальны методы компьютерного прогнозирования, призванные создать модель индивидуального течения заболевания, что позволяет оптимизировать лечебные мероприятия [7].
Цель ‒ разработка алгоритма дифференциальной диагностики простой и пролиферирующей миомы матки субсерозной локализации по данным ультразвукового исследования.
Материалы и методы исследования
На основании изучения результатов гистологического строения опухолей, полученных при хирургическом лечении 103 пациенток (в 73 случаях имела место простая миома, в 30 – пролиферирующая миома), репродуктивного возраста (средний возраст составил 34,2 ± 3,9 лет), оперированных по поводу миомы матки субсерозной локализации в Базовой акушерско-гинекологической клинике КубГМУ Минздрава РФ в период с 2009 по 2012 год, был проведен ретроспективный анализ эхографических, допплерографических, допплерометрических, гистографических показателей. Для определения диагностической ценности изучаемых параметров в качестве «золотого стандарта» использовали результаты, полученные при гистологическом исследовании удаленных миоматозных узлов. Исследование внутренних половых органов осуществляли на сканере PHILIPSHD-11. При эхографической визуализации опухолевидных образований матки определяли локализацию, форму, размеры, тип эхоструктуры. При помощи ЦДК визуально оценивали наличие кровотока, тип кровотока, количество цветовых локусов на единицу площади. При импульсной допплерометрии оценивали следующие показатели: максимальная систолическая скорость артериального кровотока (МАС), максимальная скорость венозного кровотока (МВС), пульсационный индекс (ПИ), индекс резистентности (ИР). При анализе гистограмм оценивали: среднее значение яркости в исследуемой и фоновой зонах, минимальные (Отклmin) и максимальные (Отклmax) отклонения в исследуемой и фоновой зонах, критерий эхооднородности исследуемой зоны (КЭО), критерий изоэхогенности исследуемой зоны (КИЗ). Критерий эхооднородности определяли по формуле
КЭО = ПОткл2 – Откл,
где ПОткл2 – погрешность отклонения в фоновой зоне (ПОткл2 = Отклmax – Отклmin); Откл – разница отклонений в исследуемой и фоновой зоне.
Критерий изоэхогенности исследуемой зоны определяли по формуле
КИЗ = |Срярк| – Откл2,
где |Срярк| – модуль разницы средних значений яркости в исследуемой и фоновой зонах; Откл2 – отклонение в фоновой зоне [9, 11].
Количественные переменные описывались следующими статистиками: числом пациентов, средним арифметическим значением, стандартным отклонением от среднего арифметического значения. Качественные переменные описывались абсолютными и относительными частотами (процентами). Различия считались статистически значимыми при уровне значимости p < 0,05. Для количественных переменных проводился тест на нормальность распределения при помощи критерия Шапиро–Вилка. Для сравнения двух групп нормально распределенных данных использовали t-критерий Стьюдента. При сравнении двух групп данных, распределение которых отличалось от нормального, применяли критерий Манна-Уитни в случае независимых признаков и критерий Вилкоксона для зависимых признаков. При анализе качественных признаков данные представляли в виде количественных признаков и анализировали с помощью критерия Фишера и критерия c-квадрат Пирсона. Чувствительность, специфичность показателей, а также их диагностическую ценность определяли при помощи ROC (Receiver Operator Characteristic)-анализа с последующим вычислением площади под ROC-кривой (AUC). Для разработки математической модели, позволяющей дифференцировать различные типы миомы матки, использовали логистический регрессионный анализ. Вероятность наступления события для некоторого случая рассчитывается по формуле
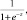
где –z = B1x1 + B2x2 + ... + Bnxn + С.
Качество приближения регрессионной модели оценивали при помощи функции правдоподобия, мерой которой служит отрицательное удвоенное значение логарифма этой функции (–2LL). Меру определенности, показывающую часть дисперсии выборки, которую можно объяснить с использованием исследуемой модели, оценивали при помощи критериев Кокса–Шела и Наделькеркеса. Проверку значимости коэффициентов проводили при помощи статистики Вальда (ZW), используя распределение χ-квадрат.
Из-за вовлечения в анализ большого количества переменных для упрощения модели проводили отбор переменных. Отбор переменных для математической модели осуществляли методом обратной селекции на основании статистики Вальда. То есть из первичной модели, включающей в себя все предикторы, пошагово исключались предикторы с наименьшим значением статистики Вальда. На каждом шаге данного алгоритма проводился расчет доли верно классифицированных наблюдений. Алгоритм остановился, когда исключение переменной с наименьшим значением статистики Вальда привело к статистически значимому снижению доли верно классифицированных случаев. Прогностическую ценность полученной регрессионной модели проверили при помощи ROC-анализа по указанной выше методике.
Расчет выполнен на персональном компьютере с использованием приложения Microsoft Excel 2010 (Microsoft Corp., USA), пакетов статистического анализа данных Statistica 8.0 for Windows (StatSoft Inc., USA), SPSS 15.0 (IBM, USA), Medcalc (MedCalcSoftware, Belgium).
Результаты исследования и их обсуждение
Согласно полученным данным, можно утверждать, что для пролиферирующей миомы субсерозной локализации характерен мультипиковый или сглаженный тип гистограммы, в то время как для простой миомы – гистограмма в виде одновершинного равностороннего или асимметричного треугольника. Тем не менее вид гистограммы не может являться единственным ультразвуковым предиктором типа субсерозной миомы, так как, обеспечивая высокую специфичность, составляющую 96,5 %, данный параметр обладает низкой чувствительностью – 51,25 %.
При анализе эхооднородности миоматозных узлов выявлено, что при простой миоме субсерозной локализации в 58 (78,8 %) случаях встречаются изоэхогенные узлы; гипо- и гиперэхогенные отмечены в 14 (19,2 %) наблюдениях; неоднородные – в 1 (1,4 %) случае. При пролиферирующей миоме преобладают гипо- и гиперэхогенные узлы – 22 (73,3 %) случая, неоднородные встречаются значительно реже – 5 (16,7 %) случаев. В 3 (10 %) наблюдениях – изоэхогенные узлы.
Если считать прогностическим признаком пролиферирующей миомы субсерозной локализации отличие эхогенности от окружающей ткани и неоднородность узла, то можно получить диагностический критерий с чувствительностью 81,2 % и специфичностью 78,7 %.
Различные типы гипо- или гиперэхогенных узлов, а также их частая встречаемость не позволяют производить однозначный прогноз, опираясь только на данные эхогенности. Эхогенность миоматозного узла является ценным прогностическим критерием, но для улучшения качества прогноза его необходимо использовать в комплексе с другими ультразвуковыми параметрами.
При анализе типа васкуляризации миоматозных узлов обнаружено: при простой миоме в 44 (60,3 %) случаях имел место периферический кровоток, что приблизительно в 1,7 раза чаще, чем единичный питающий сосуд (сосудистая ножка узла) – в 26 (35,6 %) наблюдениях; в 3 (4,1 %) случаях выявлен смешанный тип васкуляризации. В пролиферирующих миоматозных узлах преобладал смешанный тип – 14 (46,7 %) наблюдений, периферический тип васкуляризации встречается приблизительно в 1,4 раза реже – 10 (33,3 %); единичный питающий сосуд (сосудистая ножка) зарегистрирован в 6 (20 %) случаях. Таким образом, тип васкуляризации обладает хорошими прогностическими качествами, так как его специфичность достигает 85,6 %, чувствительность 72,5 %. Тем не менее рассмотрение дополнительных эхографических параметров при прогнозе типа субсерозной миомы привело к дальнейшему повышению точности результата.
Перед включением в вычислительный алгоритм количественные показатели были преобразованы указанным в табл. 1 образом.
Таблица 1
Коды качественных показателей
|
Параметр |
Частота |
Код параметра |
|
|
1 |
2 |
||
|
Вид гистограммы |
|||
|
Одновершинный |
33 |
1 |
0 |
|
Асимметричный |
46 |
0 |
1 |
|
Мультипиковый |
24 |
0 |
0 |
|
Эхогенность |
|||
|
Изоэхогенный |
44 |
1 |
0 |
|
Гипоэхогенный и гиперэхогенный |
36 |
0 |
1 |
|
Неоднородный |
23 |
0 |
0 |
|
Тип васкуляризации |
|||
|
Периферический |
51 |
1 |
0 |
|
Единичный питающий сосуд (сосудистая ножка) |
44 |
0 |
1 |
|
Смешанный |
8 |
0 |
0 |
При анализе количественных ультразвуковых, данных полученных при исследовании миоматозных узлов, выявлены высоко статистически значимые различия (p < 0,01) по следующим параметрам: увеличение максимального размера узла при динамическом наблюдении в течение 6 месяцев, количество цветовых пикселей на 1 см2, ИР в сосудах очаговых образований, Vmax в артериальных сосудах образований, VVmax венозного кровотока в узле. Между исследованными группами не получено статистически значимых (p = 0,660) различий размеров миоматозных узлов, ИР в маточных артериях, Vmax в маточных артериях, Vmax в отводящей маточной вене (табл. 2).
Рассмотренные выше качественные и количественные параметры были включены в модель многофакторной логистической регрессии. Исключение параметров, обладающих наименьшей диагностической ценностью, осуществлялось с помощью метода обратной селекции в соответствии со значением критерия Вальда.
При расчете было выполнено 8 шагов алгоритма, не более чем с 1000 итераций на каждом шаге. На 8 шаге при исключении параметра с наименьшим значением критерия Вальда происходило статистически значимое снижение качества приближения регрессионной модели, оцененное при помощи отрицательного удвоенного значения логарифма функции правдоподобия (–2LL). Кроме того, после выполнения 1000 итераций не удалось определить регрессионные коэффициенты модели с незначительными стандартными ошибками. Учитывая эти обстоятельства, алгоритм вычисления модели был остановлен на 8 шаге, за итоговую математическую модель, позволяющую диагностировать тип миомы матки, принята модель, полученная на шаге 7. Регрессионные коэффициенты приведены в табл. 3.
Таблица 2
Различия количественных ультразвуковых параметров между исследованными группами
|
Параметры |
Простая миома (n = 73) |
Пролиферирующая миома (n = 30) |
p |
|
Размеры миоматозных узлов, мм |
37,4 ± 6,3 |
38,3 ± 6,4 |
0,333 |
|
Прирост максимального узла при динамическом наблюдении, мм |
0,57 ± 0,19 |
1,40 ± 0,36 |
< 0,001 |
|
Количество цветовых пикселей на 1 см2 |
1,99 ± 1,47 |
5,12 ± 1,16 |
< 0,001 |
|
ИР в маточных артериях |
0,75 ± 0,10 |
0,70 ± 0,12 |
0,002 |
|
Vmax в маточных артериях, см/с |
39,2 ± 5,8 |
41,3 ± 5,9 |
0,015 |
|
Vmax в отводящих маточных венах |
16,8 ± 2,8 |
17,9 ± 3,7 |
0,020 |
|
ИР в сосудах очаговых образований |
0,71 ± 0,12 |
0,49 ± 0,23 |
< 0,001 |
|
Vmax в артериальных сосудах очаговых образований |
16,6 ± 3,6 |
27,3 ± 2,4 |
< 0,001 |
|
VVmax венозного кровотока в узле |
7,8 ± 1,8 |
11,1 ± 3,0 |
< 0,001 |
Таблица 3
Регрессионные коэффициенты переменных, использованных в конечном варианте модели
|
Параметр |
B |
Стандартная ошибка |
Статистика Вальда |
dF |
p |
|
Тип гистограммы |
11,106 |
2 |
0,004 |
||
|
Тип гистограммы (1) |
2,930 |
1,155 |
6,435 |
1 |
0,011 |
|
Тип гистограммы (2) |
0,245 |
0,895 |
0,075 |
1 |
0,784 |
|
Тип васкуляризации |
1,457 |
2 |
0,483 |
||
|
Тип васкуляризации (1) |
1,097 |
0,943 |
1,354 |
1 |
0,245 |
|
Тип васкуляризации (2) |
1,032 |
0,910 |
1,288 |
1 |
0,256 |
|
Увеличение размера узла за 6 месяцев |
–0,248 |
0,069 |
12,979 |
1 |
< 0,001 |
|
Коэффициент эхооднородности |
1,272 |
0,625 |
4,141 |
1 |
0,042 |
|
Количество цветовых пикселей |
–0,404 |
0,141 |
8,149 |
1 |
0,004 |
|
ИР в сосудах очаговых образований |
5,911 |
2,463 |
5,760 |
1 |
0,016 |
|
Константа |
–1,813 |
1,793 |
1,022 |
1 |
0,312 |
Наилучшая оценка качества подгонки уравнения по критерию Хосмера–Лемешова также получена на 7 шаге алгоритма. Достаточно высокий уровень значимости для модели показывает, что она хорошо откалибрована, достаточно точно описывает реальные данные и позволяет верно классифицировать 87,8 % процентов наблюдения.
Итоговая формула логистической регрессии:
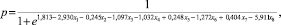
где x1 – код типа гистограммы 1; x2 – код типа гистограммы 2; x3 – код типа васкуляризации 1; x4 – код типа васкуляризации 2; x5 – увеличение размера за 6 месяцев, мм; x6 – коэффициент эхооднородности (0 – менее 0; 1 – более или равен 0); x7 – количество цветовых пикселей; x8 – ИР в сосудах очаговых образований.
При проведении проспективного исследования полученная на 7 шаге прогностическая модель обладала достаточно высокими операционными характеристиками прогностического теста: чувствительность модели – 87,3 %, специфичность – 95,0 %, эффективность – 81,1 %, прогностическая ценность положительного результата – 95,0 %, прогностическая ценность отрицательного результата – 87,3 %.
При проведении ROC-анализа также была показана очень высокая диагностическая эффективность разработанной модели. Площадь под ROC-кривой составила 0,950 (95 % ДИ 0,910 – 0,976, p < 0,0001).
Вывод
Таким образом, использование разработанной нами математической модели позволяет на основании комплексной оценки данных сонографии миоматозных узлов с высокой чувствительностью и специфичностью определять морфологический тип миомы матки, что было недоступно ранее при использовании отдельных ультразвуковых критериев.
Рецензенты:
Поморцев А.В., д.м.н., профессор, заведующий кафедрой лучевой диагностики, ГБОУ ВПО КубГМУ Минздрава России, г. Краснодар;
Астафьева О.В., д.м.н., доцент кафедры лучевой диагностики, ГБОУ ВПО КубГМУ Минздрава России, г. Краснодар.
Работа поступила в редакцию 04.02.2014.
Библиографическая ссылка
Бабкина А.В., Крутова В.А., Наумова Н.В. ВОЗМОЖНОСТИ ЭХОГРАФИИ В ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКЕ ПРОСТОЙ И ПРОЛИФЕРИРУЮЩЕЙ МИОМЫ МАТКИ СУБСЕРОЗНОЙ ЛОКАЛИЗАЦИИ // Фундаментальные исследования. 2014. № 2. С. 23-27;URL: https://fundamental-research.ru/ru/article/view?id=33537 (дата обращения: 15.05.2026).



