Основной задачей лекарственных средств, используемых в химиотерапии, является уничтожение раковых клеток при нанесении минимального урона здоровым элементам человеческого тела. Для достижения данной цели ученые стараются определить уникальные характеристики, свойственные злокачественным клеткам опухолей, отличающие данные элементы от здоровых тканей. Отдельные свойства раковых клеток могут служить целью для химиотерапевтических препаратов и отличать данные элементы от здоровых тканей. Одной из основных отличительных черт опухолей является быстрый рост и неконтролируемое размножение клеток [1, 2, 3, 4]. Вот почему резонно много внимания уделяется циклу размножения клетки и воздействию на отдельные стадии данного процесса. При химиотерапии больше всего страдают элементы, которые характеризируются быстрым ростом и размножением. Вышеупомянутая особенность становится очевидной при рассмотрении основных побочных эффектов данного метода лечения.
Цель исследования – провести анализ основных гематологических осложнений при применении различных методов полихимиотерапии.
Задача исследования: изучить частоту встречаемости отдельных гематологических симптомов при различных вариантах полихимиотерапии, а также эффективность лечения в возрастном и клиническом аспектах.
Материалы и методы исследования
В исследование было включено 122 больных с раком легкого. Возраст пациентов составил от 40 до 59 лет (средний возраст 47,2 ± 4,3 года), мужчин – 88 чел., женщин – 34 чел. Все пациенты были отнесены к трем группам.
Были выделены следующие подгруппы:
– получающие «традиционную» (этапную) химиотерапию (n = 50): возраст пациентов составил от 40 до 59 лет (средний возраст 45,3 ± 3,3 года), мужчин – 41 чел., женщин – 9 чел.;
– получающие таргетную терапию (n = 31): возраст пациентов составил от 40 до 59 лет (средний возраст 48,4 ± 4,4 года), мужчин – 25 чел., женщин – 6 чел.;
– получающие симптоматическое лечение (n = 41): возраст пациентов составил от 40 до 59 лет (средний возраст 50,1 ± 3,1 года), мужчин – 22 чел., женщин – 21 чел.
Результаты исследования и их обсуждение
Эффективность лечения у пациентов разных возрастных групп, получающих стандартную полихимиотерапию и таргетную терапию, представлена в табл. 1.
Как видно из табл. 1, у всех больных, получающих и стандартную полихимиотерапию, и таргетную терапию, полной регрессии заболевания не наблюдалось. Эффект проявлялся в виде частичной регрессии опухоли и/или метастазов, который и равнялся общей эффективности. Общий эффект у больных, получающих стандартную полихимиотерапию, составил 8,0 %. Среди больных, получающих таргетную терапию, общий эффект составил 16,1 %. Стабилизация опухолевого процесса в группе пациентов, получающих стандартную терапию, зафиксирована у 23 (46,0 %); в группе пациентов, получающих таргетную терапию, – у 13 (41,9 %).
Таблица 1
Эффективность лечения пациентов
|
Степень эффективности лечения |
Варианты терапии |
|||
|
Стандартная терапия (n = 50) |
Таргетная терапия (n = 31) |
|||
|
Абс. |
% |
Абс. |
% |
|
|
ПЭ |
0 |
0 |
0 |
0 |
|
ЧЭ |
7 |
14,0 |
5* |
16,1* |
|
СЗ |
23 |
46,0 |
13 |
41,9 |
|
ОЭ (ПЭ +ЧЭ) |
4 |
8,0 |
5* |
16,1* |
|
ПП |
16 |
32,0 |
8* |
25,8* |
Примечания:
ОЭ – общий эффект; ПП – прогрессирование; ПЭ – полный эффект; СЗ – стабилизация; ЧЭ – частичный эффект;
* – p < 0,05 между пациентами с таргетной и стандартной терапией.
Прогрессирование заболевания отмечено: у 16 (32,0 %) пациентов, получающих стандартную терапию и у 8 (25,8 %) пациентов, получающих таргетную терапию (рис. 1).
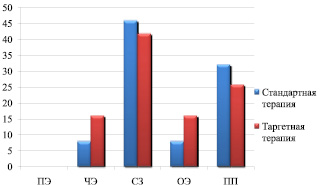
Рис. 1. Эффективность лечения при применении стандартной и таргетной полихимиотерапии
Таким образом, общий эффект у пациентов при применении таргетной терапии достоверно выше общего эффекта у пациентов, получающих стандартную полихимиотерапию. При этом прогрессирование процесса достоверно больше у больных, получающих стандартную полихимиотерапию.
Содержание лейкоцитов в крови у пациентов как в группе, получающих стандартную терапию, так и получающих таргетную терапию до начала лечения, было сопоставимо и составило, соответственно, 9,6 ± 0,3∙109/л и 9,0 ± 0,2∙109/л (табл. 2). В контрольный срок наблюдения (4 недели после окончания курса химиотерапии) эти показатели стали достоверно ниже (p < 0,05) и составили, соответственно, 3,8 ± 0,5∙109/л и 5,9 ± 0,3∙109/л. При этом снижение уровня лейкоцитов в группе пациентов, получавших стандартную терапию, было более значимым, чем среди пациентов, получавших таргетную терапию (p < 0,05) (рис. 2).
Содержание нейтрофилов в крови в обеих группах пациентов, получающих как стандартную терапию, так и таргетную терапию, до начала лечения было сопоставимо и составило, соответственно, 5,0 ± 0,3∙109/л и 4,9 ± 0,4∙109/л (табл. 3). В контрольный срок наблюдения эти показатели стали достоверно ниже (p < 0,05) и составили, соответственно, 2,1 ± 0,4∙109/л и 3,6 ± 0,1∙109/л; при этом у пациентов, получавших таргетную терапию, снижение уровня нейтрофилов было достоверно менее выраженным (p < 0,05) (рис. 3).
Таблица 2
Содержание лейкоцитов в крови больных раком легкого до и в процессе терапии
|
Вид терапии |
Динамика |
|
|
до начала лечения (∙109/л) |
во время лечения (∙109/л) |
|
|
Стандартная терапия |
9,6 ± 0,3 |
3,8 ± 0,5* |
|
Таргетная терапия |
9,0 ± 0,2 |
5,9 ± 0,3*,** |
Примечания:
* – p < 0,05 между показателями после лечения и до лечения;
** – p < 0,05 между показателями при таргетной терапии и стандартной терапии.
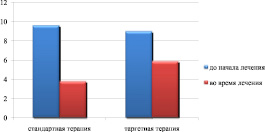
Рис. 2. Содержание лейкоцитов в крови больных раком легкого до и в процессе терапии
Таблица 3
Содержание нейтрофилов в крови больных раком легкого до и в процессе терапии
|
Вид терапии |
Динамика |
|
|
до начала лечения (∙109/л) |
во время лечения (∙109/л) |
|
|
Стандартная терапия |
5,0 ± 0,3 |
2,1 ± 0,4* |
|
Таргетная терапия |
4,9 ± 0,4 |
3,6 ± 0,1*,** |
Примечания:
* – p < 0,05 между показателями после лечения и до лечения;
** – p < 0,05 между показателями при таргетной терапии и стандартной терапии.
Содержание эритроцитов в крови у пациентов, как в группе стандартной терапии, так и в группе таргетной терапии, до начала лечения было сопоставимо и составило, соответственно, 3,6 ± 0,2∙1012/л и 3,8 ± 0,2∙1012/л (табл. 4). В контрольный срок наблюдения эти показатели стали достоверно ниже (p < 0,05) и составили, соответственно, 2,7 ± 0,3∙1012/л и 3,3 ± 0,2∙1012/л, при этом снижение уровня эритроцитов в группе пациентов, получавших стандартную терапию, было более значимым, чем среди пациентов, получавших таргетную терапию (p < 0,05) (рис. 4).
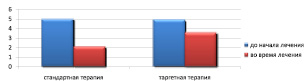
Рис. 3. Содержание нейтрофилов в крови больных раком легкого до и в процессе терапии
Таблица 4
Содержание эритроцитов в крови больных раком легкого до и в процессе терапии
|
Вид терапии |
Динамика |
|
|
до начала лечения (∙1012/л) |
во время лечения (∙1012/л) |
|
|
Стандартная терапия |
3,6 ± 0,2 |
2,7 ± 0,3* |
|
Таргетная терапия |
3,8 ± 0,2 |
3,3 ± 0,2*,** |
Примечания:
* – p < 0,05 между показателями после лечения и до лечения;
** – p < 0,05 между показателями при таргетной терапии и стандартной терапии.
Содержание тромбоцитов в крови у пациентов, как в группе стандартной терапии, так и в группе таргетной терапии, до начала лечения было сопоставимо и составило, соответственно, 215,7 ± 6,8∙109/л и 209,3 ± 5,2∙109/л (табл. 5). В контрольный срок наблюдения эти показатели стали достоверно ниже (p < 0,05) и составили, соответственно, 158,4 ± 9,0∙109/л и 187,5 ± 6,6∙109/л. При этом снижение уровня тромбоцитов в группе пациентов, получавших стандартную терапию, было более значимым, чем среди пациентов, получавших таргетную терапию (p < 0,05).
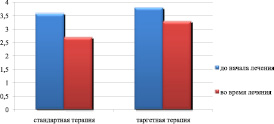
Рис. 4. Содержание эритроцитов в крови больных раком легкого до и в процессе терапии
Таблица 5
Содержание тромбоцитов в крови больных раком легкого до и в процессе терапии
|
Вид терапии |
Динамика |
|
|
до начала лечения (∙109/л) |
во время лечения (∙109/л) |
|
|
Стандартная терапия |
215,7 ± 6,8 |
158,4 ± 9,0* |
|
Таргетная терапия |
209,3 ± 5,2 |
187,5 ± 6,6*,** |
Примечания:
* – p < 0,05 между показателями после лечения и до лечения;
** – p < 0,05 между показателями при таргетной терапии и стандартной терапии.
Таким образом, уровень тромбоцитов во время лечения при применении таргетной терапии выше, чем при стандартной терапии (рис. 5).
Известно, что анализ только средних показателей содержания форменных элементов в сыворотке крови не отражает частоту гематологических осложнений. Изучение частоты таких осложнений показало следующее (табл. 6). Мы отмечали лейкопению у 13 пациентов, получавших стандартную терапию, что составило 26,0 %, и у 3 пациентов (9,7 %), получавших таргетную терапию, причем при назначении таргетной терапии лейкопения наблюдалась достоверно реже (p < 0,05).
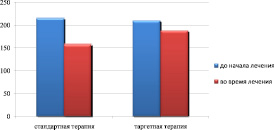
Рис. 5. Содержание тромбоцитов в крови больных раком легкого до и в процессе терапии
Такие же закономерности выявлены в отношении частоты нейтропении и тромбоцитопении. Нейтропения отмечалась у 10 пациентов (20,0 %), получавших стандартную терапию, и у 2 пациентов (6,5 %), получавших таргетную терапию, причем при назначении таргетной терапии нейтропения наблюдалась достоверно реже (p < 0,05). Тромбоцитопения диагностирована у 11 пациентов (22,0 %), получавших стандартную терапию, и у 2 пациентов (6,5 %), получавших таргетную терапию, причем при назначении таргетной терапии тромбоцитопения наблюдалась достоверно реже (p < 0,05).
Случаи анемии у пациентов, получавших стандартную и таргетную терапию, наблюдались у 6 (12,0 %) и 4 (12,9 %) соответственно. При этом отличий в частоте анемии в зависимости от вида терапии выявлено не было (p > 0,05).
Таблица 6
Гематологическая токсичность различных методов терапии рака легкого
|
Вид токсичности |
Виды терапии |
|||
|
Стандартная терапия (n = 50) |
Таргетная терапия (n = 31) |
|||
|
Абс. |
% |
Абс. |
% |
|
|
Лейкопения |
13 |
26,0 |
3* |
9,7* |
|
Нейтропения |
10 |
20,0 |
2* |
6,5* |
|
Анемия |
6 |
12,0 |
4 |
12,9 |
|
Тромбоцитопения |
11 |
22,0 |
2* |
6,5* |
Примечание. * p < 0,05 между показателями у пациентов, получающих таргетную и стандартную терапию.
Таким образом, полученные результаты позволяют сделать следующие выводы:
1) у всех больных, получающих и стандартную полихимиотерапию, и таргетную терапию, полной регрессии заболевания не наблюдалось;
2) при проведении стандартной терапии достоверно чаще встречались такие гематологические симптомы, как лейкопения, нейтропения, тромбоцитопения;
3) достоверных отличий в частоте анемии в зависимости от вида терапии выявлено не было.
Рецензенты:
Ильницкий А.Н., д.м.н., доцент, заместитель директора, АНО «НИМЦ «Геронтология», г. Москва;
Павлова Т.В., д.м.н., профессор, заведующая кафедрой патологической анатомии, ФГАОУ ВПО «Белгородский государственный национальный исследовательский университет», г. Белгород.
Работа поступила в редакцию 17.10.2013.
Библиографическая ссылка
Поляков И.С., Поляков И.С., Смагина М.В., Смагина М.В. К ВОПРОСУ О ГЕМАТОЛОГИЧЕСКИХ ОСЛОЖНЕНИЯХ РАЗЛИЧНЫХ ВАРИАНТОВ ХИМИОТЕРАПИИ РАКА ЛЕГКОГО // Фундаментальные исследования. 2013. № 9-5. С. 894-898;URL: https://fundamental-research.ru/ru/article/view?id=32787 (дата обращения: 05.05.2026).



