Нефтеполимерные смолы (НПС) – низкомолекулярные термопластичные полимеры, являющиеся составной частью более широкого класса материалов, углеводородных смол, получают полимеризацией непредельных соединений жидких продуктов пиролизанефтепродуктов. Одним из недостатков НПС является отсутствие в структуре функциональных групп, что существенно ограничивает области их применения.
Для улучшения свойств НПС, снижения себестоимости и повышения качества лакокрасочных покрытий на их основе проводят совместную полимеризацию тяжелых фракций продуктов пиролиза углеводородного сырья различного состава и температур выкипания под действием как радикальных, так и ионных катализаторов, что значительно расширяет ассортимент смол и, следовательно, области их применения. Так, совместной олигомеризацией алкенилароматических мономеров: стирола, винилтолуола, винил-м-ксилола, a-метилстирола, изо-пропенилтолуола и изо-пропенил-м-ксилола с изопреном в среде растворителей (алкилароматических углеводородов) в присутствии перекиси трет-бутила получены соолигомеры с температурой размягчения не более 40 °С, легко растворяющиеся в ароматических углеводородах и способные образовывать пленки с высокой адгезией к стеклу, металлу, дереву, которые после термообработки способны выдерживать температуру выше 200 °С [6]. А сополимеризацией циклопентадиеновых компонентов, замещенных винилароматических соединений и индена с исходным сырьем и последующим гидрированием полученных смол синтезированы НПС, пригодные в качестве адгезивов для белых и светлых теплостойких композиций [8]. В связи с необходимостью увеличения ресурсов синтетических пленкообразующих, работы по исследованию сополимеризации алкенилароматических соединений жидких продуктов пиролиза с полярными мономерами приобретают исключительную важность. Следует отметить, что при каталитической (катионной) полимеризации активны все непредельные углеводороды (стирол, a-метилстирол, винилтолуолы, инден, циклопентадиен, дициклопентадиен, изопрен и др.), входящие в состав фракций пиролиза. Однако акриловые мономеры, выбранные в качестве модифицирующих агентов, не способны полимеризоваться под действием катионных катализаторов, например, апротонных кислот (тетрахлорид титана) или алкилпроизводных металлов (триэтилалюминий, диэтилалюминий хлорид), образуя с ними комплексы, что было доказано методами криоскопического и диэлектрометрического титрования [11] и спектральными методами [1, 2, 11].
Экспериментально нами было установлено, что при сополимеризации комплексов «акриловый мономер – TiCl4» с мономерами фракций пиролиза образуются НПС с выходом 37…54 % [10]. Возможность сополимеризации, вероятно, связана с изменением дипольных моментов акриловых мономеров, со смещением электронной плотности или переносом заряда от одного компонента к другому при комплексообразовании. Изучение механизма сополимеризации непредельных соединений фракций с полярными мономерами (эфирами акриловой и метакриловой кислот) и исследование свойств полученных смол способствует более квалифицированным технологическим решениям в области получения модифицированных НПС.
Целью данной работы является теоретическое исследование состава и структуры комплексов «акриловый мономер – TiCl4» с помощью квантово-химических методов.
Материалы и методы исследования
Для моделирования комплексов различного строения и состава на основе метилакрилата (МА), как наиболее простой молекулы из рассматриваемых эфиров, и TiCl4, оценки изменения дипольных моментов и кратности образующихся связей в комплексах был выбран полуэмпирический метод РМ6 программы MOPAC 2009.
Результаты исследования и их обсуждение
Изучение строения органических соединений и механизма реакций тесно связано с использованием квантово-химических расчетов, позволяющих оценить электронное строение и геометрию молекул, суммарные заряды на атомах, энтальпию образования, изменение кратности двойной связи мономера в результате вхождения его в состав донорно-акцепторного комплекса [5]. В комплексах мономер обычно выступает как нуклеофильный агент, что влечет за собой перераспределение электронной плотности на атомах углерода двойной связи по сравнению со свободным мономером.
Существенная роль эффекта комплексообразования показана в процессах радикальной полимеризации. Присутствие комплексообразующих акцепторных агентов (солей лития, цинка) приводит к заметному повышению констант скорости реакции роста, что обусловлено повышением электрофильности двойной связи мономера, благоприятствующей его взаимодействию с макрорадикалами [5, 7]. Аналогичные или противоположные эффекты неизбежны и в ионных системах, т.к. активные центры ионного типа не менее чувствительны к смещению электронной плотности двойной связи мономера, чем радикалы. В реальных системах роль комплексообразования, по-видимому, сводится к перераспределению электронной плотности в молекуле мономера.
В синтезе модифицированных нефтеполимерных смол сополимеризацией непредельных соединений фракций жидких продуктов пиролиза с эфирами акриловой и метакриловой кислот принимают участие комплексы галогенида металла TiCl4 (акцептора) с эфиром (донором). Образование межмолекулярных связей в них осуществляется в основном в результате частичного переноса электрона (или смещения электронной плотности) от молекулы донора к молекуле акцептора. О степени переноса заряда можно судить по величине дипольного момента межмолекулярной связи, о прочности образующихся связей – по энтальпии образования комплексов [4]. Эти два параметра далее нами будут рассмотрены в качестве наиболее важных для характеристики образующегося комплекса «метилакрилат – TiCl4». На основании результатов исследования комплексов можно предложить механизм инициирования и роста цепи, т.е. объяснить возможность получения нефтеполимерных смол при использовании в качестве модифицирующих агентов мономеров, не способных полимеризоваться по катионному механизму.
Известно, что метилметакрилат способен образовывать окрашенный комплекс с SnCl4, который в отличие от комплексных соединений его со стиролом, инденом и другими мономерами этого типа является устойчивым [3]:
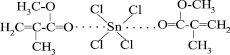
Методом диэлектрометрического титрования в работе [11] показано, что образование комплекса проходит постадийно: сначала при избытке TiCl4 образуется соединение состава 1:1, затем при дальнейшем добавлении донора – соединение состава 1:2.
Молекула метилакрилата в процессе комплексообразования с TiCl4 обладает двумя реакционными центрами: карбонильной и винильной группами. Поэтому существует возможность образования комплексов типа nV (n – неподеленная пара электронов карбонильной группы донора, V – вакантная орбита акцептора) или πV(p – электроны ненасыщенных связей донора). Также следует учитывать, что SnCl4 и TiCl4 дают с соединениями кислорода комплексы с координацией металла 5 (акцептор–донор) и 6 (донор–акцептор–донор) [9, 11] различной конформации: тетрагональной пирамиды, тригональной бипирамиды, октаэдрической конформации цис- и трансизомерных форм [4]. Для комплексов акриловых мономеров с TiCl4 возможно образование комплексов цис-конформаций, в которых донор выступает как бидентантный агент [5].
Рассчитанные характеристики исходных молекул и комплексов различного состава: эквимолярного (1:1), при избытке TiCl4 (1:2) и недостатке (2:1) и строения с учетом наличия двух реакционноспособных центров МА и возможных конформаций комплекса, представлены в табл. 1, 2.
Таблица 1
Энтальпии образования и пространственное строение комплексов TiCl4–метилакрилат различного состава
|
Номер комплекса |
Мольное соотношение TiCl4: МА |
Тип |
Энтальпия образования, ккал/моль (кДж/моль) |
Конформация |
|
1 |
2:1 |
nV, πV |
–439,70 (–1839,71) |
– |
|
2 |
1:1 |
πV |
–254,80 (–1067,61) |
Тригональная бипирамида |
|
3 |
1:1 |
nV |
–263,18 (–1101,16) |
Тригональная бипирамида |
|
4 |
1:1 |
бидентантный: nV, πV |
–257,72 (–1078,50) |
Октаэдрическая |
|
5 |
1:2 |
nV, nV |
–349,48 (–1462,23) |
Октаэдрическая транс |
|
6 |
1:2 |
nV, πV |
–349,70 (–1463,18) |
Октаэдрическая транс |
|
7 |
1:2 |
πV, πV |
–338,65 (–1416,92) |
Октаэдрическая транс |
|
8 |
1:2 |
nV, nV |
–349,48 (–1464,32) |
Октаэдрическая цис |
|
9 |
1:2 |
nV, πV |
–337,84 (–1415,55) |
Октаэдрическая цис |
Установлено, что энтальпия образования комплекса TiCl4–МА состава 2:1 (комплекс 1) максимальна, т.е. его образование энергетически невыгодно. Величины зарядов на атомах, кратности связей и дипольного момента для этого комплекса также показывают, что существование его маловероятно: заряды на атомах второй молекулы TiCl4 практически не меняются, следовательно, эта молекула не испытывает влияния молекулы-донора, т.е. в основном образуется комплекс состава 1:1.
Комплексы TiCl4–МА состава 1:1 имеют конформацию тригональной бипирамиды. Сравнивая энтальпии их образования, можно заключить, что комплексообразование идет в основном по карбонильной группе (комплекс 3, табл. 1). Изменение энтальпии образования (рисунок) при получении комплекса 2 (при сближении молекул TiCl4 и МА), которое протекает через состояние (S), имеющее минимальную энтальпию образования (–1101,64 кДж/моль), практически равную энтальпии образования комплекса 3 (–1101,16 кДж/моль), дополнительно подтверждает этот факт.
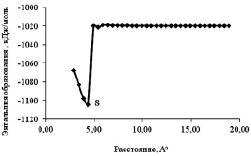
Изменение энтальпии образования при сближении молекул TiCl4 и МА
Получение бидентантного комплекса TiCl4–МА состава 1:1 октаэдрической конформации (комплекс 4) маловероятно, т.к. энтальпия образования его значительно выше (–1078,5 кДж/моль).
При дальнейшем добавлении донора (МА) идет образование шестикоординационных комплексов TiCl4–МА октаэдрической конформации цис- и транс- формы с координацией атома металла TiCl4 по карбонильной и двойной связи метилакрилата (комплексы 5–9, табл. 1). Минимальная энтальпия соответствует образованию комплексов цис-формы с координацией металла по карбонильной группе (комплекс 8, –1464,32 кДж/моль). Полученные результаты согласуются с результатами исследований комплексообразования TiCl4 с альдегидами (производные бензальдегида) и кетонами [12].
Энтальпия образования комплекса транс-формы (комплекс 6, – 1463,18 кДж/моль) с координацией по карбонильной и двойной связям близка к энтальпии образования комплекса 8, что позволяет сделать вывод о возможности образования цис- и трансизомеров комплексов, как было показано при исследовании комплексов TiCl4 с органическими сульфидами [4]. Далее рассмотрим эти два комплекса.
Таблица 2
Результаты расчетов комплексов ТХТ–МА
|
Номер комплекса |
Мольное соотношение TiCl4:МА |
Кратность связи |
Дипольный момент, Д |
||
|
Ti–C |
Ti–O |
C = C |
|||
|
1 |
0:1 |
– |
– |
1,954 |
2,507 |
|
2 |
1:1 |
0,002–0,007 |
0,435 |
1,924 |
6,907 |
|
3 |
1:1 |
0,001–0,007 |
0,435 |
1,928 |
8,075 |
|
4 |
1:1 |
0,001–0,011 |
0,385 |
1,937 |
9,700 |
|
6 |
1:2 |
0,007 |
0,417 |
1,935 |
8,023 |
|
0,002 |
0,438 |
1,928 |
|||
|
8 |
1:2 |
0,007 |
0,430 |
1,942 |
8,244 |
|
0,002 |
0,433 |
1,914 |
|||
Результаты выполненных расчетов (табл. 2) показывают, что дипольные моменты комплексов, в которых донорной является карбонильная группа, высоки и близки между собой (комплексы 3, 6, 8). Наиболее полярным является комплекс 4, в котором метилакрилат выполняет функцию бидентантного агента, но энтальпия образования этого комплекса выше, чем у остальных исследованных комплексов состава 1:1 (табл. 1). Полученные данные указывают на то, что вероятность образования комплексов с участием карбонильной группы выше, но это не исключает комплексообразование и по двойной связи.
Заключение
Комплексообразование приводит к поляризации p-электронов двойной связи, снижению кратности двойной связи, которая становится более электронодефицитной по сравнению с двойной связью в исходной молекуле мономера. В результате этого становится возможной сополимеризация полученного комплекса с мономерами жидких продуктов пиролиза (инденом, циклопентадиеном, стиролом и др.), имеющими избыток электронной плотности на двойной связи. Наиболее предпочтительным является взаимодействие комплекса с молекулами индена и циклопентадиена, имеющими более высокие значения дипольного момента (0,792 и 0,794 соответственно).
Результаты исследования сополимеризации акриловых мономеров с непредельными соединениями жидких продуктов пиролиза [10] согласуются с результатами расчетов.
Работа выполнена в рамках государственного задания «Наука» по теме 3.2702.2011.
Рецензенты:
Бакибаев А.А., д.х.н., профессор, заведующий кафедрой физической и аналитической химии, ФГБОУ ВПО «Национальный исследовательский Томский политехнический университет», г. Томск;
Пестряков А.Н., д.х.н., профессор, проректор по научной работе и инновациям, заведующий кафедрой технологии органических веществ и полимерных материалов, ФГБОУ ВПО «Национальный исследовательский Томский политехнический университет», г. Томск.
Работа поступила в редакцию 01.07.2013.
Библиографическая ссылка
Бондалетова Л.И., Бондалетов В.Г., Бондалетов О.В., Старцева К.С. КВАНТОВО-ХИМИЧЕСКИЕ РАСЧЕТЫ КОМПЛЕКСОВ МЕТИЛАКРИЛАТА С ТЕТРАХЛОРИДОМ ТИТАНА // Фундаментальные исследования. 2013. № 8-3. С. 551-555;URL: https://fundamental-research.ru/ru/article/view?id=31955 (дата обращения: 17.05.2026).



