Возможности варьирования свойств полимеров и создания на их основе иммобилизованных соединений позволяют разрабатывать лекарственные препараты с регулируемым высвобождением лекарственных веществ. Особенно актуально использование в этом направлении гидрофильных набухающих полимеров, обладающих не только формообразующей способностью, но и спектром функциональных свойств и высокой биосовместимостью с тканями макроорганизма, таких как полисахариды и аминополисахариды, к которым относятся хитин и хитозан [2, 7, 12].
Хитозан – поли-(1-4)-2-амино-2-дезокси-β-D-глюкоза получают при удалении ацетильной группы из положения С2 в хитине в результате обработки его в жестких условиях раствором щелочи. Появление в каждом элементарном звене макромолекулы свободной аминогруппы придает хитозану свойства полиэлектролита, одним из которых является характерный для растворов полиэлектролитов эффект полиэлектролитного набухания – аномального повышения вязкости разбавленных растворов при уменьшении концентрации полимера [1, 3, 6, 13].
Физико-химические и биологические свойства данного полимера и публикуемые результаты клинического применения позволяют рассматривать хитозан и его производные перспективными веществами для получения лекарственных препаратов с различным фармакотерапевтическим действием [1, 13]. Вместе с тем изучению функциональных и технологических показателей хитозана посвящено ограниченное число работ [8].
Лучшим видом сырья для получения хитина и хитозана считается крупка из панциря краба камчатского (Paralithodes camtschaticus), позволяющая получить хитозан высокого качества с большим выходом готового продукта. Другими источниками могут служить гладиус кальмара и сепион каракатицы, куколка шелкопряда, кутикула тараканов, биомасса микроорганизмов, диатомовые водоросли, пчелиный подмор, панцирь речного рака, отходы промышленного производства вешенки обыкновенной [1, 3, 10, 13].
Значительный резерв сырья для получения хитозана представляют запасы озерного рачка-бокоплава гаммаруса (Gammarus lacustris), принадлежащего к типу членистоногих, подтипу ракообразных, который обитает в озерах Южного Урала, Западной Сибири и Казахстана. Благодаря высокой способности рачка гаммарус к размножению сырье является возобновляемым и потенциально значимым в регионе для получения хитина и хитозана. Относительно высокое содержание (25–30 %) и малая толщина (100–500 мкм) панциря облегчают процесс его диспергирования, необходимого при всех способах получения хитина [3, 13]. Все вышеизложенное позволяет рассматривать хитозан гаммаруса как перспективное вспомогательное вещество для производства лекарственных препаратов, что и определило направление наших исследований.
Цель работы – получение хитозана из гаммаруса и определение его физико-химических и технологических свойств для нормативной документации и определения направлений использования в фармацевтической технологии.
Материалы и методы исследования
Хитозан получали из рачка гаммарус по реакции дезацетилирования хитина согласно методике, описанной в патенте [11].
Спектрофотометрию в инфракрасной области проводили в лаборатории Алтайского центра контроля качества и сертификации ЛС на ИК–Фурье спектрометре «Infralum FТ – 801». Подготовку образцов для исследования проводили по методике ОФС 42-0043-07 ГФ XII изд. [4]. Результаты исследования обрабатывали с использованием программы «ZaIR» для «Windows». Элементный состав (CHN) хитозана гаммаруса определяли по газообразным продуктам сгорания на хроматографе Thermo- Electron с программным обеспечением Eager 300, преобразующим результаты в процентное содержание азота, углерода и водорода в образце [3].
Степень дезацетилирования хитозана устанавливали колориметрическим способом по методике, описанной в работе [9], основанной на определении оптической плотности растворов нингидрина, в который вносили навески хитозана от 2 до 10 мг.
Вязкость растворов хитозана устанавливали вискозиметрически при температуре 25 °С в уксусной кислоты растворе водном 2 % согласно методике, описанной в ОФС 42-0038-07 [4]. Определение характеристической вязкости образцов хитозана позволило рассчитать среднюю молекулярную массу [3], по уравнению: [η] = 1,38∙10–4 Мw0,85.
Определение остаточного белка в хитозане проводили по методике ГФ ΧII, ч. 1, ОФС 42-0053-07 «Определение белка колориметрическим методом с биуретовым реактивом» [4].
Удельную поверхность хитозана устанавливали по методике, описанной в [8], согласно которой величина адсорбции 45 мг метиленового синего соответствует примерно 700 м2 поверхности.
Технологические свойства хитозана определяли по стандартным методикам. Ситовой анализ проводили по ОФС 42-0136-09, ГФ XII, ч. 2, используя набор сит с величиной отверстия 7,1; 5,6; 5,0; 4,5; 3,5; 3,0; 2,5; 1,0; 0,25 мм. Влагосодержание полимера определяли по ОФС 42-0087-08 «Потеря в массе при высушивании». Сыпучесть хитозана оценивали на приборе ВП-12А. Насыпной объем порошков определяли по методике ОФС 42-0137-09 на вибрационном уплотнителе порошков модели 545р-АК-3 ЖЗТО [5].
Результаты исследованияи их обсуждение
Рачок гаммарус содержит до 6 % хитина, который выделяли путем последовательной обработки сырья 3 % раствором пероксида водорода, раствором хлороводородной кислоты 0,6 моль/л, раствором натрия гидроксида 0,175 моль/л. Каждую стадию сопровождали промыванием сырья до нейтральной реакции промывных вод (рН = 7). Выделенный хитин промывали этанолом и ацетоном под вакуумом до полного извлечения пигментов и высушивали. Затем проводили дезацетилирование хитина натрия гидроксида раствором 50 % при температуре 120–130 °С в течение одного часа в инертной среде. Для окончательной очистки хитозан промывали этанолом и ацетоном, высушивали на воздухе. Из 400 г исходного сырья (гаммарус) получили 25,13 г хитина, а после дезацетилирования 15,9 г хитозана. Выход хитозана по хитину составил 79,8 % от теоретического.
Хитозан, полученный из гаммаруса, представлял собой светло-желтый мелкий порошок без запаха, не растворимый в воде очищенной, и натрия гидроксида растворе 10 %, частично набухающий в названных растворителях с образованием на поверхности частиц полимера гелеобразной оболочки. Образец хитозана гаммаруса растворим в минеральных кислотах, легко растворим в органических кислотах.
Идентификация хитозана гаммаруса проведена по элементному составу и ИК-спектрам. Элементный анализ (табл. 1) показал, что для хитозана, выделенного из рачка гаммарус, характерно такое же соотношение углерода, водорода и азота, как и для хитозана из краба камчатского, и оно близко к вычисленному по формуле хитозана соотношению названных элементов. Как известно, хитозан из морских ракообразных отличается от хитина более низким содержанием углерода и более высоким содержанием азота (в хитине содержание углерода – 47,3 %; водорода – 6,4 %; азота – 6,9 %), данная особенность наблюдается и в хитозане из гаммаруса.
Таблица 1
Содержание углерода, водорода и азота в хитозане
|
Источник хитозана |
Углерод, % |
Водород, % |
Азот, % |
|
Вычислено по формуле |
44,7 |
6,9 |
8,7 |
|
Краб камчатский |
43,7 |
6,4 |
7,4 |
|
Рачок гаммарус |
43,8 |
6,3 |
7,3 |
Для сравнительной характеристики структуры полимера снимали ИК-спектр хитозана гаммаруса и крабообразных, предоставленный ЗАО «Эвалар» (рисунок).
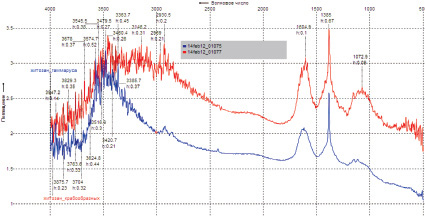
ИК-спектр хитозана гаммаруса (1) и хитозана крабообразных (2)
В ИК-спектре хитозана наблюдаются характерные полосы поглощения в областях 3500–3300 см–1 и 1390–1000 см–1, которые свидетельствуют о присутствии NH2-группы. При этом поглощение в области 3500–3300 см–1 вызвано колебанием связи N–Н, а в области 1360–1000 см–1 у всех типов аминов появляются полосы поглощения, вызванные участием С–N связи в скелетных колебаниях молекулы. В образце хитозана гаммаруса зарегистрированы полосы с максимумами при 1433 см–¹ деформационного колебания СН2- и СН3-групп, 1373 см–¹ (перегиб) деформационного колебания ОН-связи. В образце хитозана крабообразных наблюдается широкая полоса средней интенсивности в области 1320–1387 см–¹, соответствующая колебанию ОН-связи [3,11].
Анализ ИК-спектров показал идентичность химического строения обоих образцов хитозана. Относительно широкий разброс характеристических полос по волновым числам может быть обусловлен структурно-молекулярной неоднородностью исследуемых материалов.
Таблица 2
Сравнительная характеристика физико-химических свойств хитозана рачка гаммарус и хитозана крабообразных
|
Физико-химические характеристики |
Допустимый интервал |
Хитозан гаммаруса |
Хитозан крабообразных |
|
Степень дезацетилирования, % |
Не менее 75 |
89,5 ± 0,15 |
70,0 ± 0,20 |
|
Вязкость растворов в 2 % уксусной кислоте, Дл/ г |
4–30 |
17,9 |
12,0 |
|
Удельная поверхность, м2/г |
1–200 |
21,6 ± 0,50 |
7,88 ± 0,23 |
|
Минеральный остаток (зольность), % |
Не более 0,5 |
0,69 ± 0,038 |
0,36 ± 0,063 |
|
Остаточный белок, % |
Не более 0,1 |
0,05 ± 0,025 |
0,49 ± 0,038 |
|
Средняя молекулярная масса |
1,0·106–1,4·106 |
1,38·106 |
1,29·106 |
|
Уровень кислотности, рН |
6,8–7,3 |
7,1 ± 0,25 |
7,3 ± 0,25 |
Хитозан из рачка гаммарус обладает физико-химическими свойствами, характерными для хитозана крабообразных (табл. 2), при этом образует в уксусной кислоте растворе 2 % более вязкие растворы (17,9 и 12,0 Дл/г соответственно), обладает выраженными сорбционными свойствами по отношению к метиленовому синему – маркеру низко- и среднемолекулярных токсинов, модели лекарственных средств (21,6 ± 0,50 м2/г). Данные функциональные свойства хитозана гаммаруса позволяют рассматривать его как перспективное вспомогательное вещество для получения лекарственных форм в виде гелей, а также матрицы-носителя лекарственных веществ в иммобилизованных лекарственных формах.
Таблица 3
Фракционный состав хитозана гаммаруса
|
Размер частиц, мм |
Содержание, % |
Размер частиц, мм |
Содержание, % |
||||||||
|
Серия |
Серия |
||||||||||
|
1 |
2 |
3 |
4 |
5 |
1 |
2 |
3 |
4 |
5 |
||
|
> 7,1 |
5 |
5 |
8 |
6 |
- |
> 3,0 < 3,5 |
3 |
4 |
5 |
3 |
6 |
|
> 5,6 < 7,1 |
8 |
7 |
10 |
3 |
- |
> 2,5 < 3,0 |
6 |
7 |
8 |
2 |
11 |
|
> 5,0 < 5,6 |
8 |
8 |
8 |
4 |
1 |
> 1,0 < 2,5 |
35 |
38 |
20 |
35 |
53 |
|
> 4,5 < 5,0 |
3 |
3 |
5 |
1 |
1 |
> 0,25 < 1,0 |
18 |
20 |
16 |
40 |
21 |
|
> 3,5 < 4,5 |
4 |
2 |
5 |
3 |
1 |
< 0,25 |
10 |
6 |
15 |
3 |
2 |
Таблица 4
Технологические свойства хитозана гаммаруса
|
Серии хитозана |
Насыпной объем, кг/м3 |
Сыпучесть, г/с |
Потеря в массе при высушивании, % |
|
Серия 1 |
80,45 ± 0,460 |
0,372 ± 0,006 |
6,52 ± 0,76 |
|
Серия 2 |
108,11 ± 1,028 |
0,466 ± 0,027 |
6,87 ± 0,16 |
|
Серия 3 |
89,69 ± 0,500 |
0,234 ± 0,005 |
5,29 ± 0,08 |
|
Серия 4 |
96,91 ± 2,137 |
0,420 ± 0,020 |
8,43 ± 0,29 |
|
Серия 5 |
146,64 ± 2,043 |
1,040 ± 0,060 |
8,26 ± 0,28 |
Изучение технологических свойств хитозана гаммаруса показало, что он имеет неоднородный состав с доминирующей фракцией частиц 0,25–2,5 мм, влагосодержанием от 5,29 ± 0,08 до 8,43 ± 0,29 %, с очень малой насыпной массой от 80,45 ± 0,460 до 146,64 ± 2,043 кг/м3 и плохой сыпучестью менее 1,0 г/с.
Заключение
Сравнительная характеристика физико-химических свойств хитозана рачка гаммарус и хитозана крабообразных свидетельствует об их близкой химической природе и молекулярной структуре. Показатели вязкости раствора хитозана в уксусной кислоте растворе 2 % и сорбционная способность по метиленовому синему позволяют рассматривать хитозан гаммаруса как перспективное вспомогательное вещество для получения лекарственных форм в виде гелей и матрицы-носителя в иммобилизованных лекарственных формах. Технологические показатели характеризуют хитозан гаммаруса как полиморфную систему с доминирующей фракцией частиц 0,25–2,5 мм, влагосодержанием не более 10 %, с очень малой насыпной массой и плохой сыпучестью, что необходимо учитывать в процессе переработки и создания лекарственных форм.
Рецензенты:
Новоженов В.А., д.х.н., профессор, зав. кафедрой неорганической химии, ФГБОУ ВПО «Алтайский государственный университет» Министерства образования и науки России, г. Барнаул;
Федосеева Л.М., д.фарм.н., профессор, зав. кафедрой фармацевтической химии с курсом органической и токсикологической химии, ГБОУ ВПО «Алтайский государственный медицинский университет» Минздрава России, г. Барнаул.
Работа поступила в редакцию 08.05.2013.
Библиографическая ссылка
Гартман О.Р., Воробьева В.М. ТЕХНОЛОГИЯ И СВОЙСТВА ХИТОЗАНА ИЗ РАЧКА ГАММАРУС // Фундаментальные исследования. 2013. № 6-5. С. 1188-1192;URL: https://fundamental-research.ru/ru/article/view?id=31713 (дата обращения: 02.05.2026).



