Диагностика повреждений передней крестообразной связки коленного сустава клиническим методом зачастую вызывает значительные затруднения. Анамнез травмы не несет значительной информации, поскольку у пациентов с дегенеративной патологией усилие, необходимое для разрыва связки,может быть минимальным [5]. У пациентов, ведущих активный образ жизни, повреждение, напротив, возникает при значительных нагрузках и затрагивает несколько структур коленного устава, сопровождаясь при этом выраженным гемартрозом и отёком периартикулярных тканей [1, 6]. Степень выраженности клинических симптомов в остром периоде может быть также различна и зависит от индивидуальных особенностей пациента. Так, непосредственно после травмы выявить переднюю нестабильность коленного сустава затруднительно вследствие рефлекторного напряжения мышц бедра и отёка тканей, которые затрудняют визуализацию смещения голени кпереди при проведении стандартных диагностических тестов [3]. Дополнительные неинвазивные методы обследования (рентгенография, ультрасонография, магнитнорезонансная томография) также не всегда позволяют достоверно установить повреждение передней крестообразной связки, что подтверждается достаточно высоким количеством расхождений их результатов с данными артроскопии.
Вопрос о выборе материала для восстановления передней крестообразной связки остаётся дискутабельным. Сторонники использования собственных тканей указывают на отсутствие аллергических реакций; возможность с течением времени полной интеграции связки с восстановлением не только биомеханических, но и проприоцептивных свойств; относительно низкую травматичность забора тканей из донорского места с применением современных технологий; похожие прочностные показатели близких по структуре тканей, применяемых для пластики. Оппоненты утверждают, что помещенные в сустав аутотрансплантанты интегрируются лишь частично, их кровоснабжение и иннервация не восстанавливается и рассчитывать на полноценную реконструкцию связки не приходится. Доказано, что прочность аутотрансплантата со временем уменьшается, при этом современный синтетический протез обладает постоянными характеристиками [1, 3].
Таким образом, нерешённые проблемы диагностики повреждений передней крестообразной связки коленного сустава и практические трудности в оценке функционального состояния ее протеза при оперативном восстановлении с учетом послеоперационных изменений в окружающих тканях явились основанием для изучения возможностей однофотонной эмиссионной томографии коленного сустава у данной категории пациентов.
Цель исследования: изучение возможностей однофотонной эмиссионной томографии для диагностики повреждении ПКС коленного сустава и оценки послеоперационных изменений в тканях при ее оперативном восстановлении.
Материал и методы исследования
В исследовании принимали участие 4 пациента. Первый пациент, мужчина 29 лет, не имел повреждения ПКС (условно здоров). Второй пациент, мужчина 30 лет, со свежим (менее 3 недель) разрывом передней крестообразной связки (диагноз верифицирован артроскопически). Третий пациент, мужчина 47 лет, обследован через 10 месяцев после артроскопического протезирования передней крестообразной связки синтетическим протезом из полиэтилентерефтолана размерностью 80 волокон с фиксацией титановыми интерферентными винтами производства «Остеомед», Россия. Четвёртый пациент, женщина 37 лет, обследована через 3 месяца после пластики передней крестообразной связки трансплантатом из собственной связки надколенника, фиксированным биодеградируемыми интерферентными винтами из полимолочной кислоты «De Puy», США.
Всем пациентам был внутривенно введён изотоп: Тс-99м, 700 МБк, фосфотех. Первым двум исследуемым произведена однофотонная эмиссионная томография скелета в режиме «всё тело», последующим – однофотонная эмиссионная трёхфазная томография коленных суставов. Лучевая нагрузка – 4,0 мЗв. Радионуклидное исследование костной системы получено при выполнении 3-фазной сцинтиграфии: первая фаза – стадия оценки кровотока, начинается непосредственно после внутривенного введения 700 МБк радиофармпрепарата. Детектор гамма-камеры при этом располагается над областью коленного сустава и проводится динамическая запись в течение 60 секунд (2 секунды на 1 кадр). Вторая фаза – стадия оценки кровенаполнения, статическая сцинтиграфия с набором 500000 импульсов выполняется через 5–10 минут после первой фазы без смены положения детектора. Третья фаза – статическое исследование костей скелета, при котором сцинтиграммы получают через 3–4 часа после инъекции радиофармпрепарата [2, 4].
Результаты исследования и их обсуждение
У пациента без повреждения ПКС на сцинтиграммах костной системы на момент обследования очаги патологического включения радиофармпрепарата не визуализируются. Во всех отделах скелета накопление радиофармпрепарата относительно равномерное, без особенностей (рис. 1).
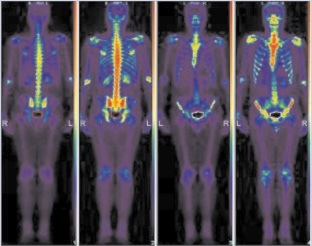
Рис. 1. Накопление радиофармпрепарата у пациента без повреждения передней крестообразной связки
У пациента со свежим разрывом передней крестообразной связки на момент обследования присутствовали жалобы на периодическое чувство «нестабильности коленного сустава», сопровождающееся болевыми ощущениями. На сцинтиграммах визуализируется очаг патологического включения радиофармпрепарата в проекции соответствующего коленного сустава, что не указывает прямо на разрыв передней крестообразной связки, однако может служить важным косвенным признаком повреждения в остром периоде травмы (рис. 2).
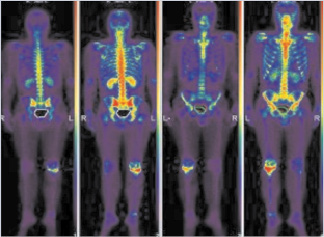
Рис. 2. Накопление радиофармпрепарата в области мыщелков левой большеберцовой кости у пациента с разрывом передней крестообразной связки.
Пациент с синтетическим протезом передней крестообразной связки справа жалоб на момент обследования не предьявлял. На остеосцинтиграммах диффузно повышенная аккумуляция радиофармпрепарата визуализируется в проекции правого коленного сустава и соответствует местам расположения титановых интерферентных винтов, отражая нормальную перифокальную реакцию костной ткани на имплантат. На наш взгляд, подобная картина может являться примером стабильного положения фиксаторов ПКС в костной ткани с отсутствием выраженной воспалительной реакции на них (рис. 3).
При исследовании пациентки с пластикой передней крестообразной связкой из собственной связки надколенника через 3 месяца после операции было выявлено повышение кровотока (в 1,93 раза в сравнении со здоровой стороной) и кровенаполнения (в 2,21 раза) в оперированном суставе с последующим усилением очаговой аккумуляции радиофармпрепарата при однофотонной эмиссионной трёхфазной томографии (рис. 4, рис. 5). При этом у больной присутствовали жалобы на отёчность сустава и боли в области донорского места трансплантата в проекции надколенника.
Повышенный кровоток и кровенаполнение в области исследуемого сустава, на наш взгляд, соответствует клинической картине умеренного синовиита, сохраняющегося вследствие высокой травматичности данной методики пластики передней крестообразной связки. Накопление радиофармпрепарата в надколеннике может свидетельствовать о нормальной регенерации костной ткани в донорском месте трансплантата передней крестообразной связки.
В процессе исследования выявлено, что результаты сцинтиграфии чётко соответствуют анамнезу и клинической картине. Данные, полученные при обследовании пациентов, позволяют оценить интенсивность кровоснабжения тканей коленного сустава, выявить очаги накопления радиофармпрепарата и степень его аккумуляции в сравнении с контрлатеральным суставом.
Выводы
1. Однофотонная эмиссионная (трёхфазная) томография коленного сустава позволяет выявить косвенные признаки повреждения передней крестообразной связки в остром периоде травмы, что позволяет повысить качество диагностики на фоне невысокой информативности традиционных методов дополнительного обследования.
2. Однофотонная эмиссионная (трёхфазная) томография коленного сустава пригодна для оценки послеоперационных изменений в тканях коленного сустава при пластике передней крестообразной связки синтетическим или аутотрансплантатом, ее возможности требуют дальнейшего изучения.
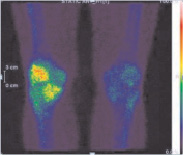
Рис. 3. Однофотонная эмиссионная трёхфазная томография коленных суставов пациента с синтетическим протезом передней крестообразной связки без признаков нестабильности
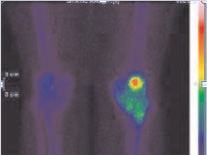
Рис. 4. Очаг накопления радиофармпрепарата в области донорского места трансплантата в проекции надколенника
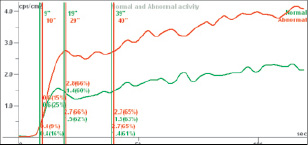
Рис. 5. Накопление изотопа при трёхфазной однофотонной эмиссионной томографии у пациентки после пластики передней крестообразной связки аутотрансплантатом
Рецензенты:
Сергеев К.С., д.м.н., профессор, заведующий кафедрой травматологии, ортопедии и ВПХ, ГБОУ ВПО «Тюменская государственная медицинская академия» Министерства здравоохранения РФ, г. Тюмень;
Атманский И.А., д.м.н., профессор, заведующий кафедрой травматологии и ортопедии, ГБОУ ВПО «Челябинская государственная медицинская академия» Министерства здравоохранения РФ, г. Челябинск.
Работа поступила в редакцию 08.04.2013.
Библиографическая ссылка
Чмутов А.М., Астапенков Д.С., Люкова Л.И., Плотников К.А. ПЕРВЫЙ ОПЫТ ОДНОФОТОННОЙ ЭМИССИОННОЙ ТОМОГРАФИИ ПРИ ПОВРЕЖДЕНИЯХ ПЕРЕДНЕЙ КРЕСТООБРАЗНОЙ СВЯЗКИ КОЛЕННОГО СУСТАВА // Фундаментальные исследования. 2013. № 5-1. С. 180-183;URL: https://fundamental-research.ru/ru/article/view?id=31488 (дата обращения: 16.05.2026).



