Диоксид титана считается наиболее эффективным фотокатализатором для разложения широкого круга органических и неорганических токсичных веществ [3], причем фотокаталитические свойства наноразмерного анатаза признаются лучшими [7]. Однако такой фотокатализатор может работать лишь под действием УФ-излучения с длиной волны < 386 нм, что соизмеримо с шириной запрещенной зоны анатаза (3,2 eV соответствует 387 нм) [5]. При уменьшении ширины запрещённой зоны TiO2 или появлении в ней примесных энергетических уровней «красная граница» фотопоглощения сдвигается в сторону более длинноволнового видимого диапазона (т.е. максимальная длина волны «рабочей» спектральной области увеличивается, а минимально необходимая для фотовозбуждения энергия квантов уменьшается). Для приготовления фотокатализаторов на основе диоксида титана, активных под видимым светом, используют преимущественно фотосенсибилизацию, в частности, допирование [2] или модифицирование [8]. Допирование, как правило, проводится при повышенных температурах, что удается избежать модифицированием диоксида титана. При этом используются органические красители, а также окрашенные неорганические и координационные соединения.
Цель работы − модификация диоксида титана марганцем(IV) для повышения фотокаталитической активности образцов и сдвига спектрального отклика в видимую область.
Материалы и методы исследования
Объектами исследования были образцы, полученные сульфатным методом [1], условия модифицирования которых приведены в таблице.
Рентгеновская съёмка образцов с вращением проведена на дифрактометре HZG-4 (Ni – фильтр): CuKa на дифрагированном пучке в пошаговом режиме (время набора импульсов 10 с, величина шага 0,02°, интервал углов 2...80°2q). Качественный фазовый анализ образцов проведен с использованием базы данных JCPDS PDF-2 и оригинальных работ. При расчете размеров областей когерентного рассеяния (ОКР) применяли формулу Дебая−Шеррера (уширение дифракционных пиков обусловлено только размерным эффектом): D, Å = Kl/bcos q, где l – длина волны, 2q ~ 25°, b – ширина пика на половине высоты, K = 0,9. Стандартное отклонение величины D ± 5 %. Соотношение рутила и анатаза в образцах определялось по уравнению: xр, % = 1∙100/(1 + 0,794Iа/Iр), где xр, % – содержание рутила в смеси, Ia и Iр – интегральные интенсивности соответственно 101 и 110 рефлекса анатаза и рутила [9].
Условия получения образцов
|
Образец |
Условия получения |
|
1 |
1) Нагревание смеси 7,35 г TiOSO4·H2O·H2SO4 (Aldrich, 2012) с 40 мл воды до t = 91 °С и выдерживание (при перемешивании) при t = 95–98 °С в течение 16 мин с последующим термостатированием суспензии при t = 80 ± 0,5 °С в течение 4 ч; 2) ввод в реакционную смесь через 1 ч термостатирования 10 М раствора H2O2 (5 мл), а через 2,5 ч термостатирования – 0,05 М раствора KMnO4 (20 мл); 3) отделение осадка вакуумным фильтрованием (через несколько суток), промывание его водой и ацетоном, высушивание в шкафу (t ~ 100 °С, 1 ч), УФ облучение (125 Вт) в течение 1 ч |
|
5 |
1) Диспергирование 0,24 г промышленного нано-TiO2 (марки HombifineN) в 0,05 М растворе KMnO4 (24 мл) и выдерживание полученной суспензии (при перемешивании) при t = 56–60 °С в течение 10 мин; 2) УФ-облучение реакционной смеси (125 Вт, при перемешивании) в течение 1 ч; 3) отделение осадка вакуумным фильтрованием (через несколько суток), промывание его водой и ацетоном, высушивание в шкафу (t ~ 100 °С, 1 ч), УФ-облучение (125 Вт) в течение 1 ч |
|
6 |
1) Нагревание смеси 7,35 г TiOSO4·2H2O (СССР, 1990) с 40 мл воды до t = 98 °С и выдерживание (при перемешивании) при t = 97–102 °С в течение 25 мин с последующим введением в реакционную смесь 10 М раствора H2O2 (10 мл) и (через 2 мин перемешивания реакционной смеси) – 0,01 М раствора KMnO4 (40 мл); 2) термостатирование полученной суспензии при t = 75 ± 0,5 °С в течение 5 ч; 3) отделение осадка вакуумным фильтрованием (через несколько суток), промывание его водой и ацетоном, высушивание в шкафу (t ~ 100 °С, 1 ч) |
|
9 |
1) Нагревание смеси 3,85 г TiOSO4·H2O·H2SO4 (Aldrich, 2012) с 20 мл воды до t = 88 °С и выдерживание (при перемешивании) при t = 90–94 °С в течение 4 мин до просветления реакционной смеси (т.е. до превращения суспензии в коллоидный раствор); 2) выдерживание реакционной смеси (при перемешивании) при t = 88–92 °С в течение 2,5 мин и охлаждение полученного прозрачного (при любом угле наблюдения) золя в ледяной бане (до t = 0 °С); 3) смешение 0.6 М раствора ацетата марганца (II) (32 мл) и 0,9 М раствора перманганата калия (32 мл) и выдерживание полученной суспензии (при перемешивании и облучении галогеновой лампой мощностью 250 Вт) при t ~ 76 °C в течение 1 ч (до исчезновения фиолетовой окраски жидкой фазы) 4) отделение осадка вакуумным фильтрованием (через несколько суток), промывание его водой и ацетоном, высушивание в шкафу (t ~ 100 °С, 1 ч), УФ облучение (125 Вт) в течение 1 ч; 5) диспергирование 0,282 г полученного в п. 4 порошка в титаноксидном золе, полученном в п. 2 и термостатирование суспензии при t = 80 ± 0,5 °С в течение 7 ч; 6) отделение осадка вакуумным фильтрованием (через несколько суток), промывание его водой и ацетоном, высушивание в шкафу (t ~ 100 °С, 1 ч) |
|
12 |
Промышленный фотокатализатор TiO2(MnIV) (Aldrich, 2012, CAS № 13463-67-7) |
Фотокаталитическая активность образцов изучена на модельной реакции фотокаталитического разложения красителя метилового оранжевого (МеО) [10]: исходная концентрация водного раствора МеО (с0) – 1,04 ммоль/л, массовая концентрация суспендированного фотокатализатора – 0,4 г/л. Отношение текущей концентрации МеО (после облучения смеси в течение τ минут галогеновой лампой мощностью 250 Вт) к исходной (величина с/с0) контролировали спектрофотометрически по изменению интенсивности полосы поглощения МеО при длине волны около 490–510 нм.
Результаты исследования и их обсуждение
Серия 1
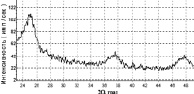
В данной серии в качестве исходного был взят модифицированный марганцем (IV) образец 1 (таблица), дифрактограмма которого представлена на рис. 1,а.
Образец 1 содержит в основном нанокристаллический анатаз с D = 60(3) Å. При отжиге этого образца при t = 400 °С с увеличением длительности выдержки при этой температуре от 1 ч (образец 2) до 7 ч (образец 4) увеличивается содержание рутила (соответственно от ~ 61,5 % до ~92 %). При этом по сравнению с образцом 1 в образцах 2 и 4 величина D для анатаза больше (D = 265(13) Å). На дифрактограммах образцов 3 и 4 появляется дифракционное отражение при 2q ~ 11.5° (межплоскостное расстояние d ~ 7,72 Å). Фазовый анализ не позволил по одному отражению уверенно определить примесную фазу, но тем не менее данный рефлекс характерен для фаз H2TixOy, в частности, H2Ti3O7 (JCPDS№ 47-0561), H2Ti2O5×H2O (JCPDS № 47-0124), TiO2×nH2O, TiO(OH)2, Ti4O7(OH)2×H2O (JCPDS № 48-1278) и титанатов. В любом случае эта фаза (в дальнейшем будем называть эту фазу с 2Q~12° «гидролизный диоксид титана») содержит группы OH или (и) H2O, и содержание ее увеличивается при переходе от образца 3 к образцу 4. Данный факт свидетельствует о том, что изучаемые материалы представляют собой совокупность сравнительно слабо взаимодействующих нано-кристаллических частиц анатаза и рентгеноаморфных частиц «гидролизного диоксида титана», причем при отжиге они переходят сначала в аморфное, а потом и в наноразмерное состояние.
Как видно из рис. 1,д, фотокаталитические свойства ухудшаются при переходе от образца 1 (k = 0.08685 мин−1) к образцу 4: k = 0,00206 мин−1 для образца 2 и k = 0,00046 мин−1 для образца 4.
 б)
б) 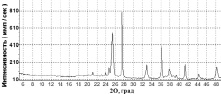
в) 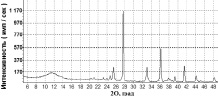 г)
г) 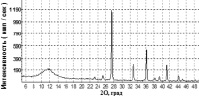
д)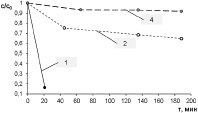
Такое изменение свойств может быть связано с увеличением размеров ОКР нано-анатаза или (и) увеличением содержания фазы рутила.
Серия II
В данной серии в качестве исходных были взяты коммерческий образец Hombifine N и полученный нами образец с наноразмерным анатазом, которые были модифицированы марганцем (IV) (соответственно образцы 5 и 6) (рис. 2). Оба образца содержат только наноразмерный анатаз с размерами ОКР: D = 80(4) Å (образец 5) и D = 55(3) Å (образец 6).
По фотокаталитическим свойствам образец 6 сопоставим с образцом 1 (серия I) и лучше по сравнению с образцом 5 – Hombifine (MnIV). Необходимо отметить, что по результатам работы [4] модифицированный марганцем коммерческий образец Hombikat оказался наиболее перспективным по сравнению с другими диоксидами титана в качестве катализаторов для низкотемпературного каталитического восстановления NO.
Серия III
Данная серия представлена двумя образцами (таблица, рис. 3), которые отличаются как составами (образец 7: ~65 % нано-анатаз и ~35 % гидролизный диоксид титана; образец 8 – ~65 % нано-анатаз и ~35 % нано-рутил), так и размерами ОКР: (D = 25(3) Å для образца 7 и D = 100(5) Å для образца 8).
Фотокаталитические свойства незначительно ухудшаются при переходе от образца 7 (k = 0,022 мин−1) к образцу 8 (k = 0,019 мин−1). Такое изменение свойств может быть связано и (или) с увеличением размеров ОКР, и (или) с присутствием нано-рутила. Если сравнить эти результаты с результатами, полученными при изучении образцов 1 и 6, можно сделать предварительный вывод, что гидролизный диоксид титана не оказывает заметного влияния на скорость фотореакции, во-первых, а, во-вторых, существенную роль в появлении фотокаталитических свойств действительно играет размер ОКР, причем величина D ~ 25 Å явно мала для их оптимизации.
а) 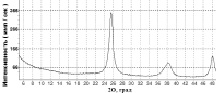 б)
б)  в)
в)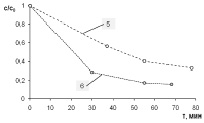
Рис. 2. Дифрактограммы образцов: а – 5 (Hombifine (MnIV)), б – 6; в – зависимость относительного изменения концентрации с МеО от времени τ облучения видимым светом (250 Вт) в присутствии образцов 5 и 6
а) 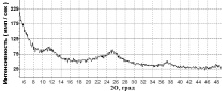 б)
б)  в)
в) 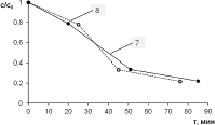
Рис. 3. Дифрактограммы образцов: а – 7 (исходный); б – 8 (отжиг: t = 300°C, т = 1 час); в – зависимость относительного изменения концентрации с МеО от времени τ облучения видимым светом (250 Вт) в присутствии образцов 7 и 8
Необходимо отметить, что в данном случае уже при t = 300 °С в образце 8 присутствует нано-рутил в количестве ~35 %. Результаты исследования образцов серий I и III свидетельствуют о том, что переход из нано-анатаза в нано-рутил в модифицированных Mn (IV) образцах начинается при более низких температурах (по крайней мере, не выше 300 °С), чем в «немодифицированных» образцах, причем степень трансформации структуры анатаза в структуру рутила увеличивается с увеличением длительности нагрева. Полученные нами результаты не противоречат данным работы [9].
Серия IV
Образец 9 представляет собой начальную стадию образования нано-диоксида титана: основная доля принадлежит гидролизному диоксиду титана (~84 %), а на долю нано-анатаза и нано-рутила приходится соответственно ~6 % и ~10 % (рис. 4,а). Необходимо обратить внимание, что уже в данном образце присутствует нано-рутил, образование которого при данных условиях синтеза обусловлено большой концентрацией MnO2 в растворе (см. таблицу). При отжиге образца 9 при t ≈ 400 °C в течение первого часа (образец 10) увеличивается содержание нано-рутила (~65 %) (рис. 4,б), а при продолжении отжига при той же температуре (образец 11) содержание нано-рутила достигает уже 100 % (рис. 4,в). В этом же ряду образцов наблюдается увеличение размеров ОКР: D = 70(4) Å (образец 9) и D = 90(4) Å (образец 10) для нано-анатаза, D = 160(8) Å (образец 9) для нано-рутила.
Фотокаталитические свойства образцов 9 и 10 оказались хуже, чем у образцов 1 и 6, но значительно лучше, чем у коммерческого образца TiO2, содержащего 1 % Mn фирмы Sigma Aldrich (образец 12, рис. 4,г), который содержит ~75 % рутила (D = 275(14) Å) и ~25 % анатаза (D = 275(14) Å). Таким образом, основываясь на полученных данных, можно сделать вывод, что фотокаталитические свойства коррелируют с размерами ОКР, и максимальная фотокаталитическая активность достигается при D ~ 55...60 Å.
Известно, что с размерами наночастиц (во многих работах наночастицы приравниваются к кристаллитам, а они, в свою очередь, к размерам ОКР), связана ширина запрещенной зоны, являющаяся одним из основных параметром фотокатализатора: по мере уменьшения ширины запрещённой зоны TiO2 увеличивается сдвиг края его фотопоглощения в видимую область (в сторону бóльших длин волн) и наоборот. В работе [6] исследована связь ширины запрещенной зоны TiO2 с размерами наночастиц, а в [7] найдено, что при уменьшении размеров наночастиц от 29 до 17 нм ширина запрещенной зоны уменьшается, а для размеров 3,8; 4,9 и 5,7 нм – увеличивается на 0,05; 0,012 и 0,036 эВ соответственно, что связывается с наличием агрегации.
а) 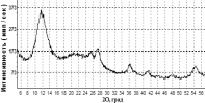 б)
б) 
в) 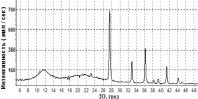 г)
г) 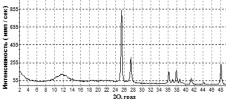
д)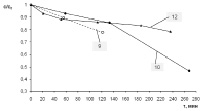
Рис. 4. Дифрактограммы образцов: а – 9 (исходный), б – 10 (отжиг: t = 400 °C, т = 1 ч); в – 11 (отжиг: t = 400 °C, т = 2 ч); г – 12 (коммерческий образец TiO2 (MnIV) фирмы Sigma Aldrich); д – зависимость относительного изменения концентрации с МеО от времени τ облучения видимым светом (250 Вт) в присутствии образцов 9, 10 и 12
Отсюда следует, что скорость фотореакции будет определяться размерными параметрами нанообъектов, что и было показано в данной работе для модифицированных Mn(IV) образцов с нано-анатазом, а оптимальный размер способствует наилучшему соотношению скоростей рекомбинации пар электрон–дырка в объеме и на поверхности.
Исследование выполнено при поддержке Министерства образования и науки Российской Федерации, соглашение 14.B37.21.1621.
Рецензенты:
Аминов Т.Г., д.х.н., профессор, ведущий научный сотрудник Института общей и неорганической химии имени Н.С. Курнакова Российской академии наук, г. Москва;
Чернышев В.В., д.ф.-м.н., ведущий научный сотрудник химического факультета МГУ имени М.В. Ломоносова, г. Москва.
Работа поступила в редакцию 11.01.2013.
Библиографическая ссылка
Оболенская Л.Н., Доморощина Е.Н., Савинкина Е.В., Кузьмичева Г.М. ПОЛУЧЕНИЕ, ХАРАКТЕРИЗАЦИЯ И ФОТОКАТАЛИТИЧЕСКИЕ СВОЙСТВА НАНОРАЗМЕРНОГО АНАТАЗА, МОДИФИЦИРОВАННОГО МАРГАНЦЕМ // Фундаментальные исследования. 2013. № 1-3. С. 796-801;URL: https://fundamental-research.ru/ru/article/view?id=31031 (дата обращения: 07.04.2026).



