В последнее время возрос интерес к новым производным нафтилпиразолов в связи с проявлением такими соединениями фунгицидной и антибактериальной активности [4]. Недавно были получены нитрозопиразолы нафталинового ряда путем конденсации нафтилзамещенных изонитрозо-β-дикетонов с алкилгидразинами [1, 3]. Мы продолжили исследования в области применения реакции циклоароматизации и попытались впервые получить нафтилнитрозопиразолы, содержащие в своем составе этоксиметильную группу. Выбор данного направления обусловлен тем, что использование лекарственных веществ со спиртовой или карбоксильной группой в виде их сложных или простых эфиров изменяет полярность молекулы и улучшает проявление фармакологической активности [2].
Цель исследования – разработка метода синтеза нового потенциально биологически активного пиразола с этоксиметильным и нафтильным заместителями на основе этилового эфира этоксиуксусной кислоты. Выделение и идентификация новых дикетонов, изонитрозодикетонов и пиразолов. Изучение физико-химических свойств синтезированных соединений.
Материалы и методы исследования
Структура полученных соединений подтверждена спектральными методами анализа. УФ спектры записывали на спектрофотометре HELIOS OMEGA в этаноле. Спектры ЯМР 1Н записывали в ДМСО-d6 на приборе Bruker Avance III 600,13 МГц. Масс-спектры регистрировали на приборе Finnigan MAT 8200. ИК спектры получены на ИК микроскопе SpecTRA TECH InspectIR на базе ИК Фурье-спектрофотометра Impact 400. Ход реакции и чистоту соединений контролировали методами ТСХ на пластинах Silufol UV-254 в системе этилацетат-толуол (1:3), пятна детектировали в ультрафиолетовом свете.
Результаты исследования и их обсуждение
В результате конденсации этилового эфира этоксиуксусной кислоты с 2-ацетонафтоном под действием этилата натрия в абсолютном эфире был впервые получен 1-(2-нафтил)-4-этоксибутандион-1,3 (I) (схема 1).
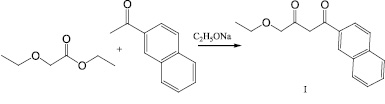 (1)
(1)
При нитрозировании дикетона нитритом натрия в уксусной кислоте согласно методике [5] был выделен 1-(2-нафтил)-4-этокси-бутан-1,2,3-трион-2-оксим (II) (схема 2).
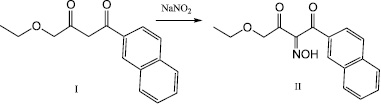 (2)
(2)
Для синтеза этоксиметилнитрозопиразола изонитрозодикетон вводили в реакцию с гидразингидратом в водно-щелочной среде. Новый нафтилнитрозопиразол с этоксиметильным заместителем был выделен в виде кристаллов зеленого цвета с четкой температурой плавления (схема 3).
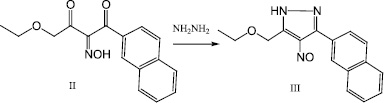 (3)
(3)
Экспериментальная часть
1-(2-нафтил)-4-этоксибутандион-1,3 (I). Смешивали 28,695 г этилового эфира этоксиуксусной кислоты с 26,04 г ацетофенона в 100 мл абсолютного этилового эфира над свежеприготовленным этилатом натрия, приготовленного из 5 г натрия. После растворения этилата натрия нагревали на водяной бане 40 минут. В реакционную массу добавляли 100 мл воды и водный слой экстрагировали эфиром. Водный раствор подкисляли серной кислотой до слабокислой реакции. Осадок фильтровали и промывали гексаном. Белые кристаллы, Т плавления 128-130 °С. Выход 25,5 г (46 %). Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 1,18 т (СН3), 3,52 к (СН2), 2,72 c (СН2), 3,74 с (СН2), 7,51-8,69 м (нафтил). Масс спектр, m/z (Iотн, %): 256 (6) [M]+, 127 (100), 155 (92), 31 (79), 43 (57), 170 (40).
1-(2-нафтил)-4-этоксибутан-1,2,3-трион-2-оксим (II). К раствору 1,5 г (5 ммоль) 1-(2-нафтил)-4-этоксибутандиона-1,3 в 20 мл ледяной уксусной кислоты при охлаждении и перемешивании добавляли 0,545 г (7 ммоль) сухого нитрита натрия. Нитрит натрия добавляли порциями, чтобы температура смеси была не выше 16 °С. Реакционную массу перемешивали 2,5 ч. Выпавший осадок промывали гексаном и отфильтровывали. Выход 1-(2-нафтил)-4-этоксибутан-1,2,3-трион-2-оксима составил 1,1 г (76 %), вещество белого цвета, Tпл 146-147 °С. Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 1,16 т (СН3), 3,55 к (СН2), 4,83 с (СН2), 7,6-8,4 м (нафтил), 13,12 c (NOH). ИК спектр, ν, см-1: 1673 (СН2С=О), 1701 (нафтил С=О). Масс спектр, m/z (Iотн, %): 285 (4) [M]+, 31 (100), 127 (75), 155 (74), 59 (58), 77 (118).
5-этоксиметил-4-нитрозо-3-(2-нафтил)-1Н-пиразол (III). К раствору 0,2 г (0,6 ммоль) 1-(2-нафтил)-4-этоксибутан-1,2,3-трион-2-оксима в 10 мл воды и 0,1 г КОН при перемешивании добавляли 0,05 г (0,8 ммоль) сухого гидразингидрата. После перемешивания в течение 20 минут при 20 °С раствор подкисляли. Выпадал осадок зеленого цвета. выход 0,57 г (81 %), зеленые кристаллы, Tпл 115 °С. УФ-спектр, λмакс, нм (ε): 705 (52,4). Спектр ЯМР 1Н (ДМСО-d6), δ, м.д.: 1,19 с (СН3), 3,59 к (СН2), 4,46 с (СН2), 7,6-8,8 м (нафтил), 14,2 (NH). Масс спектр, m/z (Iотн, %): 281 (18) [M]+, 153 (100), 29 (98), 31 (75), 127 (54), 179 (11).
Выводы
- В ходе проведенного исследования был впервые получен этоксидикетон с нафтильным заместителем.
- Синтезирован ранее неизвестный 1-(2-нафтил)-4-этоксибутан-1,2,3-трион2-оксим.
- Впервые выделен 5-этоксиметил-4-нитрозо-3-(2-нафтил)-1Н-пиразол.
- Индивидуальность соединений подтверждена с помощью ТСХ, а химическая структура – современными спектральными данными.
Работа выполнена при финансовой поддержке гранта Красноярского краевого фонда поддержки науки и научно-технической деятельности «Молодым ученым» (2014 г.).
Рецензенты:
Твердохлебов В.П., д.х.н., профессор, зам. директора Института нефти и газа, зав. кафедрой химии и технологии переработки углеродных материалов, Сибирский федеральный университет по стратегическому развитию, г. Красноярск;
Левданский В.А., д.х.н., доцент, главный научный сотрудник лаборатории каталитической химии угля и биомассы, Институт химии и химической технологии СО РАН, г. Красноярск.
Работа поступила в редакцию 06.11.2014.
Библиографическая ссылка
Любяшкин А.В., Субоч Г.А., Товбис М.С. СИНТЕЗ 1-(2-НАФТИЛ)-4-ЭТОКСИБУТАНДИОНА-1,3 И ЭТОКСИМЕТИЛНИТРОЗОПИРАЗОЛА НА ЕГО ОСНОВЕ // Фундаментальные исследования. 2014. № 11-7. С. 1552-1554;URL: https://fundamental-research.ru/ru/article/view?id=35805 (дата обращения: 17.01.2026).



