Операционный стресс закладывает основы функциональных расстройств, которые продолжают действовать в послеоперационном периоде. Факторы операционного стресса могут быть разделены на две большие группы:
1) психоэмоциональное напряжение;
2) афферентная импульсация, возникающая в результате механического повреждения тканей.
Послеоперационная боль при ее выраженном и длительном течении ассоциируется с многими системными осложнениями ХС [7], что в основном предопределяется избыточными симпато-адреналовыми эффектами [3, 10, 11], сопровождающими болевые ощущения. Продолжительные вегетативные нарушения проявляются в виде регионарных ганглионевритов, провоцирующих дегенативно-дистрофические процессы в периферическом аппарате внутренних гениталий [9]. Это может стать причиной хронических тазовых болей, а также стойких нарушений в мочеполовом тракте и репродуктивной сфере [5]. Возникновение послеоперационных осложнений связано с тем, что адаптивные механизмы организма оказываются неспособными к адекватной реакции на последующие воздействия стрессоров, вызывающих тканевые повреждения в связи с истощением своего потенциала [8, 10]. С нарушением адаптации организма также связана длительная послеоперационная девиация в вегетативной нервной системе, c которой могут быть связаны различные послеперационные осложнения. В связи с этим в послеоперационном периоде должна быть обеспечена антистрессовая защита, включающая специальные меры, нормализующие состояние вегетативной нервной системы, купированию послеоперационной боли, ранней и полной активизации больных, уменьшению частоты осложнений.
Цель исследования – определить характер изменений преобладающего типа вегетативной регуляции в послеоперационном периоде у пациенток с длительным послеоперационным болевым (дПБС) синдромом и оценка влияния на вегетативный статус применения лазеротерапии на область тимуса и электрофореза пантовегина по данным индекса Кердо и вегетативного индекса.
Материалы и методы исследования
В исследование были включены пациентки после гинекологических операций лапаратомным доступом. Показанием к операции являлись следующие заболевания: миома матки, аденомиоз, опухолевые и опухолевидные образования яичников, воспалительные образования придатков матки, сочетанная патология матки и яичников. В I группу вошли 97 пациенток с развившимся длительным послеоперационным болевым синдромом, 123 пациентки не имели указанного осложнения (без дПБС) Диагноз дПБС ставился пациенткам, нуждавшимся в продолжении анальгетической терапии с применением НПВС более 4 суток после выполненного вмешательства из-за сильной боли (более 50 % по ВАШ). В зависимости от проводимого физиотерапевтического лечения внутри групп пациентки были распределены на 3 подгруппы, сопоставимые по основным морфо-функциональным параметрам:
● пациентки подгруппы А получали комбинированную терапию, включающую низкоинтенсивную инфракрасную лазеротерапию на область тимуса и электрофорез пантовегина (32 женщины);
● пациентки подгруппы В получали низкоинтенсивную инфракрасную лазеротерапию на тимус (33 женщины);
● пациентки подгруппы С получали электрофорез пантовегина (32 женщины).
Всем больным наряду с общеклиническим обследованием (анализы крови, мочи, биохимический анализ крови, ЭКГ, Rg легких) проводили специальные методы исследований.
Определение преобладающего типа вегетативной регуляции (симпатикотония, парасимпатикотония или эйтония) проводилось на основании оценки вегетативного индекса Кердо (ВИК) (Вейн А.М. с соавт., 1997), рассчитывавшегося по формуле
ВИК = (1 – диастолическое АД/ЧСС)∙100.
Определение ВИК производилось в состоянии покоя в период перед операцией и после окончания физиотерапевтического лечения. Вегетативный индекс (ВИ) рассчитывали по формуле:
ВИ = 1 – d/P∙100 % – 100,
где ВИ – значение вегетативного индекса; d – диастолическое давление; Р – пульс у пациента. Оценка выраженности боли. Для измерения интенсивности боли в послеоперационном периоде использовали тесты субъективной самооценки с применением визуальной аналоговой шкалы (ВАШ) и 4-балльной вербальной рейтинговой шкалы боли (ВРШ/Б) (Huskisson E.C. et al., 1983; Melzak R. et al., 1987). Для субъективной самооценки эффективности терапии применяли 4-балльную вербальную рейтинговую шкалу купирования боли (ВРШ/КБ) (Keef J. et al., 1987). В первые сутки после операции тесты ВАШ и ВРШ/Б использовали перед первой процедурой и далее через 2, 4, 8, 12, 18 и 24 часа. Тест ВРШ/КБ использовали через 12 и 24 часа после выполненной операции. В последующем тесты ВАШ, ВРШ/Б и ВРШ/КБ продолжали применять 2 раза в сутки в течение всего периода регистрации болевых ощущений
В послеоперационном периоде использовали традиционную тактику ведения хирургических гинекологических больных.
Послеоперационное обезболивание. В первые 24 часа после операции всем пациенткам назначали наркотические анальгетики (НА) в сочетании или без параллельного использования ненаеркотического анальгетика кеторола. В последующем для анальгезии применяли только кеторол.
В послеоперационном периоде использовали традиционную тактику ведения хирургических гинекологических больных.
Физиотерапевтическое лечение включало процедуры лазеротерапии (ИК НЛИ)[5] и электрофореза пантовегина [1, 2].
Процедуры лазеротерапии проводились с помощью аппарата «Азор-2К-02» (Россия), генерирующего импульсное лазерное излучение инфракрасного диапазона с длиной волны λ = 0,89 мкм, с частотой следования импульсов 1500 Гц, при импульсной мощности 4–6 Вт/имп. Процедуры проводились на область тимуса, контактно, стабильно, время воздействия – 10 минут, на курс 10 ежедневных процедур.
Процедуры электрофореза пантовегина проводились от аппарата «Поток-1» (Екатеринбург), сила тока определялась по ощущениям и составляла 10–15 мА, длительность процедуры 15 минут, расположение электродов (S = 150 см²) продольно-поперечное, индифферентный электрод (S = 200 см²) накладывался на область поясницы. В настоящем исследовании применяли субстанцию «пантогематоген сухой» (рег. уд. № 000051/01-2000 от 12.10.2000) «пантовегин». Пантовегин вводился с 2 раздвоенных электродов (анод), на которые наносилась разовая доза раствора. На курс 10 ежедневных процедур. Физиотерапия назначалась с 5 суток.
Статистический анализ клинических данных производился с использованием программного обеспечения для ПК Microsoft Excel и Statistica 6.0. Для представления итоговых данных использовали стандартные методы описательной статистики. Количественные показатели представлены в виде средних и стандартных квадратных отклонений, а качественные признаки сгруппированы в таблицы сопряжённости. Для сравнения групп использовались методы, основанные на дисперсионном анализе – F-критерий, t-критерий Стьюдента (для анализа нормально распределённых выборок); непараметрические критерии – критерий хи-квадрат, точный критерий Фишера (основанные на хи-квадрат-распределении), ранговые критерии: U-тест Манна‒Уитни (непараметрический критерий для сравнения данных по группам) и критерий Вилкоксона (для сравнения данных, полученных до и после лечения). Для определения связи между параметрами использовали коэффициент корреляции Пирсона (для нормально распределенных совокупностей) и коэффициент ранговой корреляции Спирмена (непараметрический ранговый метод).
Результаты исследования и их обсуждение
В исходном состоянии истинное симпатическое влияние было выявлено у большинства пациенток с дПБС (рис. 1)
После применения комбинированной физиотерапевтической методики у 94 % пациенток 1А подгруппы отмечалась девиация ВНС в сторону эйтонии – индекс Кердо составил 0,22 ± 0,01 % (р < 0,05, сравнение с показателям до лечения). В 1В подгруппе наблюдались однонаправленные сдвиги – 84 % пациенток индекс Кердо также соответствовал эйтонии – 0,28 ± 0,06 % (р < 0,05, сравнение с показателями до лечения). В 1С подгруппе у большинства пациенток индекс Кердо статистически достоверных изменений не претерпевал и соответствовал симпатикотонии (рис. 2).

Рис. 1. Вегетативное обеспечение в послеоперационном периоде в группе без дПБС и с дПБС
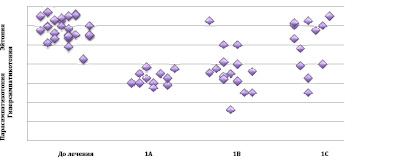
Рис. 2. Вегетативный статус на фоне физиотерапевтического лечения в подгруппах
Однако, если индекс Кердо указывает на то, что почти у всех пациенток с дПБС отмечалось выраженное влияние симпатической нервной системы, то вегетативный индекс (ВИ) дает четкое представление именно о типе ВНС. При анализе ВИ выявлено, что большинство пациенток с дПБС имели выраженную тенденцию к влиянию симпатического тонуса: ВИ до лечения составил + 21,6 ± 3,2 (р < 0,05, сравнение с показателями до лечения). После лечения в 1А подгруппе отмечалась нормализация показателя ВИ, который значительно снизился и соответствовал нормальным значениям + 6,2 ± 1,8 (p < 0,05, сравнение с показателем до лечения). В 1В подгруппе после применения ИК НЛИ на область тимуса также отмечалась нормализация типа реагирования ВНС, при этом ВИ снизился с + 19,9 ± 2,2 (p < 0,05, сравнение с нормой) до + 5,2 ± 1,1 (p < 0,05, сравнение с показателем до лечения). В 1С подгруппе лишь у 24 % пациенток значения ВИ соответствовали эйтоническому типу ВНС.
Таким образом, исходная симпатикотония является одним из факторов риска развития длительного послеоперационного болевого синдрома, а применение ИК НЛИ(4) на область тимуса оказывает выраженное положительное влияние на вегетативный баланс, что лежит в основе формировании высокого терапевтического эффекта разработанного комбинированного метода. На фоне лечения наблюдалось более быстрое купирование послеоперационной боли, а также улучшение общего состояния больных ‒ исчезала слабость, улучшались сон и аппетит.
Выводы
Комбинированное применение лазеротерапии на область тимуса и электрофореза пантовегина у пациенток с длительным послеоперационным болевым синдромом обеспечивает повышение резервов вегетативной нервной системы, что проявляется в устранении явлений гиперсимпатикотонии, восстановлении типа реагирования и подтверждается нормализацией показателей индекса Кердо и вегетативного индекса. Указанные изменения способствуют благоприятному течению послеоперационного периода, более быстрому купированию болевого синдрома, ранней активизации больных. Перечисленные свойства метода позволяют рекомендовать данный вид лечения гинекологическим больным с длительным послеоперационным болевым синдромом после лапаротомных операций.
Рецензенты:
Щукин А.И., д.м.н., профессор кафедры неврологии Института последипломного профессионального образования, ФГБУ «Государственный научный центр Российской Федерации – Федеральный медицинский биофизический центр имени А.И. Бурназяна», г. Москва;
Орехова Э.М., д.м.н., профессор кафедры восстановительной медицины, спортивной медицины, курортологии и физиотерапии Института последипломного профессионального образования, ФГБУ «Государственный научный центр Российской Федерации ‒ Федеральный медицинский биофизический центр им. А.И. Бурназяна» ФМБА, г. Москва.
Работа поступила в редакцию 21.01.2014.
Библиографическая ссылка
Корчажкина Н.Б., Дугиева М.З. ПРИМЕНЕНИЕ СОВРЕМЕННЫХ ФИЗИОТЕРАПЕВТИЧЕСКИХ ТЕХНОЛОГИЙ ДЛЯ ПОВЫШЕНИЯ СТРЕССОУСТОЙЧИВОСТИ ПОСЛЕ ОПЕРАТИВНЫХ ВМЕШАТЕЛЬСТВ У БОЛЬНЫХ С ДЛИТЕЛЬНОЙ ПОСЛЕОПЕРАЦИОННОЙ БОЛЬЮ // Фундаментальные исследования. 2013. № 12-3. С. 491-494;URL: https://fundamental-research.ru/ru/article/view?id=33436 (дата обращения: 22.03.2026).



