Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
FACTORS OF LOCAL IMMUNITY IN PATIENTS WITH ORAL MUCOSA AND TONGUE CARCINOMA WITH ABSENCE AND PRESENCE OF REGIONAL METASTASES AND RECURRENCES
Биологическое поведение злокачественной опухоли, которое характеризует скорость ее роста, способность к инвазии и распространению, а, в конечном итоге, и прогноз заболевания, зависит от многих причин, связанных как с ее особенностями, так и с эффективностью или неэффективностью системных защитных механизмов, среди которых важное место занимают иммунные. По-видимому, свойства опухоли и реакции иммунной системы организма на нее тесно взаимосвязаны. С учетом значения иммунокомпетентных клеток в процессах апоптоза, пролиферации, неоангиогенеза (в частности, через продукцию цитокинов), их роль в микроокружении опухоли представляется существенной, однако, не полностью проясненной. Иммунная защита организма от опухоли осуществляется не только на системном, но и на локальном уровне. Участие в ней различных клеточных факторов, главным образом, Т- и NК-клеток, а также их растворимых продуктов, в настоящее время не подлежит сомнению [4, 6, 7]. Однако, хотя присутствие иммунокомпетентных клеток и гуморальных факторов в микроокружении опухоли давно описано, их роль в очаге расценивается двояко, т.е. они рассматриваются как факторы, не только способствующие ее регрессии, но и могущие стимулировать ее рост, тем более, при распространенных стадиях [1, 8, 9].
Оценка факторов локального иммунитета у онкологических больных, в частности, при раке слизистой полости рта и языка, представляет собой важную проблему, могущую иметь теоретические и прикладные аспекты.
Цель исследования
Провести сравнительную оценку факторов клеточного и гуморального иммунитета в тканевых образцах опухоли и ее перитуморальной зоны у больных раком слизистой полости рта и языка без метастазов, с регионарными метастазами и с рецидивами.
Материалы и методы исследования
Объектом исследования были 69 больных раком слизистой полости рта и языка (55 мужчин, 14 женщин; возраст 40–77 лет), которые были разделены на 3 группы по 23 человека: 1-я группа больных без регионарных метастазов и рецидивов, 2-я – с наличием метастазов, 3-я – с рецидивами. Больные проходили лечение в отделении опухолей головы и шеи ФГБУ «РНИОИ» МЗ РФ в 2006–2014 гг. Распространенность процесса у больных первых двух групп составила: со II стадией (T2N0M0) было 10 человек, с III – 25 (T2N1M0 – 4, T3N0M0 – 13, T3N1M0 – 8), с IV – 11 (T3N2M0 – 2, T4N0M0 –5, T4N1M0 – 4). У 57 (82,6 %) больных опухолевым процессом был поражен язык, у 12 (17,4 %) – слизистая дна полости рта. На языке опухоль располагалась чаще на боковой поверхности (52,2 %). У всех больных был плоскоклеточный рак, с высокой степенью дифференцировки (G1) у 18 больных, средней (G2) – у 34 и низкой (G3) – у 17.
В тканевых гомогенатах образцов опухоли и перитуморальной зоны (неизмененная ткань на расстоянии 1–3 см от опухоли) проводили определение уровней про- и противовоспалительных цитокинов (IL-1ß, IL-1RА, IL-2,IL-6, IL-8, IL-10, IFN-α, IFN-γ, TNF-α) методом ИФА с тест-системами производства «Вектор-Бест» (Новосибирск); результаты выражали в пг/мл; удельное содержание цитокинов вычисляли путем пересчета полученных данных на 1 г белка. В срезах тканей оценивали содержание основных субпопуляций Т-лимфоцитов методом ИГХ с антителами к CD4, и CD8, CD68 фирмы DAKO.
Результаты исследования и их обсуждение
Сравнительная характеристика удельных уровней цитокинов в тканях опухоли и перитуморальной зоны (ПЗ) представлена в таблице. Вариабельность значений оказалась существенной; несмотря на это, удалось установить ряд статистически достоверных различий содержания провоспалительных цитокинов.
Удельное содержание цитокинов в тканях опухоли и ПЗ больных различных групп (пг/мл/г белка)
|
Цитокины |
Группы больных, образцы тканей |
|||||
|
1-я |
2-я |
3-я |
||||
|
Опухоль |
ПЗ |
Опухоль |
ПЗ |
Опухоль |
ПЗ |
|
|
TNF-α |
2,32 ± 1,16 |
1,47 ± 0,24 |
2,83 ± 0,91 |
3,1 ± 0,96 |
2,82 ± 0,78 |
2,32 ± 0,357 |
|
IL-8 |
16,3 ± 3,5* |
5,5 ± 2,33 |
26,7 ± 7,2* |
7,3 ± 2,78 |
17,0 ± 7,4 |
12,7 ± 7,2 |
|
IL-6 |
7,1 ± 3,2* |
0,71 ± 0,158 |
5,95 ± 2,03* |
1,23 ± 0,49 |
13,3 ± 7,3 |
1,4 ± 0,56 |
|
IL-10 |
2,5 ± 0,33 |
2,42 ± 0,33 |
2,92 ± 1,1 |
3,64 ± 1,69 |
1,23 ± 0,4 |
1,84 ± 0,5 |
|
IL-1ß |
14,4 ± 3,8* |
4,7 ± 0,71 |
19,0 ± 4,2* |
6,7 ± 2,1 |
17,5 ± 8,2 |
26,5 ± 10,7 |
|
IL-1RА |
492 ± 83 |
397 ± 33,4 |
– |
– |
– |
– |
|
IFN-α |
0,576 ± 0,1 |
0,548 ± 0,09 |
0,442 ± 0,11 |
0,47 ± 0,08 |
– |
– |
|
IFN-γ |
1,3 ± 0,2 |
1,576 ± 0,19 |
1,26 ± 0,17 |
2,35 ± 0,76 |
– |
– |
|
IL-2 |
0,533 ± 0,06 |
0,5 ± 0,06 |
0,884 ± 0,24 |
1,19 ± 0,56 |
– |
– |
Примечание. * – статистически достоверные отличия от показателей ПЗ (Р < 0,05).
Как видно из таблицы, в опухолевой ткани по сравнению с ПЗ отмечено статистически значимо более высокое содержание провоспалительных цитокинов IL-1ß, IL-6, IL-8 в группе больных без регионарных метастазов; у больных с регионарными метастазами наблюдались сходные различия. При рецидивах подобная разница отмечена только по уровню IL-6, но она оказалась статистически недостоверной вследствие высокой индивидуальной вариабельности показателей. Тканевые уровни интерферонов, IL-2 и IL-10 в опухоли и в ПЗ были невысоки и не имели статистически достоверных различий.
Сопоставление исследованных показателей в ткани опухоли выявило отсутствие статистически значимых различий между данными больных различных групп. В ткани ПЗ сравниваемых групп обнаружены некоторые отличия, например, у больных 3-й группы по сравнению с больными 1-й группы отмечено более высокое содержание TNF-α (2,32 ± 0,357 против 1,47 ± 0,24 пг/мл/г белка) и IL-1ß (26,5 ± 10,7 против 4,7 ± 0,71 пг/мл/г белка); для обоих показателей различия статистически достоверны (Р < 0,05).
Таким образом, показан ряд статистически значимых различий тканевого уровня цитокинов между тканью опухоли и перитуморальной области с преобладанием содержания провоспалительных цитокинов IL-1ß, IL-6, IL-8 в опухолевой ткани. При рецидивах в тканевых образцах ПЗ и опухоли утрачиваются различия по IL-1ß, IL-6 и IL-8, выраженные в двух других группах, что говорит о приближении иммунологических характеристик визуально немалигнизированной ткани к опухолевой и может косвенно свидетельствовать об утрате ею свойств, ограничивающих пролиферативный потенциал опухоли.
Вероятно, избыток провоспалительных цитокинов, у которых описаны ростостимулирующие свойства [1], наблюдается за счет их продукции опухолевыми клетками, а также присутствующими в очаге активированными макрофагами, что способствует росту и распространению опухоли.
При морфологическом исследовании в строме и паренхиме опухолевой ткани выявлено наличие лимфоцитарно-макрофагальной инфильтрации различной степени выраженности: от незначительной (одиночно рассеянные лимфоциты и мелкие лимфоцитарные инфильтраты) до более выраженной преимущественно расположенной на границе опухоли с ПЗ.
Иммуногистохимическое (ИГХ) исследование с использованием моноклональных антител к Т-лимфоцитарным субпопуляциям: Т-хелперам (CD4) и Т-цитотоксическим (CD8) лимфоцитам, а также макрофагам (СD68) позволило оценить состав иммунокомпетентных клеток, инфильтрирующих опухоль.
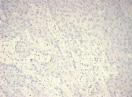
Результаты ИГХ-исследования выявили ряд общих черт для опухолей сравниваемых групп. Так, во всех группах отмечено преобладание в лимфоцитарно-макрофагальном инфильтрате CD8+ лимфоцитов над CD4+ клетками, а также выраженная инфильтрация CD68+ макрофагами, тогда как инфильтрация CD4+ клетками была представлена в виде одиночных лимфоцитов, разрозненно расположенных как в строме, так и в зонах сплошного опухолевого роста (рис. 1).
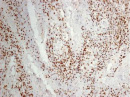
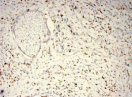
Были обнаружены и некоторые различия между сравниваемыми группами. Так, в 1-й группе выявлена наиболее выраженная инфильтрация CD8+ лимфоцитами (рис. 2), как в строме опухоли, так и в паренхиме. Инфильтрация CD68+ макрофагами была также ярко выражена, составляя в паренхиме опухоли до 20 %, в инфильтратах на границе опухоль – ПЗ от 20 до 40 % инфильтрата (рис. 3).
В группах с метастазами и рецидивами отмечено более низкое содержание CD8+ лимфоцитов как в строме, так и в паренхиме опухоли, в сравнении с 1-й группой больных (рис. 2). В отдельных образцах ткани из 2-й группы выявлены только единичные CD8+ лимфоциты в паренхиме опухоли и более выраженная инфильтрация ими на границе опухоль – ПЗ. В образцах ткани больных 3-й группы на отдельных участках в зонах сплошного опухолевого роста отмечено формирование из CD8+ лимфоцитов скоплений по типу лимфоидных фолликулов.
 а)
а) 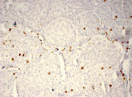 б)
б) 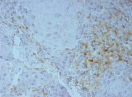 в)
в)
Рис. 1. Инфильтрация единичными CD4+ лимфоцитами опухолевой ткани: а) 1-я группа; б) 2-я группа; в) 3-я группа. Ув. х 200
 а)
а) 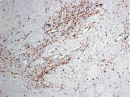 б)
б) 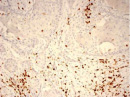 в)
в)
Рис. 2. Инфильтрация CD8+ лимфоцитами опухолевой ткани: а) 1-я группа; б) 2-я группа; в) 3-я группа. Ув. х 100
 а)
а) 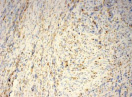 б)
б) 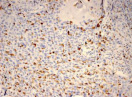 в)
в)
Рис. 3. Инфильтрация CD68+ макрофагами опухолевой ткани: а) 1-я группа; б) 2-я группа; в) 3-я группа. Ув. х 200
Инфильтрация опухоли CD68+ макрофагами опухоли без метастазов также была выше, чем при их наличии. Так, на долю CD68+ макрофагов в лимфоцитарно-макрофагальном инфильтрате больных 1-й группы в паренхиме приходилось от 10 до 20 %, на границе опухоли – ПЗ от 20 до 40 %. В образцах ткани больных 2-й группы выявлено снижение доли CD68+ макрофагов до 10 % как в строме опухоли, так и в ее паренхиме. Напротив, в группе с рецидивами отмечена обильная диффузная инфильтрация макрофагами и в строме и в паренхиме, составляющая до 40 % инфильтрата (рис. 3, в).
Итак, инфильтрация опухолей и пертуморальных зон иммунокомпетентными клетками формируется, главным образом, за счет макрофагов и предшественников цитотоксических Т-лимфоцитов, содержание которых преобладает в группе больных, не имеющих метастазов, над метастатической и рецидивной. Скопление CD8+ и CD68+ клеток отмечено на границе опухоли и перитуморальной зоны. Сопоставляя данные, полученные по уровням провоспалительных цитокинов и по содержанию макрофагов в исследованных образцах, мы предполагаем, что, по-видимому, основной вклад в формирование высокого тканевого содержания цитокинов вносит продукция их опухолевыми клетками (несмотря на сопутствующее воспаление во многих случаях, связанное с активацией макрофагального звена). В опухолях метастатической группы присутствует меньшее количество макрофагов по сравнению с группой без метастазов, однако, высокие уровни IL-1ß, IL-6, IL-8 отмечены в образцах обеих групп; такое несоответствие можно объяснить преимущественной продукцией этих цитокинов опухолевыми клетками.
Вклад СD8+ лимфоцитов в продукцию исследованных нами лимфокинов, вероятно, невелик, поскольку их основными продуцентами среди лимфоцитов считаются активированные СD4+ клетки, присутствие которых в тканевых образцах оказалось незначительным.
По данным литературы, оценка роли лимфоцитарной инфильтрации опухоли представляется неоднозначной, по-видимому, в связи с антигенной неоднородностью опухоли. Наличие или отсутствие экспрессии опухолевыми клетками различных антигенов, в частности, HLA I и II класса некоторые авторы связывают с различной степенью вовлеченности иммунокомпетентных клеток в противоопухолевый ответ [3]. В этих работах прослеживается (на примере рака молочной железы) положительная корреляция между Т-клеточной инфильтрацией опухоли (включая СD4+ и СD8+ лимфоциты) и положительным клиническим прогнозом, однако, судя по данным авторов, это относится к HLA-DR II позитивным опухолям [3]. В других исследованиях подчеркивается однозначно позитивная прогностическая роль инфильтрации СD8+ Т-клетками как предшественниками цитотоксических Т-лимфоцитов – эффекторов адаптивного иммунитета [5]. Преобладание СD8+ над СD4+ клетками, по-видимому, является общим свойством тканей, в отличие от крови, что подтверждено на примере рака слизистой полости рта и языка. Высокие уровни провоспалительных цитокинов, как показано в данной работе, отличают опухолевую ткань рака слизистой полости рта и языка от немалигнизированной, и могут быть неблагоприятным фактором ее развития и распространения, как было ранее продемонстрировано нами на примере опухолей других локализаций [2, 10].
Итак, установлен ряд особенностей локального иммунитета у больных первичным, рецидивирующим и метастазирующим раком слизистой полости рта и языка.
Выводы
1 Формирующийся высокий уровень провоспалительных цитокинов (IL-1ß, IL-6, IL-8) в ткани опухоли слизистой полости рта и языка, могущий вносить вклад в прогрессию и диссеминацию опухоли, является вероятным следствием их продукции опухолевыми клетками; уровни этих цитокинов в ткани опухоли превышают их содержание в перитуморальной зоне.
2. Различия между перитуморальными зонами первичной и рецидивной опухолей по содержанию TNF-α и IL-1ß свидетельствуют о приближении их цитокиновых характеристик к опухолевой ткани при рецидиве.
3. Преобладающей Т-лимфоцитарной субпопуляцией в опухоли являются CD3+СD8+ клетки, найденные в наиболее высоком количестве в опухолях больных без наличия метастазов и в минимальном – у больных с регионарными метастазами.
4. Присутствие макрофагов СD68+ является наиболее выраженным на границе опухоли и перитуморальной зоны у больных без наличия метастазов.
Рецензенты:
Каймакчи О.Ю., д.м.н., ассистент кафедры онкологии Ростовского Государственного Медицинского Университета, г. Ростов-на-Дону;
Владимирова Л.Ю., д.м.н., профессор, руководитель отделения противоопухолевой лекарственной терапии № 1, ФГБУ «РНИОИ» МЗ РФ, г. Ростов-на-Дону.
Библиографическая ссылка
Златник Е.Ю., Светицкий П.В., Новикова И.А., Нистратов Г.П., Аединова И.В., Волкова В.Л., Баужадзе М.В., Ульянова Е.П., Закора Г.И., Селютина О.Н. ФАКТОРЫ ЛОКАЛЬНОГО ИММУНИТЕТА У БОЛЬНЫХ РАКОМ СЛИЗИСТОЙ ОБОЛОЧКИ ПОЛОСТИ РТА И ЯЗЫКА С ОТСУТСТВИЕМ И НАЛИЧИЕМ РЕГИОНАРНЫХ МЕТАСТАЗОВ И РЕЦИДИВОВ // Фундаментальные исследования. 2015. № 1-5. С. 953-957;URL: https://fundamental-research.ru/en/article/view?id=37494 (дата обращения: 16.05.2026).



