В последнее время диагностике и лечению вирусных офтальмологических патологий как у нас в стране, так и за рубежом уделяется большое внимание. По данным статистики Министерства здравоохранения и социального развития РФ, болезнями глаз и глазного аппарата страдают около 4,7 млн человек в России [1]. На долю вирусных конъюнктивитов приходится около трети от всех офтальмологических патологий, при этом по результатам проведенного маркетингового анализа установлено, что одной из наиболее эффективных противовирусных субстанций на российском рынке является ацикловир [2].
Возможности методов идентификации и количественного определения ацикловира определяются его принадлежностью к производным пуриновых нуклеозидов [3]. Однако поиски и разработка новых более модифицированных методов анализа данного вещества не теряют своей актуальности и по сей день. В научной литературе широко представлены методы анализа определения количественного содержания ацикловира в различных лекарственных формах, однако отсутствует информация о возможности количественного определения ацикловира в водных растворах, в связи с низкой растворимостью ацикловира в воде и не применяющегося ввиду этого в наиболее широкого распространенной и удобной лекарственной форме в офтальмологии – глазных каплях. Целью исследования является изу чение растворимости ацикловира в модельных смесях с солюбилизатором бета-циклодекстрином.
Материалы и методы исследования
Ацикловир USP 29; бета-циклодекстрин USP 29; ВЭЖХ.
Результаты исследования и их обсуждение
Разработка современного комплексного препарата для лечения конъюнктивитов не может быть осуществлена без разработки современного метода анализа. В ходе изучения научной и патентной литературы данных было установлено, что основным методом анализа ацикловира в различных лекарственных формах в общемировой практике является высокоэффективная жидкостная хроматография.
ВЭЖХ, интенсивно развиваясь несколько последних десятилетий, зарекомендовала себя в качестве одного из самых универсальных методов разделения и фармакопейного анализа субстанций и лекарственных средств.
При этом требования к проведению анализа ацикловира несколько отличаются в нормативной документации различных стран. Так, ГФ XII[4] предлагает метод обращенно-фазовой ВЭЖХ для субстанции ацикловира, от него не отличаются методики, представленные в Украинской фармакопее (УФ)[5], Белорусской фармакопее (БФ)[6], Британской фармакопее (BP) [7]. При этом в БФ и BP приведено описание возможных примесей в субстанции ацикловира, как и в Японской (JP) [8] и Американской (USP) [9] фармакопеях.
В табл. 1 приведена сравнительная характеристика условий высокоэффективной жидкостной хроматографии для количественного определения ацикловира.
Таблица 1
Сравнительная характеристика методов анализа ацикловира методом ВЭЖХ в различных фармакопеях мира.
|
Фармакопеи, страна |
Условия хроматографирования |
|||||||
|
Подвижная фаза |
Колонка |
Скорость потока, объем пробы |
Детектор, длина волны, |
Количество примесей |
Время хроматогра-фирования |
Число теоре-тических тарелок |
||
|
ГФ XII |
6,0 натрия дигидрофосфата, 1,0 натрия дисульфоната до рН 3+/-1 кислотой фосфорной, 40 мл ацетонитрила и до 1000 мл воды |
Длина 0,10 м, внутренний диаметр 4,6 мм Октадецильный силикагель 3 мкм для хроматографии |
2 мл/мин, проба 20 мкл |
Спектро-фото-метрический, 254 нм |
Не более 0,7 % гуанина Не более 0,5 % любой другой примеси |
7-кратное удерживание времени ацикловира |
Не указано |
|
|
УФ (украинская фармакопея) |
Не отличается от ГФ XII |
|||||||
|
БФ(белорусская фармакопея) |
Не отличается от ГФ XII |
|||||||
|
BP (британская фармакопея) |
Не отличается от ГФ XII |
|||||||
|
USP 29 (американская фармакопея) |
Раствор уксусной кислоты профильтро-ванный и дегазиро- ванный (1:1000) |
Длина 0,25 м Внутренний диаметр 4,6 мм Сорбент типа L1 (для капсул внутренний диаметр 4,2 мм) |
3 мл/мин Проба 20 мкл (в инъек-ционном растворе 1 мл/мин)для капсул 1,5 мл/мин, |
Спектрофотометрический, 254 нм |
Гуанина не более 0,7 % |
Время хроматогра-фирования – 56 минут |
Не указано |
|
|
JP 16 (японская фармакопея) |
Мобильная фаза А: ацетонитрил R, фосфатный буфер раствора с pH 2,5 |
Длина колонки 0,15 м, внутренний диаметр 4,6 мм Сорбент – октадецильный силикагель для хроматографии |
3 мл/мин Объем пробы 5 мл |
Спектрофотометрический, 254 нм |
Гуанина не более 0,7 % |
Время удержания – 7 минут |
Не указано |
|
|
EPh (европейская фармакопея) |
Смесь растворителей: ДМСО R, R вода (20:80 V / V). Фосфатный буферный раствор рН 2,5. 3,48 г дикалия гидрофосфата R в 1000 мл воды R рН до 2,5 с фосфорной кислотой до рН 3,1. |
Длина колонки 0,25 м, внутренний диаметр 4,6 мм Сорбент – октадецильный силикагель для хроматографии, 5 мкм |
1 мл/мин Объем пробы 10 мкл |
Спектро-фото-метрический, 254 нм |
Гуанина не более 0,7 % |
Время удержания – 7 минут |
Не указано |
|
Как видно из табл. 1, в силу распространенности ацикловира в различных лекарственных формах в этих странах, требования к проведению анализа методом ВЭЖХ несколько разнятся. Европейская фармакопея 2010 (EPh) [10] предлагает использование колонки 25×0,46 см против требований в ГФ XII 10×0,46 см, отличается также скорость потока в минуту: 1 мл против 2 мл соотвественно, отличается и объем пробы, составляющий 10 мкл раствора для EPh и 20 мкл для ГФ XII. При этом в ГФ XII в качестве одного из компонентов подвижной фазы предложено использование натрия фосфата в ацетонитриле против калия дигидрофосфата в диметилсульфоксиде и ацетонитриле. Требования к ВЭЖХ между собой ГФ XII и BP 2009 не отличаются.
Несколько отличаются между собой методики ГФ XII и USP 29, в первую очередь, длиной хроматографической колонки, что объединяет требования USP 29 и EPh, однако, скорость подачи потока, согласно требованиям USP 29 составляет 3 мл в минуту, что отличает эту методику от прочих. При этом скорость потока для различных лекарственных форм вариабельна в силу химических и технологических особенностей приготовления. Так, малая скорость подачи потока сольвента для инъекционного раствора ацикловира характеризуется необходимостью особенно высокой точности разделения пиков на хроматограмме, что возможно удлиняет время хроматографирования.
Ввиду широкого применения активной фармацевтической субстанции ацикловира для количественного определения ацикловира в водных растворах при разработке методики повышения растворимости ацикловира был выбран способ обращенно-фазовый как оптимальный для решения поставленных задач.
На рис. 1 представлен алгоритм количественного определения ацикловира методом ВЭЖХ в образцах, полученных по различным технологическим методикам.
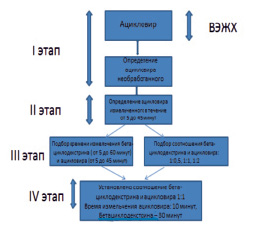
Рис. 1. Алгоритм количественного определения ацикловира методом ВЭЖХ
Как видно из рис. 1, исследование включает 4 этапа. На первом этапе исследования изучали растворимость ацикловира методом обращенно-фазовой ВЭЖХ, разрабатывали и апробировали методику анализа методом ВЭЖХ. На втором этапе исследования изучали количество ацикловира, перешедшего в раствор, в зависимости от времени измельчения в вибрационной шаровой мельнице МЛ-1. На третьем этапе исследования подбирали время измельчения бета-циклодекстрина и ацикловира, для обеспечения максимального количества перешедшего в раствор ацикловира одновременно с подбором оптимального соотношения бетациклодекстрина и ацикловира. На четвертом этапе исследования определили оптимальное время измельчения ацикловира, составляющее около 10 минут, бетациклодекстрина – 30 минут. Оптимальное соотношения ацикловира к бетациклодекстрину составляет 1:1.
На первом этапе исследования подбирали состав раствора подвижной фазы и раствора сравнения для апробации методики количественного определения ацикловира методом обращенно-фазовой ВЭЖХ.
Приготовление раствора подвижной фазы: около 6 г натрия фосфата однозамещенного и 1,0 натрия декансульфоната растворяют в 900 мл воды, доводят рН раствора до 3–3,1 фосфорной концентрированной кислотой, прибавляют 40 мл смеси ацетонитрила и разбавляют водой до 1000 мл.
Испытуемый раствор: 0,1 г ацикловира растворяют в 100 мл воды очищенной при перемешивании в ультразвуковом гомогенизаторе Bandelin HD Sonoplus 3200 в течение 7 минут с амплитудой около 50 %, затем 1 мл раствора переносят в колбу на 100 мл, доводят до метки водой очищенной, затем 1 мл раствора доводят до метки водой очищенной в колбе на 25 мл.
Раствор сравнения: около 0,01 испытуемого раствора помещают в мерную колбу вместимостью на 50 мл и доводят объем раствора подвижной фазой до метки, затем 1 мл доводят в колбе на 100 мл объем раствора подвижной фазой до метки.
В ходе работы были выявлены следующие оптимальные условия хроматографического разделения исследуемых веществ [7]:
Хроматографическая система – Shimadzu LC-20 Prominence (Kyoto, Япония), снабженная насосом LC-20AD, дегазатором DGU-20 A5, термостатом CTO-20A, диодно-матричным детектором – SPD-M20A, автодозатором – SIL-20AC – Rack 1.5 ml в режиме охлаждения (4 ºC) для обеспечения стабильности анализируемых проб.
Результаты, удовлетворяющие поставленным задачам по разделению исследуемых веществ, были получены с применением аналитической колонки – Supelco Ascentis Express C18 100×4,6 мм, 2,7 мкм в режиме термостатирования при 30 °С. Детекцию проводили спектрофотометрически при длине волны 254 нм. Объем вводимой пробы составил 10 мкл.
Скорость потока составила 2 мл/мин.
Количественное содержание веществ (Xi, мг/мл) в препарате рассчитывали по формуле 1:
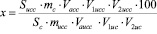 , (1)
, (1)
где Sисс – среднее значение площадей пиков испытуемого раствора; Sс – среднее значение площадей пиков стандартного ацикловира; mс – масса навески стандартного образца ацикловира, г; mисс– масса навески испытуемого образца ацикловира, г; Vacc – объем препарата, взятый для анализа, мл; V1исс – объем первого разведения раствора испытуемого образца, V2исс – объем второго разведения раствора испытуемого образца, V1ис – объем первого разведения стандартного раствора образца, V2ис – объем второго разведения раствора испытуемого образца, х – содержание основного вещества в стандартном образце ацикловира, г.
В результате эксперимента были получены хроматограммы ацикловира (рис. 2), Как видно из данных, представленных на рис. 1, ацикловиру соответствует пик со временем удерживания около 3 минут.
Полученные пики характеризуются достаточной интенсивностью и симмет ричностью.
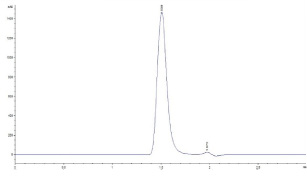
Рис. 2. Хроматограмма раствора ацикловира (образца сравнения)
Исходя из данных хроматограммы раствора ацикловира, представленного на рис. 3, для ацикловира характерно наличие одного пика со временем удерживания 1,5 мин. Как видно из полученных результатов, пики ацикловира на хроматограмме раствора ацикловира, измельченного в течение 10 минут, и ацикловира, измельченного в течение 10 минут с бета-циклодекстрином, совпадают по времени удерживания с таковыми на хроматограмме исследуемого вещества, что свидетельствует о возможности применения разработанной методики для разделения и анализа указанного соединения.
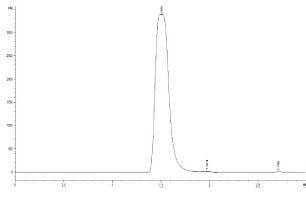
Рис. 3. Хроматограмма раствора измельченного ацикловира в течение 10 минут
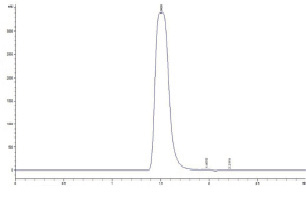
Рис. 4. Хроматограмма раствора измельченного ацикловира в течение 10 минут с бета-циклодекстрином, измельченным в течние 30 минут, 1:1
Концентрация исследуемого вещества была рассчитана по величине площадей их пиков с учетом полученных хроматограмм стандартного образца ацикловира. Полученные результаты и результаты их статистической обработки представлены в табл. 2.
Таблица 2
Результаты количественного определения ацикловира методом ВЭЖХ
|
Определяемое вещество |
Определено (Х, мг/мл) |
S2 |
S |
Δх, р = 0,95 |
ε, % |
|
Ацикловир |
2,85 |
0,0001 |
0,01 |
0,01 |
0,04 |
|
2,84 |
|||||
|
2,83 |
|||||
|
2,84 |
|||||
|
2,85 |
|||||
|
2,83 |
|||||
|
Хср = 2,84 |
Как видно из табл. 2, относительная ошибка опыта не превышает 5 %, для ацикловира относительное стандартное отклонение составляет 0,01 % при определенной в опыте концентрации 2,84 ± 0,01 мг/мл.
На втором этапе исследования изучали изменения растворимости ацикловира при использовании такого технологического приема, как введение солюбилизаторов. Известно, что бета-циклодекстрин представляет собой один из наиболее перспективных солюбилизаторов [6], поэтому на втором этапе исследования была выдвинута гипотеза, что возможно повышение растворимости ацикловира в комплексе с бета-циклодекстрином. На этом этапе исследования изучали оптимальное время измельчения навески ацикловира с бета-циклодекстрином 1:1 при совместном и раздельном супрамикроструктурировании в течение от 5 до 60 минут. Количество ацикловира, перешедшего в раствор, изучали методом ВЭЖХ.
Полученные результаты при совместном микродиспергировании ацикловира с бетациклодекстрином представлены в табл. 3.
Таблица 3
Изучение растворимости ацикловира с b-циклодекстрином 1:1 при совместном супрамикроструктурировании от 5 до 60 минут
|
Время измельчения |
Площадь пика, maU×S |
Количество перешедшего в раствор ацикловира, мг |
|
5 минут |
1549,52 |
2,85 |
|
10 минут |
3146,03 |
5,79 |
|
15 минут |
4625,24 |
8,52 |
|
30 минут |
5864 |
10,8 |
|
45 минут |
5650,97 |
10,41 |
|
60 минут |
4703,11 |
8,66 |
Как видно из табл. 3, максимальное количество ацикловира, перешедшего в раствор, наблюдается у ацикловира и b-CD, измельченных совместно в течение 30 минут.
Результаты, полученные при раздельном измельчении субстанций ацикловира и бета-циклодекстрина при соотношении 1:1, представлены в табл. 4.
Таблица 4
Изучение растворимости ацикловира, супрамикроструктурированного в течение 10 минут и супрамикроструктурированного b-циклодекстрина 1:1
|
Время измельчения b-циклодекстрина |
Площадь пика, maU×S |
Количество перешедшего в раствор ацикловира, мг |
|
5 минут |
6203,23 |
11,43 |
|
10 минут |
6729,33 |
12,39 |
|
15 минут |
6861,75 |
12,62 |
|
30 минут |
11765 |
21,67 |
|
45 минут |
9098,41 |
16,76 |
|
60 минут |
6328,04 |
11,65 |
Как видно из табл. 4, наибольшее количество ацикловира, перешедшего в раствор, наблюдается при времени измельчения b-циклодекстрина в течение 30 минут. Следовательно, оптимальное время супрамикроструктурирования b-циклодекстрина составляет 30 минут.
Также на втором этапе исследования растворимости ацикловира изучали подбор оптимального соотношения ацикловира к бета-циклодекстрину в соотношении от 1:0,5 до 1:2.
Результаты, полученные при измельчении ацикловира с бета-циклодекстрином в соотношении 1:0,5, представлены в табл. 5.
Как видно из табл. 5, максимальное количество ацикловира переходит в раствор при супрамикроструктурировании b-циклодекстрина в течение 30 минут, около 17,94 мг из навески около 100 мг, что несколько меньше, чем у соотношения ацикловира и бетациклодекстрина 1:1. Поэтому соотношение 1:0,5 использовать нецелесообразно.
Таблица 5
Изучение растворимости ацикловира, супрамикроструктурированного в течение 10 минут и супрамикроструктурированного b-циклодекстрина 1:0,5
|
Время измельчения b-циклодекстрина |
Площадь пика, maU×S |
Количество перешедшего в раствор ацикловира, мг |
|
5 минут |
4435,13 |
8,42 |
|
10 минут |
8227,71 |
14,94 |
|
15 минут |
8571,4 |
15,56 |
|
30 минут |
9878,12 |
17,94 |
|
45 минут |
6159,75 |
11,19 |
|
60 минут |
4271,56 |
47,75 |
Таблица 6
Изучение растворимости ацикловира, супрамикроструктурированного в течение 10 минут и супрамикроструктурированного b-циклодекстрина 1:2
|
Время измельчения b-циклодекстрина |
Площадь пика, maU×S |
Количество перешедшего в раствор ацикловира, мг |
|
5 минут |
3986,85 |
7,34 |
|
10 минут |
4832,97 |
8,9 |
|
15 минут |
7655,84 |
14,1 |
|
30 минут |
7819,91 |
14,4 |
|
45 минут |
4500,86 |
8,29 |
|
60 минут |
2239,98 |
4,12 |
Полученные результаты при изучении растворимости ацикловира с бета-циклодекстрином в соотношении 1:2, представлены в табл. 6.
Как видно из табл. 6, с увеличением количества b-циклодекстрина, количество перешедшего ацикловира в раствор снижается, при этом при супрамикроструктурировании b-циклодекстрина в течение 30 минут наблюдается максимальное количество перешедшего в раствор ацикловира при данном соотношении субстанций.
Следовательно, соотношение ацикловира и b-циклодекстрина 1:2 при времени измельчения ацикловира в течение 10 минут и b-циклодекстрина в течение 30 минут нецелесообразно использовать.
На четвертом этапе исследования установлено, что максимальное количество ацикловира переходит в раствор при раздельном супрамикроструктурировании ацикловира в течение 10 минут и супрамикроструктурировании бета-циклодекстрина в течение 30 минут при соотношении субстанций 1:1 в вибрационной шаровой мельнице МЛ-1 и составляет около 21,67 мг, что превышает растворимость субстанции, не подвергнутой супрамикроструктурированию в раз, и растворимость субстанции, подвергнутой измельчению в течение 10 минут без бета-циклодекстрина в 8 раз, что является перспективным для создания глазных капель на основе ацикловира.
Выводы
Таким образом, разработанная методика ВЭЖХ идентификации ацикловира в водных растворах может быть использована при анализе водных растворов ацикловира при разработке состава и технологии глазных капель противовирусного действия на основе ацикловира.
Рецензенты:
Степанова Э.Ф., д.ф.н., профессор кафедры «Технологии лекарств» Пятигорского медико-фармацевтического института – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск;
Голивец Т.П., д.м.н., профессор, заведующая кафедрой терапии ФПМО МИ НИУ «БелГУ», г. Белгород.
Работа поступила в редакцию 02.09.2014.



