Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
BEHAVIOR OF ALYUMINUM NITRIDE COMPOSITE NANOPOWDERS IN AQUEOUS MEDIA
В настоящее время активно исследуются пористые оксигидроксиды алюминия – продукты взаимодействия с водой электровзрывных нанопорошков алюмонитридной композиции (Al/AlN). Особенностями данных оксигидроксидов являются характерная морфология частиц из агломерированных нанопластин, высокая пористость, удельная поверхность, положительный заряд поверхности и высокая эффективность сорбции микроорганизмов. На основе частиц оксигидроксида алюминия, закрепленных на поверхности полимерных волокон, разрабатываются антимикробные повязки нетоксического действия, являющиеся эффективной альтернативой антибиотикам и антисептикам при лечении поверхностных ран [1─3]. Для целенаправленного регулирования получения продуктов с заданными и постоянно воспроизводимыми характеристиками необходимо выявление закономерностей превращения нанопорошков Al/AlN в водных средах с учетом всех факторов, влияющих на протекание процесса.
В данной работе представлены результаты исследования зависимости основных макрокинетических параметров гидролиза нанопорошков Al/AlN, фазового состава и текстурных характеристик оксигидроксидов алюминия от состава алюмонитридной композиции и условий проведения реакции.
Материалы и методы исследований
Нанопорошки алюмонитридной композиции получали методом электрического взрыва алюминиевой проволоки в атмосфере азота. Основные характеристики нанопорошков Al/AlN представлены в табл. 1.
Морфологию наночастиц алюмонитридной композиции и продуктов гидролиза исследовали методом просвечивающей электронной микроскопии («JEM-2100», JEOL). Распределение частиц алюмонитридной композиции по размерам рассчитывали по электронно-микроскопическим изображениям. Фазовый состав продуктов реакции исследовали на рентгеновском дифрактометре RD-6000 (Shimadzu) на CuKα-излучении с использованием баз данных PCPDFWIN. Текстурные характеристики продуктов гидролиза и исходных порошков алюмонитридной композиции определяли по тепловой десорбции азота и рассчитывали методом БЭТ (Сорбтометр М, Катакон).
Кинетику взаимодействия нанопорошков с водой исследовали методом непрерывной регистрации изменения рН и температуры реакционной смеси [4]. Реакцию проводили в течение 50 мин, продукты отфильтровывали, промывали дистиллированной водой, сушили при 105 °С.
Таблица 1
Основные характеристики нанопорошков состава Al/AlN [4]
|
№ п/п |
Среда взрыва, (P, атм) |
WAlN, % масс. |
WAl, % масс. |
Sуд, м2/г |
δ, Ǻ расчетное значение |
Среднемассовый размер агломератов, нм |
Средний размер частиц dа, нм |
|
1 |
Ar |
< 0,50 |
90 |
8 |
37 |
513 |
99,8 |
|
2 |
N2 (0,5) |
34 |
57 |
11 |
22 |
490 |
69,8 |
|
3 |
N2 (0,9) |
52 |
43 |
14 |
11 |
452 |
67,4 |
|
4 |
N2 (1,1) |
67 |
30 |
16 |
6 |
436 |
71,5 |
|
5 |
N2 (1,8) |
82 |
16 |
23 |
3 |
406 |
77,7 |
Массовую долю нитрида алюминия в нанопорошках определяли косвенным спектрофотометрическим методом (Spekol 1300) с использованием реактива Несслера [5]. Содержание активного алюминия определяли волюмометрическим методом [6]. Электрофоретическую подвижность частиц в воде определяли методом макроэлектрофореза [7]. ζ-потенциал частиц рассчитывали по уравнению Гельмгольца-Смолуховского. Адсорбцию эозина (С20Н6О5Br4K2) образцами оксигидроксида алюминия изучали в статических условиях, концентрацию красителя в растворах определяли спектрофотометрически («Spekol 1300») [8]. Исследование антимикробной активности проводили на примере палочковидных и кокковых культур микроорганизмов E. coli 7935, St. aureus 209, P. aeruginosa 27583 [9].
Результаты исследований и их обсуждение
Рассмотрение реакции алюмонитридной композиции следует начать с рассмотрения исходных нанопорошков. В отличие от нанопорошков алюминия, полученных в атмосфере аргона и имеющих сферическую форму частиц со средним размером 70–100 нм, частицы нанопорошков Al/AlN со средним размером 40–80 нм (рис. 1), как правило, огранены и объединены в агломераты размером около 500 нм.
Предположительно, частица алюмонитридной композиции представляет собой ядро из металлического алюминия, покрытое слоем нитрида алюминия. При пассивации нанопорошка на поверхности частиц образуется тонкая оксидная пленка, расчетные значения толщины которой для ряда нанопорошков Al/AlN приведены в табл. 1.
Массовая доля нитрида алюминия в нанопорошках Al/AlN зависит от условий получения порошка и может достигать 84 %. Увеличение содержания нитрида алюминия в Al/AlN приводит к увеличению удельной поверхности исходного порошка (рис. 2).

Рис. 1. ПЭМ-изображение нанопорошка Al/AlN с содержанием AlN 67 % масс.
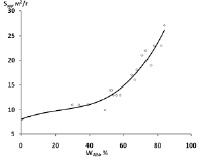
Рис. 2. Зависимость удельной поверхности Al/AlN от массовой доли AlN (WAlN) в композиции
Продуктом реакции алюмонитридной композиции с водой является псевдобемит AlOOH, реакция AlN и Al с водой сопровождается выделением аммиака (1) и водорода (2), соответственно:
ALN + 2H2O = ALOOH + NH3; (1)
2AL + 4H2O → 2ALOOH + 3H2↑. (2)
Кривые изменения рН имеют типичную для топохимических процессов S-образную форму интегральных зависимостей, а дифференциальные проходят через максимум [4]. Реакция нанопорошков Al/AlN с водой, судя по изменению рН реакционной среды, протекает в три стадии, включающие индукционный период, гидролиз поверхностного слоя наночастиц из нитрида алюминия и последующее окисление металлического алюминия.
На кривых газовыделения при реакции Al/AlN с водой наблюдался один максимум, обусловленный выделением газообразного водорода. Исследование скорости газовыделения показало, что окисление металлического алюминия в нанопорошке Al/AlN близко по времени ко второму пику на дифференциальной кривой изменения рН, что позволяет отнести второй максимум на дифференциальной кривой изменения рН к процессу окисления алюминиевого ядра наночастиц Al/AlN (рис. 3).
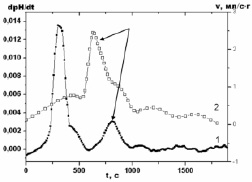
Рис. 3. Дифференциальная кривая изменения рН (1) и кривая скорости газовыделения (2)
Увеличение массовой доли нитрида алюминия в нанопорошках Al/AlN способствует сокращению времени реакции и изменению ее закономерностей. При содержании нитрида алюминия менее 50 % масс. реакция протекает с выраженным индукционным периодом, далее гидролиз нитрида алюминия и окисление алюминия идут одновременно. При 50−60 % масс. нитрида алюминия реакция идет в три стадии, а при 60 % масс. и более нанопорошки реагируют с водой без различимого индукционного периода в две последовательные стадии: гидролиз нитрида алюминия и окисление алюминия. Это связано с увеличением удельной поверхности порошков Al/AlN с возрастанием содержания нитрида алюминия и, соответственно, увеличением площади реагирующей поверхности.
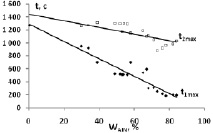
Рис. 4. Зависимость времени превращения нитрида алюминия (а) и металлического алюминия (б) от массовой доли нитрида алюминия в композиции
При этом наблюдается сокращение времени превращения как нитрида алюминия (рис. 4, t1max), так и металлического алюминия. (рис. 4, t2max).
При исследовании влияния температуры на закономерности превращения Al/AlN (массовая доля нитрида алюминия в исходной композиции WAlN = 52 % масс.) было установлено, что при 30–60 °С три последовательные стадии реакция сохраняются, увеличение температуры приводит к ускорению гидролиза нитрида алюминия и окисления алюминия, которые при температуре 80 °C и выше идут одновременно [8]. Кроме того, с ростом температуры сокращается индукционный период вплоть до полного исчезновения при 70 °C и выше.
Скорость превращения нанопорошков алюмонитридной композиции зависит также от рН исходной реакционной смеси. При рН 4–6 видимых признаков реакции не наблюдалось даже в течение 90 мин. Повышение рН реакционной смеси от 7 до 9 приводит к росту скорости превращения металлического ядра наночастицы с 2,3 до 2,8 мл∙с/г и сокращению индукционного периода. При рН более 9 образцы реагируют полностью менее чем за 5 минут.
Вне зависимости от температуры проведения реакции, рН и массовой доли нитрида алюминия в нанопорошках продукты реакции имеют форму нанолистов толщиной 5–10 нм и размером 150–300 нм, агломерированных в близкие к сферическим кораллоподобные структуры (рис. 5) [10].
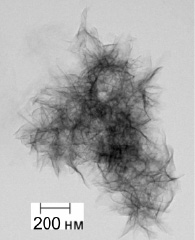
Рис. 5. ПЭМ-изображение продуктов превращения порошка алюмонитридной композиции
Фазовый состав продуктов реакции с водой нанопорошков Al/AlN, как и нанопорошка Al, представлен, в основном, псевдобемитом AlOOH [8]. В образцах, полученных при 30–50 °С, присутствует также фаза байерита Al(OH)3, содержание которой с повышением температуры до 60−70 °С снижается практически до нуля. Байерит образуется из псевдобемита в водной среде относительно медленно и обнаруживается методом РФА только в образцах, полученных при низких температурах и, соответственно, достаточно длительным ведении процесса. При 80 °С помимо псевдобемита обнаруживается около 1 % непрореагировавшего металлического алюминия. Изменение состава алюмонитридной композиции и рН реакционной смеси от 6,5 до 11,0 не оказывает влияния на фазовый состав продуктов реакции.
По виду изотерм адсорбции-десорбции все образцы относятся к материалам с щелевидными мезопорами с характерными петлями гистерезиса в области капиллярной конденсации. С увеличением массовой доли нитрида алюминия наблюдается уширение петли гистерезиса и увеличение объема мезопор с 0,363 см3/г для 1 образца до 0,439 см3/г для 5 образца. Однако, вне зависимости от состава нанопорошка Al/AlN, средний размер пор продуктов взаимодействия с водой составляет 4…10 нм. Увеличение содержания нитридной фазы в образце приводит к увеличению удельной поверхности продуктов реакции от 255 до 357 м2/г, ζ-потенциал возрастает с 36 до 48 мВ, а величина адсорбции тестового адсорбата эозина увеличивается с 3,96 до 4,68 мг/г.
Удельная поверхность продуктов реакции Al/AlN с водой, полученных в изотермических условиях, зависит от температуры проведения реакции и достигает максимального значения 330 м2/г при 60–70 °C. При повышении температуры до 80 °C удельная поверхность оксигидроксида алюминия уменьшается, вероятно, за счет снижения степени превращения частиц Al/AlN и повышения плотности агломератов.
Важной характеристикой, определяющей адсорбционную активность оксигидроксида алюминия по отношению к микроорганизмам, является электроположительный заряд поверхности, который оценивают по величине ζ-потенциала. Как оказалось, величина ζ-потенциала частиц оксигидроксида алюминия в воде зависит от температуры синтеза. Максимальный ζ-потенциал 46 мВ характерен для образцов, полученных при 60–70 °C. При этом величина адсорбции эозина также достигает максимума.
Таблица 2
Основные характеристики продуктов реакции Al/AlN
|
№ п/п |
Температура синтеза Тс, °C |
Sуд, м2/г |
Адсорбция эозина Аэозина, мг/г |
ζ-потенциал, мВ |
|
1 |
30 |
280 ± 3 |
3,76 ± 0,02 |
38,2 ± 0,1 |
|
2 |
40 |
270 ± 2 |
3,19 ± 0,04 |
38,4 ± 0,2 |
|
3 |
50 |
280 ± 2 |
3,67 ± 0,02 |
41,2 ± 0,2 |
|
4 |
60 |
330 ± 3 |
4,38 ± 0,07 |
45,0 ± 0,3 |
|
5 |
70 |
291 ± 2 |
4,37 ± 0,09 |
46,1 ± 0,3 |
|
6 |
80 |
274 ± 2 |
4,33 ± 0,07 |
41,2 ± 0,1 |
Полученные образцы оксигидроксида алюминия эффективно адсорбируют из водных сред микроорганизмы. Так, при исследовании антимикробной активности было показано, что эффективность удержания бактерий P. Aeruginosa, E. coli и St. aureus составляет 75, 87 и 93 %, соответственно [9].
Таким образом, температура и время проведения реакции играют важную роль при формировании фазового состава и пористой системы оксигидроксида алюминия. При температурах 30–50 °C и длительности реакции более 3 ч наблюдается формирование фазы байерита и, как следствие, снижение удельной поверхности и ζ-потенциала продуктов реакции. Проведение реакции при 60–70 °C способствует сокращению времени реакции и образованию псевдобемита, как основного продукта реакции с удельной поверхностью более 330 м2/г, максимальным значением ζ-потенциала и высокими сорбционными характеристиками по отношению к эозину и бактериям различной морфологии. При 80 °C высокая скорость реакции и образование плотного слоя продуктов реакции на поверхности частицы приводят к неполной конверсии Al/AlN, снижению удельной поверхности и сорбционных характеристик продуктов реакции.
Работа выполнена при финансовой поддержке ГК 14.527.12.0001 и Программы фундаментальных исследований III.23.2.3.
Выводы
1. По изменению рН реакционной смеси изучены закономерности превращения нанопорошков алюмонитридной композиции в водных средах в зависимости от массовой доли нитрида алюминия в композиции. Превращение композиций протекает в три макрокинетические стадии: индукционный период, гидролиз нитрида алюминия на поверхности наночастиц и последующее окисление металлического алюминиевого ядра. При содержании нитрида алюминия 30−50 % масс. наблюдается выраженный индукционный период, далее гидролиз нитрида алюминия и окисление алюминия идут одновременно, Превращения композиций, содержащих 50−60 % масс. нитрида алюминия, протекают в три последовательные стадии, а при 60 % масс. и более нанопорошки реагируют с водой без индукционного периода в две стадии – гидролиз нитрида алюминия и окисление алюминия.
2. Исследовано влияние внешних условий на закономерности превращения нанопорошков алюмонитридной композиции и физико-химические свойства продуктов. С увеличением температуры от 30 до 60 °С скорость превращения возрастает, индукционный период сокращается, а на кривой изменения рН наблюдаются два максимума – гидролиз нитрида алюминия и окисление алюминия. Выше 70 °С реакция идет без индукционного периода, при 80 °С гидролиз нитрида алюминия и металлического алюминиевого ядра протекают одновременно в одну стадию с максимальной скоростью. Изменение исходного рН реакционной среды с 6,5 до 11,0 приводит к увеличению скорости превращения прекурсора.
3. Величина ζ-потенциала частиц оксигидроксида алюминия в воде зависит от температуры синтеза. Максимальный ζ-потенциал 46 мВ характерен для образцов, полученных при 60–70 °C. При этом величина адсорбции тестового адсорбата эозина также достигает максимума.
4. Исследование текстурных характеристик, ζ-потенциала и адсорбционных свойств продуктов реакции алюмонитридной композиции с водой показало, что с увеличением массовой доли нитрида алюминия в исходной композиции от 30 до 80 % удельная поверхность продуктов увеличивается с 259 до 357 м2/г, ζ-потенциал возрастает с 36 до 48 мВ, а величина адсорбции эозина увеличивается с 3,96 до 4,68 мг/г.
Рецензенты:
Мамаева В.А., д.т.н., научный руководитель технологической группы ООО «Сибспарк» – резидента особой экономической зоны, г. Томска;
Коботаева Н.С., д.х.н., старший научный сотрудник Учреждения Российской академии наук Институт химии нефти Сибирского отделения РАН, г. Томск.
Работа поступила в редакцию 22.02.2013.
Библиографическая ссылка
Бакина О.В., Сваровская Н.В., Глазкова Е.А., Ложкомоев А.С., Хоробрая Е.Г., Лернер М.И. ЗАКОНОМЕРНОСТИ ПРЕВРАЩЕНИЯ НАНОПОРОШКОВ АЛЮМОНИТРИДНОЙ КОМПОЗИЦИИ В ВОДНЫХ СРЕДАХ // Фундаментальные исследования. 2013. № 4-4. С. 862-867;URL: https://fundamental-research.ru/en/article/view?id=31287 (дата обращения: 14.05.2026).



