Обонятельные сигналы играют важную роль в коммуникации млекопитающих, определяя многие аспекты их поведения. Большинство видов млекопитающих принадлежит к макросматикам. Для таких животных именно анализ запаховых раздражителей является определяющим в организации сложных форм поведения, от которых зависит их выживание.
На сегодняшний день актуальность исследования химической коммуникации не вызывает сомнений. Межвидовая химическая коммуникация млекопитающих по сей день остаётся наименее исследованной областью и, в особенности, такой важный аспект, как химическая коммуникация между хищником и потенциальной жертвой. Хорошо известен факт избегания запаха хищника потенциальной жертвой. Такого рода исследования открывают возможности разработки нетоксичных препаратов для регуляции численности грызунов, которые не вызывают привыкания при многократных применениях и наиболее стабильны. Например, для серой крысы адаптация к применяемым для регуляции численности токсичным препаратам является самой серьезной проблемой [2]. Химические сигналы, используемые в коммуникации, не только играют роль информационных посредников, но также способны оказывать влияние на физиологические процессы, протекающие в организме животного. В литературе описан эффект сокращения размера выводка у лабораторных крыс под влиянием запаха домашней кошки [8], описаны гормональные механизмы наблюдаемого явления [9]. Запах домашней кошки также оказывает достоверное влияние на длину эстрального цикла у грызунов и долю циклирующих самок в группе [10, 5]. Установлено, что биологическая активность мочи домашней кошки обусловлена наличием серосодержащих веществ с низкой летучестью [11, 12]. L-фелинин является уникальной серосодержащей аминокислотой, обнаруженной в моче кошачьих [4]. В настоящее время L-фелинин рассматривается как феромон кошачьих [6]. L-Фелинин синтезируется в почках. Продукция L-фелинина зависит от типа диеты кошки, возраста, пола, сезона размножения. Содержание мяса в диете способствует повышению вывода L-фелинина с мочой. У домашней кошки концентрация L-фелинина в моче повышается в весенний период. Кастрация достоверно снижает синтез L-фелинина. Принимая во внимание многочисленные исследования по влиянию запаха домашней кошки на поведение и репродукцию домовой мыши, L-фелинин может претендовать на роль кайромона у грызунов.
Целью данной работы являлось исследование сезонной вариабельности в чувствительности к феромону кошачьих L-фелинину в отношении подавления размножения у серой крысы Rattus norvegicus.
Материалы и методы исследования
В экспериментах использовались крысы лабораторной гетерогенной популяции, имеющие своими предками особей, отловленных в естественных биотопах. Животные содержались в стандартных клетках размером 36×50×16; вода, зерно и комбикорм для грызунов («Лабораторкорм») были в свободном доступе. Световой режим соответствовал естественному освещению. Температура в помещении варьировала от 20 до 22 °С. Использовались половозрелые животные в возрасте 3–4 месяцев. Для спаривания использовали сексуальноопытных самцов, содержавшихся по одному в клетке не менее 14 дней. Стадии эстрального цикла самок определяли по соотношению основных клеточных элементов во влагалищном смыве. Самок на стадии проэструса-эструса ссаживали с самцами на 16–18 часов и регистрировали основные элементы полового поведения: назо-анальные контакты, попытки садок, попытки садок с интромиссиями. На следующее утро успешность спаривания определяли по наличию влагалищной пробки из сперматозойдов. Успешно спарившихся крыс рассаживали по одной в клетку. Этот день считали первым днем беременности. Моча домашней кошки (Felis catus) использовалась как источник химических сигналов симпатрического хищника; L-фелинин (US Biologicals) в концентрации, сопоставимой с естественной в моче хищника (0,05 %), использовался как потенциальный активный ингредиент. Моча собиралась в эмалированную посуду и хранилась при –20 °С до момента использования. В качестве контроля использовалась вода. Экспозиции к запахам проводили с использованием перфорированных пластиковых контейнеров с фильтровальной бумагой, смоченной 0,2 мл соответствующего раствора. Контейнер прикреплялся к верхней крышке клетки самки. Обновление растворов производили каждые два дня на протяжении всего периода беременности. Для определения репродуктивного успеха и плодовитости самок оценивались следующие параметры: размер выводка, соотношение детенышей в выводке по полу, вес детенышей к 21-му дню развития, а также количество выживших детёнышей к 21-му дню развития. Было выполнено два независимых эксперимента: в осенне-зимний период и в весенне-летний.
Результаты исследования и их обсуждение
Экспозиция беременных самок крыс к моче домашней кошки на протяжении всего периода беременности в осенне-зимний период привела к достоверному снижению веса детенышей к моменту перевода на твердую пищу, т.е. в возрасте 21 дня (рис. 1) по сравнению с контрольной группой. Так, в экспериментальной группе вес детенышей в осенне-зимний период составил 53 ± 10 г (n = 102), тогда как в контроле 65 ± 10 г (n = 82). В группе, экспонированной к L-фелинину (0.05 %, US Biologicals), вес детенышей составил 55 ± 16 г (n = 101), что тоже достоверно отличается от контроля (p < 0,01, n = 82). Аналогичные результаты были получены и в весенне-летний период (рис. 2). Вес детенышей в группе, экспонированной к L-фелинину (0,05 %) на протяжении беременности, составил 42 ± 11 г (n = 68), а в контроле – 47 ± 11 г (n = 76, р < 0,05). Таким образом, как при экспозиции интактной мочи домашней кошки, так и при экспозиции феромона кошачьих L-фелинина, мы наблюдали достоверное снижение веса детенышей крыс к моменту отъема от матери.

Рис. 1. Влияние экспозиции беременных самок крыс Rattus Norvegicus к моче домашней кошки Felis catus и к феромону кошачьих L-фелинину (0,05 %, US Biologicals) на вес детенышей к моменту отъёма от матери (21-му дню развития) в осенне-зимний период. *** – p < 0,001, T – стандартная ошибка среднего
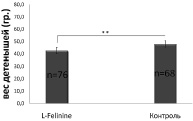
Рис. 2. Влияние экспозиции беременных самок крыс Rattus Norvegicus к феромону кошачьих L-фелинину (0,05 %, US Biologicals) на вес детенышей к моменту отъёма от матери (21-му дню развития) в весенне-летний период, ** – p < 0,01, n = 144, T – стандартная ошибка среднего
В выводках, экспонированных к фелинину (0,05 %), также наблюдалось достоверное (p < 0,001, n = 24) смещение соотношения по полу в сторону самцов по сравнению с контрольной группой (рис. 3). В основе данного эффекта может лежать дифференциальная резорбция эмбрионов [8].
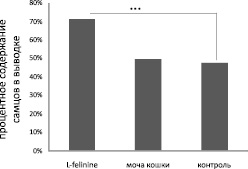
Рис. 3. Влияние экспозиции беременных самок крыс Rattus Norvegicus к феромону кошачьих L-фелинину (0,05 %, US Biologicals) на соотношение полов в выводках в осенне-зимний период. *** – p < 0,001, n = 24
Достоверное влияние L-фелинина на соотношение полов в выводке было отмечено только в осенне-зимний период. В весенне-летний период подобного эффекта не было обнаружено. Данный эффект можно объяснить более высокой уязвимостью репродуктивной системы в осенне-зимний период.
Экспозиция беременных самок крыс на протяжении беременности к интактной моче домашней кошки, феромону кошачьих фелинину как в осенне-зимний период, так и в весенне-летний приводила к достоверному снижению веса потомства к моменту отнятия от матери по сравнению с контролем. Наиболее логичным объяснением данного явления является снижение лактации у самок. Нашими более ранними исследованиями показано влияние запаха хищника на продукцию глюкокортикоидов [9]. Повышенный уровень глюкокортикоидов у лактирующих самок может негативным образом влиять на секрецию пролактина и проявление материнского поведения [13, 14, 1]. Изменение соотношения полов в пользу самцов под влиянием экспозиций химических сигналов хищника можно объяснить дифференциальной резорбцией эмбрионов, которая имеет место при понижении прогестерона на ранних стадиях беременности [8]. Общеизвестным фактом является сезонность размножения и, как следствие, сезонная чувствительность к хемосигналам других особей [3]. В осенне-зимний период фоновые значения продукции основных стероидных гормонов у крыс ниже, чем в весенне-летний период, поэтому даже небольшое снижение прогестерона может вести к изменению соотношения полов. Иными словами, репродуктивная система в осенне-зимний период более уязвима, чем в весенне-летний. С эволюционной точки зрения сдвиг по полу в сторону самцов в условиях высокой плотности хищников представляется адаптивным, поскольку самцы более мобильны и преодолевают расстояния, позволяющие им обосноваться на более благоприятной территории.
Таким образом, феромон кошачьих L-фелинин оказывает сходные в отношении подавления размножения серой крысы эффекты с интактной мочой домашней кошки. Снижение репродуктивного успеха под действием запаха хищника более выражено в осенне-зимний период, чем в весенне-летний. Подводя итог всему вышеизложенному, можно сделать следующее заключение: L-фелинин может выполнять функции межвидового химического сигнала, участвующего в регуляции репродукции серых крыс.
Исследования поддержаны Программой «Живая природа» и грантом Президента MK-709.2012.4.
Рецензенты:
Бутовский Р.О., д.б.н., профессор, программный директор Фонда «Устойчивое развитие» (ФУР), г. Москва;
Блохин Г.И., д.с.-х.н., профессор, заведующий кафедрой зоологии ФГБОУ ВПО РГАУ имени К.А. Тимирязева МСХ РФ, г. Москва.
Работа поступила в редакцию 23.01.2013.



