Нестабильность генома на хромосомном уровне (численные и структурные аномалии хромосом) является наиболее частой генетической причиной нарушения центральной нервной системы (ЦНС). В частности, по данным разных исследователей, подобные формы геномных вариаций связаны с 30–50 % случаев умственной отсталости у детей, 5–40 % – аутизма и 1–10 % – шизофрении [1, 4, 5, 16]. Известно также, что патогенез нейродегенеративных заболеваний, например, болезни Альцгеймера, связан с субмикроскопическими вариациями на хромосомном уровне, а также анеуплоидизацией тканей ЦНС [1, 6–8, 23, 44]. Более того, некоторые заболевания, которые рассматривают также в качестве молекулярных моделей нейродегенерации, представляют собой синдромы хромосомной нестабильности (например, атаксия-телеангиэктазия или АТ) [16, 28, 29]. Это позволяет сделать вывод о том, что геномные вариации и нестабильность, в частности, анеуплоидия, являются одним из значимых генетических факторов предрасположенности ко многим психическим и нейродегенеративным заболеваниям, а также связаны со старением мозга [1, 4, 17, 20, 24, 42].
Цель представленного научного обзора заключается в обсуждении результатов исследований нестабильности генома при атаксии-телеангиэктазии (АТ), синонимы – синдром Луи-Бар или синдром Бодер-Седжвика (OMIM#208900) [14, 34]. АТ является редким (орфанным) заболеванием, характеризующимся атаксией, окулокутанной телеангиэктазией, иммунодефицитом, повышенной радиочувствительностью, предрасположенностью к онкологическим заболеваниям, бесплодием, преждевременным старением и ранней мозжечковой нейродегенерацией. Несмотря на относительно низкую частоту (1 на 40000–100000), АТ – одна из наиболее частых форм наследственных атаксий. АТ является моногенным синдромом, связанным с мутациями в гене АТМ (ataxia telangiectasia mutated), основная функция которого заключается в репарации двунитевых разрывов последовательностей ДНК и поддержании целостности генома в клетке. Ген АТМ картирован в длинном плече хромосомы 11 в участке 11q22-q23 [15]. Отличительной чертой АТ является прогрессирующая мозжечковая нейродегенерация, которая поражает клетки Пуркинье и гранулярные нейроны [14, 28, 29]. Молекулярные и клеточные механизмы гибели нервных клеток мозжечка, а также связь патогенеза заболевания с нарушением стабильности генома вследствие мутаций гена АТМ остаются до сих пор неясными [29].
АТ относится к так называемым «синдромам хромосомной нестабильности» (CIN). Группа академика Н.П. Бочкова в 1974 году провела одно из первых в мире исследование нестабильности хромосом в группе больных АТ. Было проанализировано 2004 клетки от 23 больных АТ, где 151 клетка (7,5 %) содержала хромосомные аберрации. Наряду с данными перестройками в исследованных клетках наблюдалась эндоредупликация, полиплоидия, а также в одном случае анеуплоидия (потеря) хромосомы 7 [12]. По данным разных авторов, в клетках больных АТ наблюдают CIN, которая является следствием нарушения функционирования белка АТМ в ходе репарации двунитевых разрывов ДНК, при делении клеток и прохождении G1–S и G2 фаз клеточного цикла, а также при элиминации аномальных клеток в ходе апоптоза [28, 29]. Культивируемые in vitro лимфоциты больных АТ имеют высокую частоту спонтанных хромосомных перестроек, особенно с участием хромосом 7 и 14, и высокую частоту хромосомных перестроек после воздействия радиации [14, 33, 34]. В большинстве случаев точки разрывы не случайны и обнаруживаются в участках хромосом 7 (участки p14 и q35) и 14 (участки q12, и 14q32). Детальный цитогенетический анализ CIN показал, что наиболее часто перестройки затрагивают следующие районы хромосом: 7p14 (ген TCRγ), 7q35(TCRβ), 14q12 (TCRα/δ), 2p11,2p12, 22q12, 22q13.2 [10,14]. В 3 – 10 % лимфоцитов периферической крови у больных АТ обычно выявляют следующие хромосомные перестройки: inv(7)(p14q35), inv(14)(q12qter), t(7;14)(p14;q12), t(7;14)(q35;q12). Эти перестройки затрагивают гены иммуноглобулинов, в частности, ген α-цепи рецептора Т-клеток с локализацией в хромосоме 14 (участки q11-14q12) и гены β- и γ-цепей рецептора Т-клеток в хромосоме 7 (участки q35 и 7q14). Белок АTМ играет ключевую роль при соматической рекомбинации ДНК или V(D)J рекомбинации, в процессе который сегменты иммуноглобулинового гена – variable (V), diversity (D) and joining (J) – рекомбинируют для образования «зрелых» иммуноглобулиновых генов. Рекомбинация соматической ДНК необходима для продукции функциональных антигенов рецепторных генов в Т- и В-лимфоцитах. Нарушение данной функции белка АТМ приводит к характерным перестройкам, затрагивающим районы, участвующие в V(D)J рекомбинации. CIN среди индивидуумов – носителей мутаций в гене АТМ различна и может зависеть от типа мутаций, ее расположения в гене и от уровня и активности белка АТМ [14, 29]. Таким образом, CIN в клетках иммунной системы при АТ, проявляющаяся в виде повышенного уровня спонтанных хромосомных мутаций (хромосомных разрывов и транслокаций) с вовлечением хромосом 7 и 14, является значимым диагностическим маркером заболевания.
Парадоксальная особенность АТ, которая отмечается многими исследователями, связана с прогрессирующей мозжечковой дегенерацией, которая при наличии мутации в гене АТМ во всех клетках головного мозга, наблюдается преимущественно в мозжечке [28, 29]. Именно прогрессирующая мозжечковая дегенерация является основной причиной нарушений функций мозжечка и связана с высокой и ранней летальностью при этом неизлечимом заболевании ЦНС. Характерно, что другие отделы мозга больных не поражаются нейродегенерацией или нейродегенеративные процессы в них наступают на более поздних сроках заболевания [14, 29]. МакКиннон [28, 29], по-видимому, впервые обратил особое внимание на этот парадоксальный феномен, предположив, что ответ на вопрос о специфике нейродегенеративных процессов в разных отделах мозга при АТ позволит выяснить загадочную природу этого неизлечимого заболевания и разработать научно обоснованные методы его терапии.
Для объяснения этого парадокса, названного нами «парадоксом МакКиннона», была предложена гипотеза о связи прогрессирующей нейрональной гибели при АТ с повышенной хромосомной (геномной) нестабильностью, которая специфически поражает нейроны мозжечка [18]. Однако анализ генома клеток головного мозга больных АТ, в частности, мозжечка, до недавнего времени не проводился. Нашими лабораториями впервые проведены исследования нестабильности соматического генома в мозге при АТ, а также осуществлена попытка экспериментально найти объяснение «парадокса МакКиннона» с использованием оригинальных молекулярно-цитогенетических технологий и уникальных образцов аутопсийного мозга больных АТ, полученных из банка постмортальных тканей мозга Университета г. Мериленд, США (NICHD Brain and Tissue Bank for Developmental Disorders at the University of Maryland, Baltimore, USA) [2, 3, 9, 21–22].
Рассматривая проблемы нестабильности генома в головном мозге, необходимо отметить, что анеуплоидия (клетки с аномальным набором хромосом) присутствуют в разных типах тканей человека. Однако именно в мозге нестабильность генома на клеточном уровне может иметь особое патологическое значения из-за нарушений в функционировании нейрональных цепей и межклеточных взаимодействий типа нейрон-нейрон и нейрон-глия. Достаточно отметить тот факт, что каждый из 100 миллиардов нейронов головного мозга человека участвует в образовании от 1000 до 10000 синапсов с другими нейронами [32]. Поэтому весьма вероятно, что даже малое число аномальных нервных клеток, «внедренных» в нейрональные сети взрослого мозга, может оказать негативное влияние не только на клеточный гомеостаз индивидуальных нейронов или глиальных клеток, но и на функционирование всей нейрональной сети [16, 19, 43].
Таким образом, для объяснения парадокса МакКиннона [28, 29] и экспериментальной проверки оригинальной гипотезы Юрова И.Ю. с соавторами [18] о связи нестабильности генома с нейродегенерацией нами был проведен молекулярно-цитогенетический анализ особенностей CIN в клетках головного мозга больных с АТ (аутопсийные образца коры и мозжечка). Исследование хромосомных разрывов и анеуплоидии проведено с помощью многоцветовой интерфазной флюоресцентой гибридизации in situ (MFISH), интерфазного хромосомоспецифичного многоцветового окрашивания (ICS-MCB), иммуно-FISH и биоинформатического анализа как описано ранее [2, 21–22]. Примеры молекулярно-цитогенетического анализа анеуплоидии в клетках головного мозга в норме и при АТ показаны на рис. 1, 2.
В мозге больных АТ по сравнению с контролем выявлено 2–5-кратное (до 20–50 %) увеличение уровня анеуплоидии в коре и мозжечке. Кроме того, было выявлено 5-20-кратное увеличение числа клеток со специфическими разрывами хромосомы 7, 14 и Х в нервных клетках мозжечка, в то время как в других отделах мозга хромосомные аномалии не наблюдались [22]. Таким образом, наши данные в целом согласуются с гипотезой о патогенной роли нестабильности соматического генома в клетках мозжечка при АТ, и, по-видимому, представляют собой возможное объяснение парадокса МакКиннона.
Эти исследования открыли новые особенности организации и функционирования генома в клетках головного мозга при АТ, которые не удается объяснить, оперируя имеющимися в литературе данными. Во-первых, не ясно, почему резкое возрастание спонтанного уровня анеуплоидии при АТ, затрагивающее различные отделы мозга (префронтальная кора и мозжечок), не приводит к нарушениям функционирования мозга больных, например, как это наблюдается при хромосомных болезнях. Известно, что регулярные и мозаичные формы хромосомных болезней всегда негативно затрагивают функции головного мозга и проявляются в виде различных форм умственной отсталости, аутизма и эпилепсии [5–8, 17, 20]. Парадоксально, но этих психических нарушений при АТ нет (новый парадокс 1). Большинство исследователей не фиксируют нарушений когнитивных функций или психических заболеваний при АТ, а, наоборот, отмечают наличие нормального уровня интеллекта у больных АТ [14]. Тем не менее, имеются данные о том, что такие отклонения психики как умственная отсталость, встречаются у больных с АТ в 10 раз чаще, чем в нормальной популяции [31]. Связан ли этот новый парадокс с высокой пластичностью мозга или другими компенсаторными механизмами, блокирующими негативное влияние спонтанной анеуплоидии на функционирование ЦНС, или с недостаточно подробно описанным психическим статусом больных АТ, в настоящее время неясно.
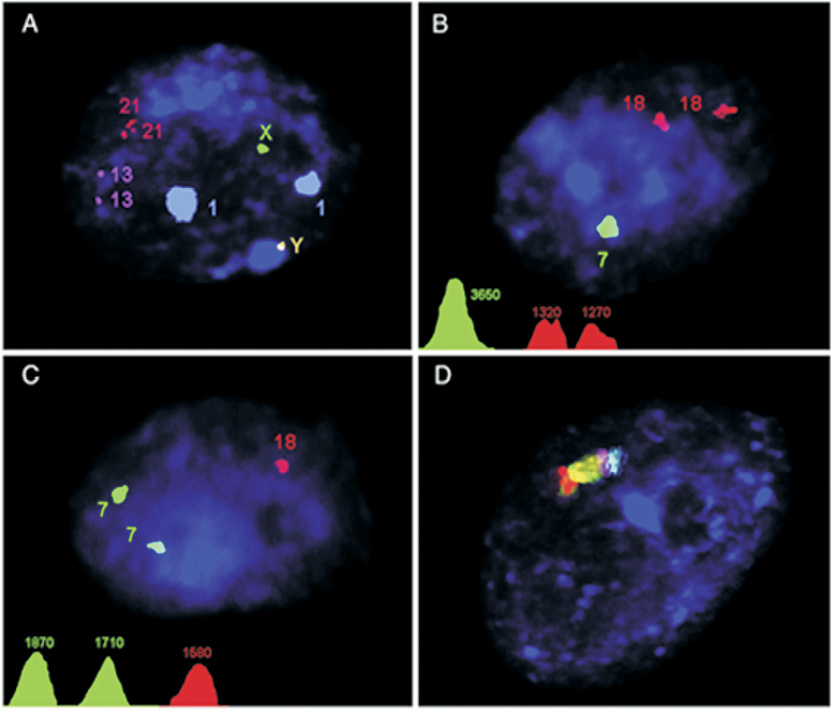
Рис. 1. Молекулярно-цитогенетический анализ анеуплоидии в клетках нормального мозга человека и при АТ (мозжечок). (А) MFISH с пятью ДНК-зондами на хромосому 21 (красные сигналы, участки 21q22-q22.22), хромосому 13 (розовые сигналы, участки 13q14), хромосому 1 (голубые сигналы, участок 1q12), хромосому Х (зеленые сигналы, участок Xp11-q11) и хромосому Y (желтые сигналы, участок Yp11-q11). (B) MFISH c ДНК-зондами на хромосому 7 (один зеленый сигнал, относительная интенсивность 3650 пикселей) и хромосому 18 (два красных сигнала, относительные интенсивности являются 1320 и 1270 пикселей), выявлено соматическое спаривание двух гомологичных хромосом 7 в нормальной диплоидной клетке мозга при AT. (C) Моносомия по хромосоме 18 в мозге при AT. MFISH с ДНК-зондами на хромосому 7 (два зеленых сигнала, относительная интенсивность каждого -1870 и 1710 пикселей соответственно) и 18 (один красный сигнал, относительная интенсивность составляет 1680 пикселей), т.е. выявлена дисомия по хромосоме и анеуплоидия (моносомия) по хромосоме 18. (D) Моносомия по хромосоме 14 (одна копия хромосомы на клетку), выявленная с помощью ICS-MCB с ДНК-зондами на всю хромосому 14 в нейроне мозжечка при AT. (Из работы [21], опубликованной в журнале «Neurobiology of Disease» c разрешением издательства ACADEMIC PRESS. Neurobiology of Disease by ACADEMIC PRESS. Reproduced with permission of ACADEMIC PRESS in the format reuse in a journal/magazine via Copyright Clearance Center)
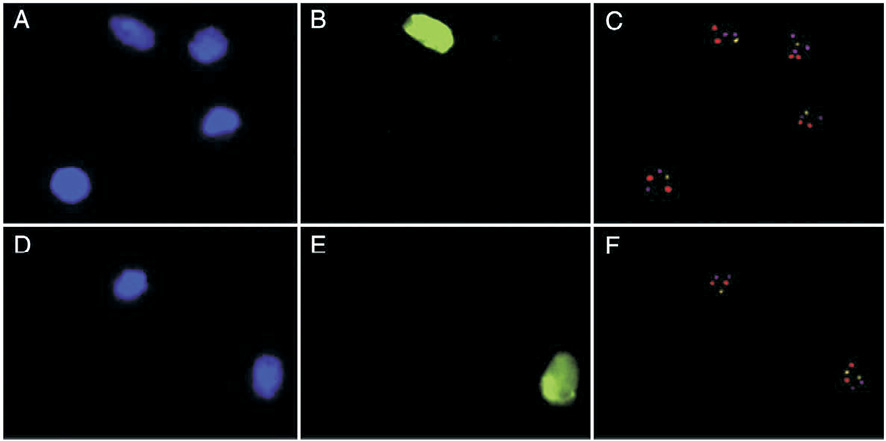
Рис. 2. Многоцветовая иммуно-FISH (иммунофенотипирование с антителами на нейрон-специфичный ядерный антиген NeuN и МFISH) в клетках мозжечка при АТ. Окраска ядер проведена флюоресцентным красителем DAPI (ядра голубого цвета – А, D, слева), NeuN иммунофенотипирование ядер (ядра зеленого цвета – В, Е в центре) и трехцветовая FISH с центромерными ДНК-зондами на хромосому 1 (сиреневые сигналы), на 18 (красные сигналы) и Х (желтые сигналы) (C, F, справа). (Из работы [21], опубликованной в журнале «Neurobiology of Disease» c разрешением издательства ACADEMIC PRESS. Neurobiology of Disease by ACADEMIC PRESS. Reproduced with permission of ACADEMIC PRESS in the format reuse in a journal/magazine via Copyright Clearance Center)
Методами молекулярной цитогенетики нами было показано, что в клетках головного мозга при АТ выявляются специфические маркеры геномной и хромосомной нестабильности, связанные с нарушением процессов репарации ДНК, сегрегации хромосом и, по-видимому, процесса запрограммированной клеточной гибели (апоптоза). Однако аномальный анеуплоидный хромосомный набор и дополнительные хромосомы с разрывами, производные хромосом 7, 14 и Х, наблюдались в 5–45 % клеток разных индивидуумов с АТ только в мозжечке. Имунно-FISH с антителами на нейрон-специфичный ядерный антиген NeuN был использован для иммунофенотипирования популяции клеток в аутопсийных образцах мозга больных АТ [21, 22]. Большинство клеток (около 80 %) с хромосомными разрывами и анеуплоидией были NeuN-негативными (рис. 3). Тем не менее, применение NeuN четко показывает, что анеуплоидия затрагивает и зрелые нейроны с аномалиями генома (до 20 % клеток с анеуплоидией и хромосомными разрывами) и глиальные клетки. Таким образом, значительное увеличение числа клеток мозжечка с анеуплоидией и хромосомными разрывами затрагивает нейроны и глию и является значимым генетическим признаком мозжечковой атаксии при АТ.
Рекуррентные точки разрыва интерфазных хромосом нервных клеток, связанные с мозжечковой нейродегенерацией при АТ, были картированы нами в участках 7p14, 14q12, Xp22.1, Xp22.3 [22]. С помощью биоинформатических технологий (анализа геномных и эпигенетических баз данных) было показано, что в участке 14q12 расположены гены-кандидаты, которые, возможно, являются мишенями CIN при АТ – FOXG1B и NOVA1. Другие точки разрыва не содержат специфических генов-мишеней, однако они расположены в участках ломкости хромосом – FRA7C, FRAXB и FRAXC (рис. 4). Следовательно, ген АТ (ATM) может регулировать стабильность сайтов ломкости. Однако для выяснения роли этих генов-кандидатов, участвующих в процессах нейрональной дисфункции и гибели в мозжечке больных АТ, необходимы дальнейшие нейробиологические и генетические исследования, которые помогут определить молекулярно-генетические механизмы мозжечковой дегенерации. Таким образом, анеуплоидия и хромосомные разрывы в дегенерирующем мозжечке затрагивают специфические хромосомы (7, 14 и Х) и, по-видимому, специфические генные локусы этих хромосом, роль которых в нейродегенеративных процессах неясна [22, 24–26].
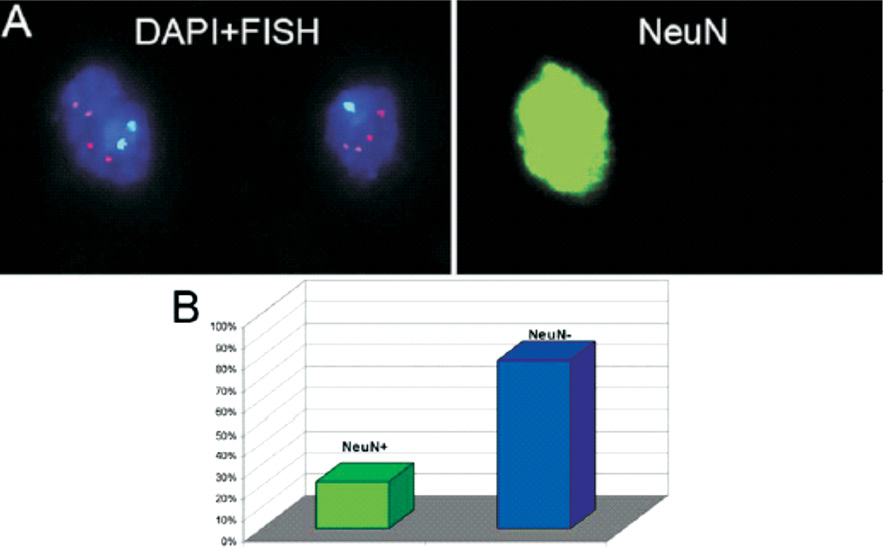
Рис. 3. Многоцветовая иммуно-FISH (NeuN иммунофенотипирование + многоцветная FISH) в клетках мозжечка при АТ (А, слева). Совместная трехцветная FISH с центромерными ДНК пробами на хромосому 1 (голубые сигналы), на 18 (розовые сигналы), и Х (красные сигналы) и окраска с DAPI, демонстрирующая одно анеуплоидное ядро (справа) (моносомия по хромосоме 1). (А, справа) NeuN иммунофенотипирование каждого ядра показывает одно NeuN- позитивное ядро нейрона (зеленый цвет, слева) с двумя хромосомами 1 и одно NeuN-негативное анеуплоидное нейронное с моносомией 1. (В) Частота NeuN-позитивных и NeuN-негативных схожих нейронов с хромосомным дисбалансом в мозжечке больных АТ. Было предположено, что генетически нестабильные NeuN-негативные нейрональные клетки могут представлять собой незрелые гранулярные нейроны –основной тип нейронов в мозжечке, а также нейрональные предшественники клеток Пуркинье, которые также являются NeuN-негативными. Кроме того, есть высокая вероятность, что они могут представлять собой также глиальные клетки, включая микроглию, которая является единственным иммунокомпетентным компартментом в ЦНС. (From [22], reproduced with permission of Springer Science + Business Media in the format reuse in a book/textbook via Copyright Clearance Center)
Хромосомоспецифические разрывы и анеуплоидия, по-видимому, представляют собой ранее неизвестную парадоксальную особенность нестабильности генома в мозге при АТ (новый парадокс 2), которая могла бы быть объяснена процессами соматической рекомбинации в нервных клетках головного мозга. Однако наличие соматической рекомбинации генома в клетках ЦНС до сих пор не доказано. Ответ на вопрос о роли специфических повреждений хромосом 14, 7 и Х при мозжечковой дегенерации требует разработки новых технологических решений, которые позволят исследовать геномные вариации в индивидуальных клетках генетически и функционально гетерогенных и мозаичных клеточных популяций головного мозга человека [25, 27].
Интересно, что при анализе спектра и частоты хромосомных аберраций у пациентов разного возраста нами обнаружена положительная корреляция частоты нервных клеток с CIN и увеличением продолжительности жизни больных АТ [22]. Эти данные не согласуются с общепринятым мнением о патогенной роли хромосомной нестабильности, так как увеличение числа аномальных анеуплоидных клеток, напротив, должно приводить к их дисфункции и ускоренной гибели, а также к тяжести клинических проявлений заболевания [13, 16, 42]. Тем не менее, у больных, доживших до старшего возраста (35–47 лет), частота CIN для хромосом 14 и 7 увеличена во много раз (от 5 до 40 %) по сравнению с более молодыми пациентами, которые умерли в возрасте 19–24 лет от осложнений при АТ (рис. 5).
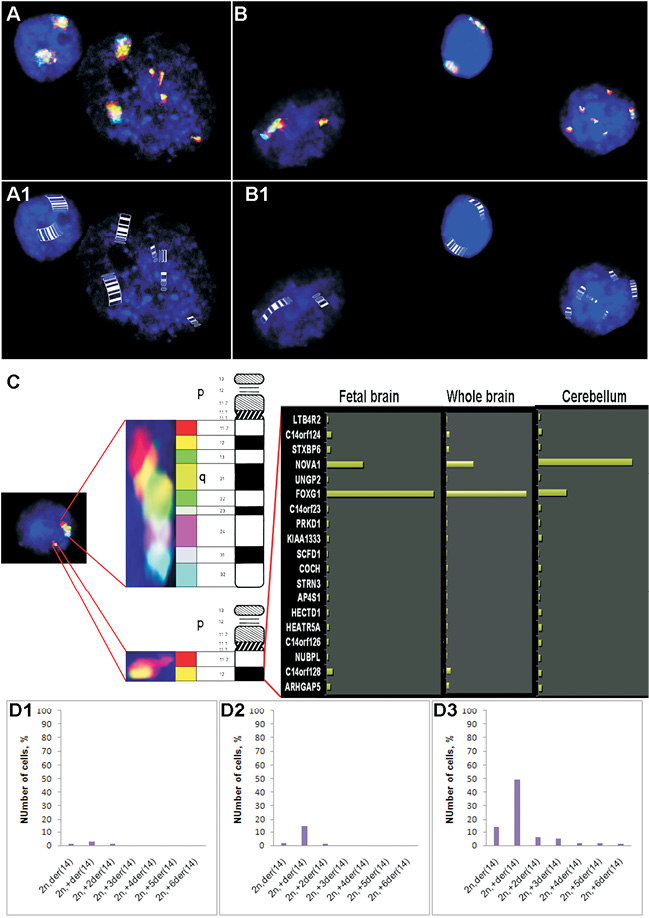
Рис. 4. Молекулярный цитогенетический анализ CIN с помощью MCB FISH. (A) Ядро нейрона (слева) с двумя неповрежденными хромосомами 14 (или дисомия 14) и другое ядро с двумя неповрежденными хромосомами 14 и четырьмя добавочными с дополнительными мини-хромосомами 14q12 (справа). (A1) схема иллюстрирует идеограммы неповрежденных и поврежденных хромосом 14 с G-полосами в том же ядре, как и в (A). (B) Ядро нейрона (слева) с одной неповрежденной хромосомой 14 и одной поврежденной дополнительной хромосомой 14 (der14q12); ядро глиальной клетки с дисомией 14 (в центре) и ядро нейрона с одной неповрежденной хромосомой 14 и пятью поврежденными дополнительными хромосомами 14 (14q12) (справа). (A1) схема иллюстрирует идеограммы неповрежденных и поврежденных хромосом 14 с G-полосы в тех же ядрах как в (B1).(C) Левая часть – ядро нейрона с одной неповрежденной хромосомой 14 и одной поврежденной (der14q12). В центре – увеличенное изображение неповрежденной хромосомы 14 и одной дополнительной хромосомы der14q12 со схемой маркировки MCB и G-окрашивания. Хромосома der14q12 содержит два участка: q11.2 (красный цвет) и q12 (желтый цвет). Большинство хромосом с разрывами (der14) в пораженном мозжечке возникли в результате разрывов двунитевой ДНК в участке14q12 с потерей дистальной части хромосомы 14. Правая часть – показаны уровни экспрессии 19-ти известных генов, локализованных в участке 14q12, в эмбриональном мозге человека, в коре взрослого мозга и в мозжечке. Только два из генов хромосомы 14 (участок q12) экспрессируются в мозжечке – NOVA1 и FOXG1B . (D1), (D2), (D3) – частота анеуплоидии с участием неповрежденной и поврежденной хромосомы 14 в нейронах мозжечка у пациентов с АТ. (D1) – пациент UMB # 1038, возраст – 24 года; (D2) – пациент UMB № 1004, возраст – 35 лет; (D3) – пациент UMB № 878, возраст – 47 лет. (From [22], reproduced with permission of Springer Science + Business Media in the format reuse in a book/textbook via Copyright Clearance Center)
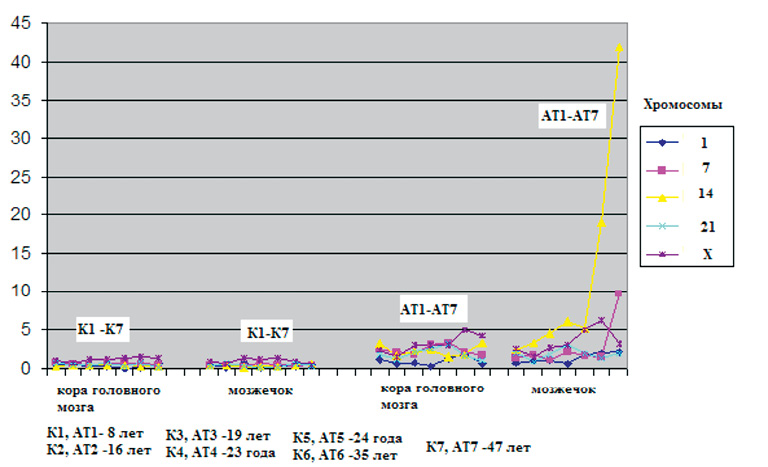
Рис. 5. Зависимость частоты анеуплоидии по хромосомам 1, 7, 14, 21, Х от возраста в диапазоне от 7 до 47 лет в группах 7 здоровых индивидуумов (К1-7) и 7 индивидуумов с АТ (АТ1-7). По оси Х – частота анеуплоидии (% %), по оси У − исследуемые аутопсийные образцы тканей головного мозга разных индивидов, ранжированные по возрасту (7, 16, 19, 23, 24, 35 и 47 лет). Видно резкое возрастание числа клеток с CIN, затрагивающих хромосомы 14 и 7 в мозжечке у больных старшего возраста
В целом наблюдается парадоксальная ситуация (парадокс 3), заключающаяся в том, что в мозжечке больных АТ в ходе онтогенеза наблюдается возрастание числа клеток с хромосомными нарушениями. Неясно, происходит ли при АТ, как это предполагалось разными авторами, преимущественная гибель клеток с генетическими нарушениями [13, 16]. Также неясно, связано ли увеличение числа анеуплоидных нейронов с тем, что нейродегенерация затрагивает нейроны с нормальным хромосомным набором, а аномальные нейроны, наоборот, не подвержены этому процессу. Экспериментального объяснения этому парадоксу пока нет. Для теоретического объяснения этого странного феномена мы выдвинули гипотезу о том, что возрастное увеличение СIN может быть связано с нейрогенезом или глиогенезом в мозжечке больных АТ. Известно, что в норме нейрогенез в мозжечке у взрослого человека не происходит. Однако теоретически можно предположить, что прогрессирующая нейродегенерация может стимулировать нейрогенез в пораженном мозжечке при АТ. Мы не можем полностью исключить предположение о том, что «взрослый» нейрогенез в мозжечке возможен при АТ. Необходимо также отметить в этой связи, что «взрослый» нейрогенез в мозжечке обнаружен у животных (кролики), используемых в качестве модельных объектов в нейронауках [35]. Таким образом, парадоксально увеличенная продолжительность жизни у некоторых больных АТ с повышенным содержанием клеток с CIN в мозжечке, по-видимому, может быть связана с нейропротективным эффектом «взрослого» нейрогенеза. С другой стороны, также возможно, что образование нейрональных и глиальных клеток с хромосомными разрывами и анеуплоидией происходит исключительно во время раннего развития мозга, когда образуется подавляющее большинство нервных клеток головного мозга человека [32]. Эти аберрантные клетки, по-видимому, устойчивы к апоптозу на всем протяжении онтогенеза, поэтому присутствуют в мозге как у здоровых людей, составляя до 10 % всех нервных клеток [38], так и до 20–50 % клеток у больных АТ [21–22]. Итак, сохранение и «накопление» нейронов с хромосомными разрывами в ходе онтогенеза компенсирует потерю клеток и, следовательно, могут защищать мозжечок от прогрессирующей гибели нейронов, что замедляет нейродегенеративные процессы, характерные для АТ.
Полученные новые данные о нестабильности генома в мозге свидетельствуют о том, что селективная мозаичная экспрессия CIN в мозжечке может являться основной причиной нейродегенерации при АТ, что и предполагает объяснение парадокса МакКиннона [28]. Применение комплекса молекулярно-цитогенетических и биоинформатических технологий позволяет проводить мониторинг геномной нестабильности и картирование генов-мишеней в нервных клетках головного мозга. Таким образом, АТ может рассматриваться в качестве адекватной генетической модели для выявления роли нестабильности генома в патогенезе нервных и нейродегенеративных заболеваний. Молекулярно-цитогенетическое исследование мозга при АТ демонстрирует то, что нарушения в поддержании целостности соматического генома из-за мутаций в гене ATM могут значительно способствовать мозжечковой нейродегенерации. Используя уникальную коллекцию аутопсийных образцов головного мозга больных АТ, мы показали, что первичный дефект в гене (мутация гена АТМ) способствует вторичному генетическому эффекту в виде хромосомной или геномной нестабильности (анеуплоидия, хромосомные разрывы). Таким образом, АТ имеет «двойственную» генетическую природу, проявляя одновременно признаки моногенного и хромосомного заболевания ЦНС.
Проведенный нами анализ собственных и литературных данных выявил новые парадоксальные особенности нейродегенеративных процессов в мозге при АТ, которые прямо или опосредованно могут быть связаны с нестабильностью соматического генома нервных клеток. Во-первых, выявлен новый феномен глобальной анеуплоидизации мозга при АТ, которая, присутствуя в 20–50 % нервных клеток префронтальной коры и мозжечка, не затрагивает основные когнитивные и психические функции мозга. Во-вторых, CIN (анеуплоидия и хромосомные разрывы) в дегенерирующем мозжечке затрагивает специфические хромосомы (7, 14 и Х), и, по-видимому, специфические гены этих хромосом, роль которых в нейродегенеративных процессах пока неясна. В-третьих, резкое возрастание патологического уровня CIN в мозге больных не приводит к ускоренной нейродегенерации, а, напротив, коррелирует с увеличением продолжительности жизни пациентов. Для объяснения и экспериментальной проверки этих парадоксальных находок высказаны следующие гипотетические объяснения, которые частично поддерживаются немногочисленными пока экспериментальными данными. Нейродегенеративные изменения могут теоретически (1) стимулировать «взрослый» нейрогенез в мозжечке [35]; (2) увеличивать миграцию недифференцированных стволовых клеток крови в пораженные отделы головного мозга [30], а также (3) вызывать активацию микроглии – фагоцитарной системы головного мозга, которая играет роль иммунной системы в ЦНС и способна к пролиферации в ходе онтогенеза [11]. Таким образом, увеличение числа глиальных и нейрональных клеток с CIN в мозжечке при АТ является отражением эндогенных нейропротективных процессов, а CIN является биологическим маркером эффективной нейропротекции. Экспериментальная проверка этих предположений представляется актуальной научной задачей, решение которой позволит определить генетические механизмы патогенеза нейродегенеративных болезней. В перспективе, исследования с привлечением геномных и клеточных технологий могут помочь в разработке научно обоснованных методов коррекции этой в настоящее время неизлечимой болезни.
АТ является уникальной моделью для изучения механизмов нейродегенерации и преждевременного старения, связанных с геномной и хромосомной нестабильностью. Разработка новых молекулярно-цитогенетических методов анализа вариаций генома на клеточном уровне с молекулярным разрешением позволяет эффективно выявлять нервные клетки с геномными и хромосомными нарушениями в мозге [36, 37]. Эти исследования в новой области биомедицины – нейрогеномики или молекулярной нейроцитогенетики − открывают перспективы для выяснения роли соматических вариаций генома нервной клетки в норме и при нервно-психических заболеваниях [20]. Необходимо отметить, что увеличение уровня мозаичной анеуплоидии в мозге выявлено не только при АТ, но и при таких генетически гетерогенных и многофакторных болезнях мозга, как аутизм и шизофрения [39, 41]. При этих заболеваниях патогенез, по-видимому, связан с геномной нестабильностью и нарушением регуляции числа анеуплоидных клеток в ходе раннего нейрогенеза [38, 40]. При нейродегенеративных заболеваниях, характеризующихся преждевременным или патологическим старением (например, АТ и болезнь Альцгеймера), наблюдается значительное увеличение числа нервных клеток с анеуплоидией и хромосомными перестройками в отделах мозга, пораженных нейродегенерацией [21–23]. Предполагается, что при нейродегенеративных заболеваниях этот феномен связан с нарушением процессов «взрослого» нейрогенеза или глиогенеза. Уровень геномной нестабильности на более поздних стадиях онтогенеза и при старении мозга как в норме, так и при патологии может варьироваться. Увеличение числа аномальных клеток с анеуплоидией, по-видимому, является одним из вероятных механизмов старения мозга [42]. В этой связи нами ранее была предложена теория, рассматривающая нестабильность соматического генома в качестве главного генетического механизма, лежащего в основе патогенеза нервных и психических заболеваний, а также старения мозга. Эта теория, основные положения которой изложены в серии наших публикаций, предполагает, что соматические геномные изменения в ходе онтогенеза являются значимыми детерминантами клеточной жизнеспособности в норме и при патологии, включая внутриутробное развитие, постнатальный период и старение [1, 4, 6–8, 16–20, 24, 25, 43]. Явление нестабильности соматического генома нервной клетки позволяет объединить и объяснить комплекс разрозненных гипотез о роли генетических факторов в этиологии и патогенезе заболеваний ЦНС, а также логически объяснить парадоксальные феномены, ассоциированные с психическими и нейродегенеративными заболеваниями. Данный обзор собственных и литературных данных, полученных при изучении АТ, подчеркивает исключительно важную роль геномных и хромосомных вариаций в ходе онтогенеза в норме и при генетически обусловленных заболеваниях мозга.
Работа выполнена в рамках плановых научных исследований НЦПЗ РАМН и частично поддержана грантом РФФИ № 12-04-00215-а.
Работа поступила в редакцию 28.12.2012.



