Множество экспериментальных данных, полученных как на клеточном уровне, так и на уровне организма, указывают на то, что фазовый переход биологической мембраны из жидкого в твердое состояние играет важную роль в механизме возбудимости нервной ткани [7–10]. Была высказана гипотеза о том, что в быстрых синапсах необходимым этапом в осуществлении синаптического экзоцитоза является Са2+-индуцированный переход мембраны из жидкого в твердое состояние – гипотеза фазово-переходного механизма [9, 10]. В активных зонах пресинапса существуют как минимум два класса мишеней, с которыми связывается Са2+ – «мишень I» и «мишень II», различающиеся по характеру функционального действия и по сродству к Са2+ [2, 12]. В состоянии покоя внутриклеточная концентрация Са2+ составляет около 0,1 мкМ [1]. При деполяризации она повышается до величин, соответствующих константам диссоциации сначала мишени I, затем мишени II. Мишень I с высоким сродством к кальцию – это центры связывания кальция на белках SNARE-комплекса, удерживающего везикулы на цитоплазматической мембране. Сродство этих центров к Са2+ соответствует константам диссоциации в диапазоне 1–10 мкМ [5, 6]. С точки зрения фазово-переходного механизма функциональное значение связывания Са2+ состоит в том, чтобы в точке контакта везикулы с цитоплазматической мембраной сформировалось механически слабое место, готовое порваться в ответ на механическое натяжение мембраны [9, 10]. Мишень II, представленная в синапсе, по-видимому, анионными липидами [6, 9], обладает на один-два порядка более низким сродством – это следует из того факта, что для инициации быстрого экзоцитоза в большинстве синапсов требуется локальная внутриклеточная концентрация Са2+ превышающая 100 мкМ [1, 6, 11, 13]. Функциональная роль связывания Са2+ с мишенью II состоит в инициации перехода мембраны в твердое состояние [9, 10]. Площадь поверхности мембраны при отвердевании сокращается, мембрана механически напрягается и рвется в слабом месте, подготовленном мишенью I; это и приводит к слиянию мембран и высвобождению нейромедиатора. Как показано ранее [4], энергия напряженного состояния и скорость фазового перехода достаточно велики для того, чтобы переход и экзоцитоз могли осуществиться за необходимое короткое время (< 0,1 мс). Однако до настоящего времени не было получено прямых доказательств фазово-переходного механизма.
Если действительно функция мишени II (экзоцитоз) осуществляется благодаря Са2+-индуцированному отвердеванию мембраны, то эту функцию можно было бы инициировать быстрым охлаждением системы без участия Са2+. Однако в такой простой постановке опыта осталась бы невыполненной важная подготовительная функция первой мишени – формирование механически слабого места под везикулой. И тогда вероятность экзоцитоза была бы крайне низка, так как вызванные отвердеванием разрывы мембраны происходили бы хаотично в любом месте. Следовательно, должны быть созданы такие условия, при которых кальций мог бы достичь уровня, достаточного для связывания с мишенью I, но не с мишенью II. Тогда слабое место под везикулой было бы подготовлено, и на этом фоне основное действие – отвердевание мембраны и акт экзоцитоза – можно было бы инициировать снижением температуры.
Цель данной работы − проверить, может ли быстрое охлаждение системы инициировать экзоцитоз без участия Са2+ при условии «подготовленного» состояния синапса. Для создания такого состояния синапса в НМП лягушки мы использовали высокочастотную (100 Гц) стимуляцию нерва в условиях инкубации препарата в растворе с пониженной концентрацией кальция.
Материалы и методы исследования
Объектом исследования был выбран классический НМП икроножной мышцы лягушки Rana temporaria. Эксперименты проводили в августе, животные (n = 7) отлавливались в естественной среде обитания за один-три дня до опыта и содержались без подкормки во влажных условиях при температуре 17–18 °C. В экспериментах использовали стандартный физиологический раствор Рингера для холоднокровных (RСа) следующего состава (мМ): NaCl – 110, KCl – 1,8, CaCl2 – 0,90, NaHCO3 – 2,0; рН = 7,2. При приготовлении номинально бескальциевого раствора (RMg) CaCl2 заменялся на молярно эквивалентное количество MgCl2 (примесное содержание кальция в этом растворе не превышало 0,050 мМ по данным атомно-абсорбционной спектрометрии). Электрическая стимуляция нерва производилась серией прямоугольных импульсов (длительность 0,1 мс, частота 100 Гц). Для измерения силы сокращения мышцы был сконструирован датчик, основанный на изгибной деформации упругого стержня, измеряемой фотометрически; диапазон измеряемых сил от 0 до 500 мН, чувствительность 1 мН.
Эксперименты (n = 21) проводили по следующей схеме. Мышца помещалась в RСа при комнатной температуре (около 20 °C). Затем стандартный раствор заменялся на RMg, при этом мышца подвергалась «массажу» стеклянной палочкой для ускорения обмена солей между мышцей и раствором. В растворе RMg сила сокращения мышцы постепенно уменьшалась до полного исчезновения ответа. Исчезновение ответа рассматривалось как указание на то, что уровень Са2+ в системе уже недостаточен для связывания с мишенью II. После этого экспериментальную камеру освобождали от РMg комнатной температуры, включали стимуляция нерва, и на ее фоне камеру заполняли ледяным РMg (0–3 °C). Температура раствора в камере сразу после заполнения поднималась до 10–13 °C из-за теплообмена со стенками. Смена раствора занимала менее 3 секунд. Предполагалось, что если экзоцитозная функция мишени II в синапсах действительно выполняется благодаря отвердеванию мембраны, то при понижении температуры раствора в мышце должна возникнуть серия сокращений, отражающих достижение холодовым фронтом синаптических окончаний внутри мышцы.
Для проверки, на какой элемент НМП действует охлаждение, проводились также контрольные эксперименты, описанные ниже.
Результаты исследования и их обсуждение
Мышечный ответ в стандартном растворе RСа значительно превышал 500 мН, будучи за пределами рабочего диапазона датчика силы. Полная потеря ответа мышцы на длительную стимуляцию нерва (длительностью 11–12 с) наступала через 60–120 мин после смены RСа на RMg. Отметим две важные особенности этого «декальцинированного» состояния. Во-первых, оно обратимо: при замене RMg на RСа ответ мышцы на раздражение нерва немедленно начинал восстанавливаться. Во-вторых, мышца сохраняла способность отвечать сокращением на непосредственную электрическую стимуляцию самой мышцы (сила ответа превышала 500 мН). Это значит, что декальцинирование блокирует синаптическую передачу, не нарушая сократительный аппарат мышцы.
После декальцинирования включали стимуляцию нерва и на ее фоне раствор RMg комнатной температуры заменяли на ледяной раствор. Было обнаружено, что с началом охлаждения мышцы в ней возникает серия спонтанных сокращений, длящаяся не менее 5 с (рисунок). При этом сила сокращения в пике составляла 10–20 мН. Эти результаты подтверждают предположение о том, что понижение температуры инкубационного раствора приводит к отвердеванию липидного бислоя мембраны и реализации экзоцитозной функции мишени II в синапсах.
В серии контрольных опытов, направленных на проверку, является ли охлаждение фактором, возбуждающим нервно-мышечное соединение, было показано, что:
1. В случае, когда мышца не декальцинирована и в ней развивается обычный тетанический ответ на электрическую стимуляцию, то охлаждение ледяным физиологическим раствором приводит к значительному падению силы ее сокращения (примерно в 1,5 раза). Следовательно, развитие силы в нашем основном опыте не вызвано действием на собственно сократительный аппарат мышцы.
2. Спонтанные сокращения мышцы не возникают, если замена теплого RMg на холодный проводится без включения фоновой высокочастотной стимуляции нерва (рисунок, тонкие линии). Следовательно, во-первых, еще раз подтверждается предыдущий вывод о том, что сокращение мышцы не является реакцией сократительного аппарата на холод, но связан с процессами в синаптическом контакте. Во-вторых, повышение внутриклеточной концентрации Са2+ (с помощью фоновой стимуляции) является обязательным условием для инициации экзоцитоза путем резкого охлаждения – как и предполагалось при планировании эксперимента.
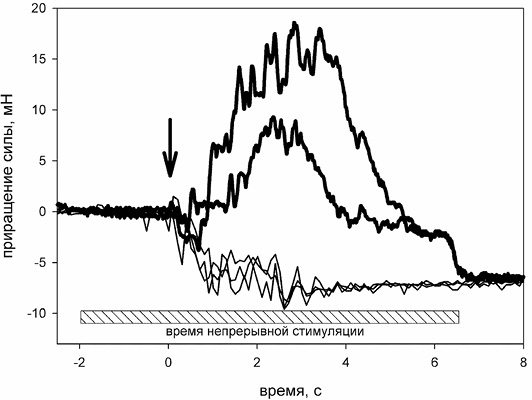
Жирными линиями показаны типичные кривые развития силы мышечного сокращения, инициированного вливанием ледяного физиологического раствора (стрелкой обозначено начало вливания) в камеру с мышцей на фоне непрерывной высокочастотной стимуляции нерва (продолжительность стимуляции показана горизонтальной штрихованной планкой внизу рисунка). Тонкими линиями показаны контрольные опыты, полученные в тех же условиях, но без стимуляции нерва. Систематическое снижение силы при заливке – результат действия архимедовой выталкивающей силы. Приращение силы на оси ординат – разность между текущей силой и начальной; начальное натяжение мышцы всегда устанавливалось в диапазоне 40–50 мН
3. Сокращение мышцы не происходит, если электрическая стимуляция нерва начинается после замены теплого RMg на холодный. Следовательно, снижение температуры не приводит к повышению сродства мишени II к ионам кальция и, значит, возбуждение холодом в нашем основном опыте вызвано процессом отвердевания синаптической мембраны в момент ее охлаждения.
Заключение
Из совокупности результатов следуют два основных вывода.
1. Обнаружено неизвестное ранее явление, заключающееся в том, что быстрое охлаждение биологической ткани может служить неспецифическим фактором возбуждения наряду с известными электрическими, химическими и механическими факторами. В исследованном нами объекте возбуждение возникает на уровне нервно-мышечного соединения, а не на уровне сократительного аппарата мышцы (иначе мышца и без стимуляции нерва сократилась бы под действием холода).
2. Способность нервно-мышечного препарата возбуждаться под действием снижения температуры является следствием фазово-переходного механизма синаптического экзоцитоза, и это следствие получило здесь экспериментальное подтверждение. Можно считать, что в работе представлено убедительное, хотя и непрямое подтверждение гипотезы о фазово-переходном механизме экзоцитоза.
Значение этого факта выходит за пределы узко поставленной задачи о молекулярных механизмах синаптической передачи, поскольку гипотеза о фазово-переходном механизме продемонстрировала свою перспективность в исследовании нерешенных проблем в разных областях физиологии и медицины, включая сомнологию, физиологию терморегуляции, анестезиологию, эволюцию теплокровности и другие [3, 8, 9, 10].
Мы благодарим И.Ю. Сергеева, С.М. Ляпкова и Г.С. Сурову за ценные консультации, В.Ю. Архипова, И.П. Амзаракову и К.Г. Тихонова за техническую помощь, а также выражаем признательность руководству Звенигородской биостанции МГУ за содействие в проведении работы на ее территории.
Рецензенты:
Кичигина В.Ф., д.б.н., зав. лабораторией системной организации нейронов ИТЭБ РАН ФГБУН «Институт теоретической и экспериментальной биофизики Российской академии наук», г. Пущино;
Орлов Н.Я., д.б.н., зав. лабораторией функциональной биофизики белка ИТЭБ РАН ФГБУН «Институт теоретической и экспериментальной биофизики Российской академии наук», г. Пущино.
Работа поступила в редакцию 28.12.2012.



