Проблема создания биологически активных волокнистых материалов в последние десятилетия вызывает все возрастающий интерес. Широкое развитие исследований по приданию биоцидных свойств именно целлюлозным волокнистым материалам обусловлено тем, что целлюлоза является доступным и распространенным в природе полимерным материалом. Исследования, посвященные синтезу производных целлюлозы, содержащих антимикробные вещества, разработке научных основ получения биоцидных целлюлозных волокнистых материалов с заданными свойствами, методов и технологии их изготовления, а также изучению свойств и наиболее эффективных областей применения указанных материалов имеют большое научное и практическое значение.
В настоящее время описано большое число биоцидных производных целлюлозы и других волокнообразующих полимеров разного строения [2].
Возможность синтеза производных целлюлозы, обладающих антимикробными свойствами путем присоединения антимикробного препарата альдиминовой связью С = N была показана в ряде работ, где к модифицированной целлюлозе, содержащей альдегидные группы, присоединяли антимикробные вещества, в молекулах которых имелись ароматические или алифатические аминогруппы [11, 12].
Основной целью получения указанных выше соединений является получение азотсодержащих производных целлюлозы, обладающих биологической активностью. Однако проявление биологически активных свойств данных соединений затруднено, так как они нерастворимы в воде и органических растворителях.
Задачей настоящего исследования являлось расширение ряда производных целлюлозы, обладающих биологической активностью, а также получение водорастворимых биологически активных производных целлюлозы, для которых действие модифицирующих целлюлозу биологически активных соединений будет иметь более ярко выраженный характер.
Для решения этой задачи в качестве объектов исследования были выбраны диальдегидцеллюлоза (микрокристаллическая целлюлоза, окисленная периодатом натрия), ДАГА, ДАГТФА.
Материалы и методы исследования
Характеристика объектов исследования:
1) МКЦ – целлюлоза хлопковая микрокристаллическая марки «хч», содержание карбонильных групп ≈ 0,65 %, степень полимеризации (СП, n ≈ 150);
2) ДАЦ – диальдегидцеллюлоза хлопковая (МКЦ окисленная периодатом натрия) [8];
3) ДАГА и ДАГТФА, полученные по методике, приведенной в работе [10];
4) инициатор радикальной полимеризации ПСА – персульфат аммония (NH4)2S2O8 марки «ч.д.а.» (перекристаллизован из бидистиллированной воды, высушен в вакууме до постоянной массы). Все использованные реактивы по своим характеристикам соответствовали литературным данным. Количество СНО-групп в МКЦ и ДАЦ определяли по методу Соболкса [9] и титриметрически по методике [5]. ИК-спектры образцов сняты на ИК-спектрофотометре SPECORD M82 в области от 4000 до 400 см–1. Образцы для ИК-спектроскопии готовили в виде таблеток с КBr или суспензии в вазелиновом масле.
Рентгенодифракционные данные получены при комнатной температуре на автоматизированном дифрактометре ДРОН-6 (36 кВ, 20 мА, λСuКα, графитовый монохроматор на вторичном пучке, съемка по Бреггу-Брентано в интервале углов 2θ от 5 до 75°, шаг 0,05°, скорость сканирования 1 град/мин).
Методика получения композиционных материалов
Композиционные материалы получали обработкой ДАЦ мономерными солями – ДАГА и ДАГТФА с последующей их полимеризацией.
К водной суспензии ДАЦ с содержанием альдегидных групп до 33 % (максимальное содержание альдегидных групп в элементарном звене 36 %) при перемешивании добавляют водный раствор ДАГА или ДАГТФА и ПСА, нагревают смесь до 60 °С и проводят полимеризацию в течение 5–20 часов. Соотношение ДАЦ:Н2О = 1:30 масс, концентрация ДАГА (ДАГТФА) в воде – 1,0–3,5 %, соотношение ДАГА (ДАГТФА):ПСА = 1:0,001 мас. Полученный продукт отделяют от маточного раствора и сушат.
Результаты исследования и их обсуждение
Формирование и исследование систем «полимерный носитель – биологически активное вещество» в последнее время приобрели большое значение. Такие системы находят применение в качестве иммобилизованных биокатализаторов, биорегуляторов и активной формы лекарственных веществ пролонгированного действия.
Применение соединений с собственной бактерицидной активностью позволяет решить данную проблему, а именно: значительно увеличить пролонгированность действия, обеспечить заданную кинетику выделения антимикробного вещества путем регулирования химического состава, предложить удобную для использования форму.
Исследования бактерицидной активности синтезированных гомо- и сополимеров на основе ДАГА и ДАГТФА, проведенные лабораторией полиэлектролитов ИНХС РАН совместно с Институтом микробиологии и эпидемиологии им. Н.Ф. Гамалеи РАМН, бактериологической лабораторией Государственного санитарно-эпидемиологического надзора Кабардино-Балкарской республики (КБР) и с фармацевтическим объединением «Эльфарми» (КБР, г. Нальчик), показали, что эти препараты весьма активны и обладают биоцидным действием по отношению к грамположительным (St.Aureus) и грамотрицательным (E.coli) микроорганизмам [6, 13].
Все вышесказанное свидетельствует о перспективности и принципиальной возможности использования в качестве биоцидных препаратов синтезированных нами новых гуанидинсодержащих мономеров ДАГА и ДАГТФА, структура которых приведена на схеме.
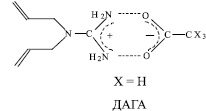
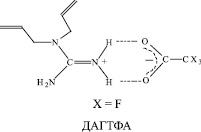
При модифицировании диальдегидцеллюлозы ДАГА и ДАГТФА наблюдаются незначительные изменения в ИК спектрах, что свидетельствует о «мягком» модифицировании без разрушения внутримолекулярных связей целлюлозы (рис. 1–3). Введение в структуру целлюлозы диаллильных производных гуанидина не приводит к появлению в ИК-спектрах новых пиков ввиду совпадения характеристических частот групп, входящих в состав модификаторов и матрицы.
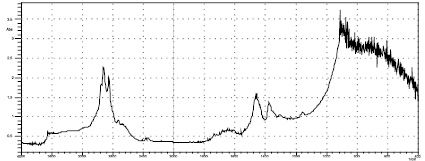
Рис. 1. ИК-спектр ДАЦ
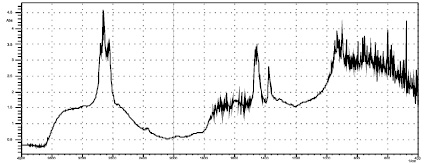
Рис. 2. ИК-спектр ДАЦ, модифицированной ДАГА
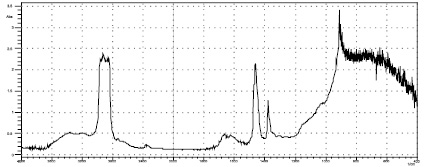
Рис. 3. ИК-спектр ДАЦ, модифицированной ДАГТФА
Широкая полоса поглощения 3700–3100 см–1 связана с валентными колебаниями гидроксильных групп, вовлеченных в водородные связи. Известно, что низкочастотная область полосы νон характеризует гидроксилы, включенные в более сильные водородные связи (внутримолекулярные), а высокочастотная – в более слабые (межмолекулярные) [7].
В спектрах модифицированной ДАЦ наблюдается увеличение поглощения νон со стороны высоких частот, особенно в спектре ДАЦ, модифицированной ДАГА. Согласно литературным данным [3] это связано с увеличением доли гидроксилов, вовлеченных в слабые водородные связи. Валентные колебания С-Н связей метиленовых и метановых групп ДАЦ проявляются в области 3000–2800 см–1 [1]. В спектрах модифицированных ДАГА и ДАГТФА диальдегидцкеллюлозы эти валентные колебания накладываются на поглощение групп СН2, входящих в состав диаллильных соединений. Это приводит к увеличению интенсивности полос поглощения частотой ~ 2900 см1, так как при модифицировании происходит привитие на поверхность образцов целлюлозы производных, содержащих дополнительные группы СН2.
В области ~1650 см–1 проявляются пики адсорбированной воды. При увеличении содержания воды максимум полосы поглощения несколько смещается в сторону больших волновых чисел [4]. Привитие полярных аминогрупп, входящих в состав модификаторов, увеличивает полярность подложки, что способствует удержанию у поверхности модифицированных образцов целлюлозы большего количества адсорбционной воды за счет водородных связей. Увеличение интенсивности полосы поглощения —1630–1655 см–1 позволяет сделать предположения о наличии аминогрупп -NH2 и -NH в составе модифицированной диальдегидцеллюлозы [4]. Кроме того, увеличение интенсивности пика 1655 см–1 в спектре ДАЦ-ДАГА и ДАЦ-ДАГТФА может указывать на образование альдиминовой связи, дающей сигнал в этой области. При полимеризации ДАГА и ДАГТФА в ДАЦ in situ пик в области 1140 см–1, присутствующий в ДАЦ исчезает. Очевидно, что концевые СНО-группы ДАЦ и гуанидинсодержащих диаллильных модификаторов прореагировали между собой.
Таким образом, при иммобилизации ДАГА и ДАГТФА в ДАЦ между компонентами образуются различные типы связей: за счет ван-дер-ваальсовых сил; внутри- и межмолекулярные координационные и водородные связи; С–С связи, образующиеся при радикальной полимеризации in situ иммобилизованных ДАГА и ДАГТФА, связи, образующиеся в ходе привитой радикальной сополимеризации ДАГА и ДАГТФА с ДАЦ, а также лабильные ковалентные альдиминовые С = N связи, образующиеся при взаимодействии альдегидных групп ДАЦ с аминогруппами гуанидинсодержащих диаллильных соединений.
Полосы поглощения (полосы кристалличности) частотой ~1431 см–1 (полоса кристалличности) и ~900 см–1 (полоса аморфности) в спектре исходной ДАЦ соответствуют ножничным колебаниям метиленовой группы и колебаниям атома С1 и четырех окружающих его атомов в спектрах р-гликозидных структур. При увеличении степени кристалличности (СК) целлюлозы в результате механической или химической модификации интенсивность полосы 1431 см–1 увеличивается, а 900 см–1 – уменьшается [1], что и наблюдается в спектрах ДАЦ, модифицированных ДАГА и ДАГТФА. Такое изменение интенсивности полос поглощения указанных частот свидетельствует об увеличении СК у образцов модифицированной целлюлозы. Причем более выражено повышение СК наблюдается у образцов ДАЦ, модифицированных ДАГА.
Об увеличении СК образцов свидетельствует и дифрактограммы модифицированной ДАЦ (рис. 4).
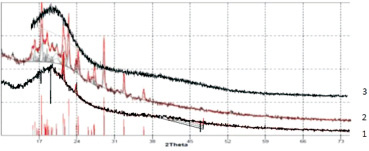
Рис. 4. Дифрактограмма; 1 – ДАЦ модифицированной ДАГТФА; 2 – ДАЦ модифицированной ДАГА; 3 – не модифицированная ДАЦ
Композиционные материалы, полученные при полимеризации ДАГА и ДАГТФА in situ в меж- и внутрифибриллярных порах ДАЦ, хорошо растворяются в воде и обладают выраженными бактерицидными свойствами. Бактериологическими исследованиями установлено, что ДАЦ/ДАГА и ДАЦ/ДАГТФА эффективны против протея вульгарного (Proteus vulgaris), синегнойной палочки (Ps. aureginosa), золотистого стафилококка (Staph. Aureus), кишечной палочки (E-coli). Разработанные материалы могут иметь широкий спектр применения. Например, могут быть использованы в медицине как антисептические средства наружного применения, как альтернативный антибиотикам лекарственный препарат, а также в качестве компонентов бактерицидных покрытий с пролонгированным действием.
Работа выполнена с использованием оборудования ЦКП «Рентгеновская диагностика материалов» КБГУ в рамках выполнения госконтракта № 16.552.11.7074.
Рецензенты:
Борукаев Т.А., д.х.н., профессор, зав. лабораторией ФГБОУ ВПО «Кабардино-Балкарский государственный университет им. Х.М. Бербекова», г. Нальчик;
Лигидов М.Х. д.х.н., профессор, декан химического факультета ФГБОУ ВПО «Кабардино-Балкарский государственный университет им. Х.М. Бербекова», г. Нальчик.
Работа поступила в редакцию 01.11.2012.



