Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE SODIUM HYPOCHLORITE INFLUENCE ON SOME LINKS OF HOMEOSTASIS IN TREATMENT OF EXPERIMENTAL BILIOUS PERITONITIS
Введение. Желчному перитониту (ЖП) как наиболее частому осложнению эндоскопических операций на органах гепатобилиарной зоны посвящено недостаточное количество публикаций [1, 6, 7]. Интерес к этой проблеме объясняется высокой летальностью, где основной причиной является нарушение гормонально-опосредованной регуляции [3, 4, 5, 8] на фоне развития эндогенной интоксикации [2, 9]. Избыточное накопление токсинов при перитоните и неспособность физиологических систем организма обеспечить их выведение, обусловливают необходимость применения специальных средств и методов лечения. В настоящее время в хирургии положительно зарекомендовал себя метод непрямого электрохимического окисления с использованием натрия гипохлорита (НГХ).
Цель исследования - повысить эффективность лечения желчного перитонита.
Материал и методы исследования
Работа выполнена на 50 беспородных собаках-самцах весом 16 ± 1,5 кг. Экспериментальные животные были разделены на две группы: в 1-ю контрольную группу для определения лабораторных показателей нормы вошли 50 собак, из которых 5 были выведены из опыта для забора биоптатов; во 2-ю группу вошли оставшихся 45 животных, у которых создавали модель 24-часового экспериментального ЖП. Суть модели заключалась в том, что предварительно на наружной поверхности заднего бедра собаки создавали очаг деструкции путем подкожного введения 10 %-ного раствора кальция хлорида из расчета 0,25 мл/кг. Через 48 часов проводили троекратное внутрибрюшинное введение аптечной желчи через каждые 8 часов из расчета 1,5 мл/кг [10]. После создания модели 24-часового ЖП из опыта были выведены еще 5 собак. Оставшиеся 40 животных с 24-часовым ЖП, в свою очередь, были разделены еще на две группы: 3-ю группу сравнения и 4-ю опытную группу, в которые были включены по 20 собак. Эксперименты проведены в соответствии со статьей XI Хельсинкской декларации Всемирной медицинской ассоциации (1964), «Международными рекомендациями по проведению медико-биологических исследований с использованием животных» (1985).
Методика лечения животных заключалась в выполнении лапаротомии, удалении воспалительного экссудата и санировании брюшной полости 400 мл раствора фурацилина (1:5000). После этого животным группы сравнения и опытной группы в брюшную полость заливали 250,0 мл 0,04 %-ного раствора НГХ и зашивали края брюшной стенки. Животным группы сравнения проводили инфузионную терапию 0,9 %-ным раствором хлорида натрия в качестве средства дезинтоксикации, а животным опытной группы - 0,04 %-ным раствором НГХ в качестве бактерицидного и детоксицирующего средства из расчета 1/10 ОЦК, сразу и через 12 часов после санации брюшной полости. Динамику развития изучали до, после создания модели 24-часового ЖП, на 1, 3, 7, 10 и 30-е сутки.
НГХ получали путём электролиза 0,9 %-ного раствора натрия хлорида в аппарате электрохимический детоксикатор организма (ЭДО-4). Определение кортизола, общего тироксина (ТТ4), свободного тироксина (СТ4), общего трийодтиронина (ТТ3) и тиреостимулирующего гормона (ТТГ) проводили иммуноферментным методом с использованием набора реактивов «Амерлайт» [5]. Результаты исследований обработаны с помощью прикладных программ «Microsoft Exel» и «Statistica 6,0» для Windows. Данные в тексте и таблицах представлены в виде среднего арифметического значения и стандартной ошибки среднего М+m, а при непараметрическом характере распределения величин - в виде медианы с указанием 25-го и 75-го квартилей [медиана (25-й - 75-й квартиль)].
Результаты исследования и их обсуждение
Для изучения динамики стрессовой реакции был исследован уровень кортизола в сыворотке крови, который у животных с 24-часовым ЖП возрастал до 244,3 ± 46,8 нмоль/л против 136,3 ± 20,2 нмоль/л (p < 0,05) у контрольных животных (рис. 1).
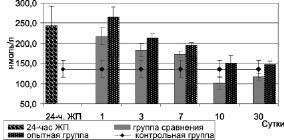
Рис. 1. Динамика уровня кортизола в крови при комплексном лечении
экспериментального желчного перитонита
В последующие сроки у животных с экспериментальным желчным перитонитом уровень кортизола, как в группе сравнения, так и в опытной группе, постепенно снижался и приходил к контрольным цифрам к 10-м суткам наблюдения (p > 0,05). Однако необходимо отметить, что уровень кортизола в опытной группе достоверно превышал данный показатель у животных в группе сравнения (p < 0,05), что можно объяснить неспецифической реакцией организма в ответ на действие промежуточных продуктов окисления белков крови натрия гипохлоритом.
Общеизвестно, что уровень ТТГ отражает состояние гипоталамо-гипофизарной системы.
У животных с 24-часовым желчным перитонитом уровень ТТГ в крови находился в пределах допустимых норм (феномен «низкого нормального ТТГ»), а у 30 % животных его не удавалось определить вообще. У животных с 24-часовым желчным перитонитом отмечалась тенденция к снижению количества ТТГ-позитивных животных относительно контрольных животных (p > 0,05). В группе сравнения относительное количество ТТГ-позитивных животных во все сроки наблюдения достоверно не отличалось от контроля (p > 0,05), в то время как в опытной группе с 3-х по 10-е сутки их относительное количество было достоверно выше уровня контрольных животных, животных с 24-часовым желчным перитонитом и животных группы сравнения (p < 0,05).
У животных с 24-часовым желчным перитонитом содержание общего тироксина в крови достоверно снижалось до 28 ± 10,0 нмоль/л против 58,9 ± 8,8 нмоль/л в контрольной группе (p < 0,05) (рис. 2).
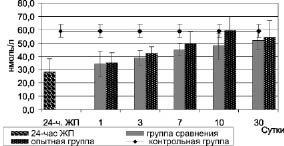
Рис. 2. Динамика уровня общего тироксина в крови при комплексном лечении
экспериментального желчного перитонита
В последующие сроки, как в группе сравнения, так и в опытной группе после начала лечения в течение первых трех суток наблюдался достоверный рост его содержания (р < 0,05). При этом в группе сравнения данный рост приходил к контрольным величинам только на 10-е сутки, в то время как в опытной группе - на 7-е сутки наблюдения (p > 0,05). Необходимо отметить, что, несмотря на важность и необходимость содержания общего тироксина в организме, физиологическим действием обладает только свободный тироксин, не связанный с белками-переносчиками.
Так, у животных с 24-часовым желчным перитонитом наблюдалось достоверное уменьшение содержания свободного тироксина в крови до 10,2 ± 1,9 нмоль/л против 19,7 ± 2,6 нмоль/л у контрольных животных (p < 0,05) (рис. 3).
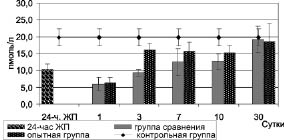
Рис. 3. Динамика уровня свободного тироксина в крови при комплексном лечении
экспериментального желчного перитонита
На 1-е сутки после начала лечения в группе сравнения и опытной группе уровень содержания свободного тироксина в крови оставался достоверно низким, как относительно контроля, так и показателей у животных с 24-часовым желчным перитонитом (р < 0,05). В последующие сроки его уровень у животных в группе сравнения вплоть до 10-х суток был достоверно ниже показателей контрольных животных, и только к 30-м суткам он приходил к контрольным данным (p > 0,05), в то время как в опытной группе данный показатель уже на 3-и сутки не отличался от контрольных величин (p > 0,05).
Общеизвестно, что большая часть общего тироксина циркулирует в крови в комплексе с белками. При этом его концентрация зависит не только от скорости выработки этого гормона, но и от изменения уровня связей с белками. Соответственно при снижении концентрации этих белков в крови происходит снижение содержания общего тироксина. Таким образом, более раннюю нормализацию уровня общего тироксина по сравнению со свободным тироксином в опытной группе можно объяснить как гипопротеинемией при развитии экспериментального желчного перитонита, так и возможным окислением свободного тироксина натрия гипохлоритом.
Исследование содержания общего трийодтиронина в крови у животных с 24-часовым желчным перитонитом показало достоверное его снижение до 1,2 ± 0,3 нмоль/л против 2,3 ± 0,2 нмоль/л (p < 0,05) у контрольных животных (рис. 4).
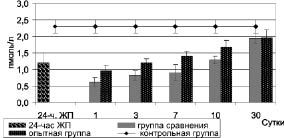
Рис. 4. Динамика общего трийодтиронина в крови при комплексном лечении
экспериментального желчного перитонита
В ходе дальнейших исследований концентрация общего трийодтиронина, как в группе сравнения, так и в опытной группе вплоть до 10-х суток наблюдения оставалась достоверно низкой относительно контрольных данных (p < 0,05) и приходила к контрольным цифрам на 30-е сутки. Такое явление получило название синдрома эутиреоидной патологии. В то же время необходимо отметить, что в опытной группе содержание общего трийодтиронина в крови в течение 10-ти суток достоверно превышала уровень данного гормона у животных в группе сравнения (p < 0,05). Данное обстоятельство может быть связано с ранним увеличением общего тироксина и стимуляцией натрия гипохлоритом синтеза белка в печени. Необходимо также отметить и стабилизацию уровня кортизола в крови у животных опытной группы, которое может свидетельствовать об уменьшении выраженности неспецифического системного воспалительного ответа на повреждение.
Заключение. Таким образом, развитие синдрома эутиреоидной патологии у животных с желчным перитонитом направлено на активацию регуляции негеномных эффектов тиреоидных гормонов, в то время как снижение уровня общего трийодтиронина может служить реакцией адаптации на сохранение энергии и белка в организме. В то же время применение натрия гипохлорита при лечении желчного перитонита способствует стабилизации гормонального дисбаланса как за счет повышения уровня кортизола, так и за счет стимуляции синтеза белка в печени. Общеизвестно, что в патогенезе перитонита особое внимание уделяется роли окислительного стресса в инициировании процессов ПОЛ в биологических мембранах. Однако в настоящее время концепция, предполагающая исключительно повреждающее влияние активных форм кислорода на функционирование клетки, пересматривается, в связи с чем широкую известность приобрёл термин «окислительная регуляция», отражающая активную роль окислительно-восстановительной модификации протеинов в регуляции гомеостаза. Отсюда можно предположить, что применение натрия гипохлорита при лечении экспериментального желчного перитонита способствует окислению молекул протеина в крови, которые являются «сигналами», несущими биологическую информацию на структуры гипоталамуса и гипофиза, необходимые для регуляции клеточных функций гомеостаза. Кроме того, нельзя исключить прямого модифицирующего влияния этих веществ непосредственно на железы внутренней секреции. Эти сложные вопросы, несомненно, требуют дальнейшего детального изучения.
Список литературы
- Багненко С.Ф., Мосягин В.Б., Карпова Е.А. Желчный перитонит как осложнение лапароскопической холецистэктомии // Эндоскопическая хирургия. - 2000. - №2. - С. 6-7.
- Зильбер А.П. Клиническая физиология в анестезиологии и реаниматологии. - М.: Медицина, 1984. - 479 с.
- Карли Ф. Метаболический ответ на острый стресс: сборник научных трудов. - Архангельск, 1996. - С. 31-33.
- Карякина Е.В., Белова С.В. Молекулы средней массы как интегральный показатель метаболических нарушений // Клиническая лабораторная диагностика. - 2004. - №3. - С. 3-8.
- Кауфман А.С. Лаборатория гормонального анализа и ее техническое оснащение // Проблемы репродукции. - 1995. - №1. - С. 105-114.
- Коровин А.Я., Выступец В.В., Зайченко Д.Н., Сергеев П.С. и др. Эндоскопическая холецистэктомия при осложненном деструктивном холецистите // Эндоскопическая хирургия. - 2000. - №2. - С. 6.
- Кригер А.Г., Ржебаев К.Э., Воскресенский П.К., Суходулов А.М. и др., Опасности, ошибки, осложнения при лапароскопических операциях на жёлчных путях // Анналы хирургической гепатологии. - 2000. - № 1. - С. 90-98.
- Левит Д.А., Лейдерман И.Н. Острое катаболическое состояние при синдроме системного воспалительного ответа различной этиологии. Попытка клинического анализа // Вестник интенсивной терапии. - 2006. - №2. - С. 9-14.
- Мартов Ю.Б., Подолинский С.Г., Кирковский В.В., Шастый А.Т. Распространенный перитонит. Основы комплексного лечения. - М.: Триада-Х, 1998. - 144 с.
- Петросян Э.А., Сергиенко В.И., Каде А.Х., Петровский А.Н. и др. Способ моделирования желчного перитонита / Патент РФ №2175784. 2001. Бюл. №31.
Библиографическая ссылка
Петросян Э.А., Иванов В.В., Долгов В.Н., Лайпанов А.М., Терещенко О.А., Боташев А.А. ВЛИЯНИЕ НАТРИЯ ГИПОХЛОРИТА НА НЕКОТОРЫЕ ЗВЕНЬЯ ГОМЕОСТАЗА ПРИ ЛЕЧЕНИИ ЭКСПЕРИМЕНТАЛЬНОГО ЖЕЛЧНОГО ПЕРИТОНИТА // Фундаментальные исследования. 2010. № 11. С. 98-102;URL: https://fundamental-research.ru/en/article/view?id=14027 (дата обращения: 16.05.2026).



